
【题目】某水系锂离子电池可实现Li+和Co2+分离回收,其装置如图。25℃时,Co(OH)2的Ksp分别为6.31×10—15,LiOH的溶解度为12.7g.下列说法不正确的是
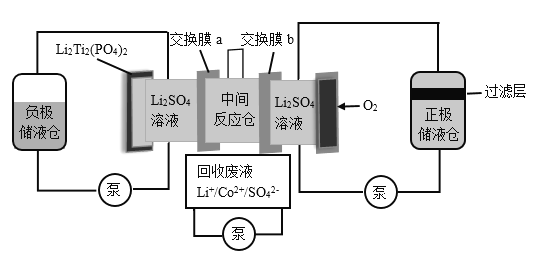
A.负极材料中发生变价的元素是Ti
B.交换膜a为阳离子交换膜
C.负极液和正极液中的c(Li+)均变大
D.在过滤层可收集到Co(OH)2
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】低碳经济成为人们一种新的生活理念,二氧化碳的捕捉和利用是一个重要研究方向, 既可变废为宝,又可减少碳的排放。工业上可用CO2和H2制备被誉为“21世纪的清洁燃料”二甲醚(CH3OCH3):
如在500℃时,在密闭容器中将炼焦中的CO2转化为二甲醚,其相关反应为:
主反应I:2CO2 (g)+6H2(g)![]() CH3OCH3(g)+3H2O(g) △H1
CH3OCH3(g)+3H2O(g) △H1
副反应II:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
(1)已知:①CO(g)+2H2(g)![]() CH3OH(g) △H=-90.1kJ/mol
CH3OH(g) △H=-90.1kJ/mol
②2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H=-24.5kJ/mol
CH3OCH3(g)+H2O(g) △H=-24.5kJ/mol
③CO(g)+H2O(g)![]() CO2(g)+H2(g) △H= -41.0kJ/mol
CO2(g)+H2(g) △H= -41.0kJ/mol
则主反应I的△H1=______。
(2)在一定温度下某密闭容器中按CO2和H2的浓度比为1:3投料进行反应,测得不同时间段部分物质的浓度如下表:

①10-20min 内,CH3OCH3的平均反应速率v(CH3OCH3)=_______。
②根据以上数据计算主反应I的平衡常数K=______(列式,代入数据,不计算结果)。
(3)欲提高CH3OCH3产率的关键的因素是选用合适的催化剂,其原因是_______。
(4)对于反应II,温度对CO2的转化率及催化剂的效率影响如图所示:下列有关说法不正确的是_______。

A.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于Ml
B.温度低于250°C时,随温度升高甲醇的产率增大
C.M点时平衡常数比N点时平衡常数大
D.实际反应应尽可能在较低的温度下进行,以提高CO2的转化
(5)利用太阳能电池将CO2转化为乙烯、丙烯等有机化工原料,其工作原理如图所示。则a为太阳能电池的_______极,写M极上生成丙烯的电极反应式为_________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10mL0.1mol/LNaOH溶液中加入0.1mol/L的一元酸HA溶液,溶液pH的变化曲线如图所下列说法不正确的是
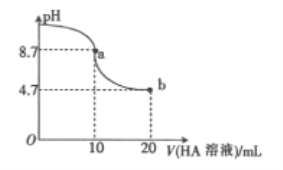
A. a点所示溶液中:c(A-)>c(Na+)>c(OH-)>c(H+)
B. a点所示溶液中:c(Na+)=0.05mol/L
C. pH=7时,c(Na+)=c(A-)
D. b点所示溶液中:c(Na+)<c(A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置进行下列实验,其中不合理的是

A.用CCl4萃取碘水中的碘B.用NaOH溶液除去溴苯中的溴
C.用水除去硬脂酸钠中的甘油D.用饱和Na2CO3溶液除去乙酸乙酯中的乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丹参醇是存在于中药丹参中的一种天然产物。合成丹参醇的部分路线如下:
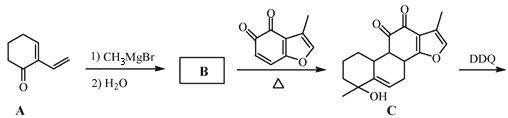
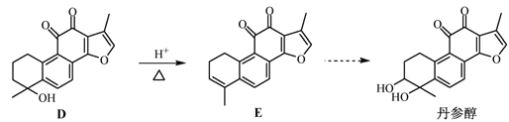
已知:①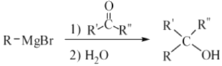 ②
②![]()
(1)A中的官能团名称为羰基和_______________。
(2)D![]() E的反应类型为__________反应。
E的反应类型为__________反应。
(3)B的分子式为C9H14O,则B的结构简式为_______________。
(4)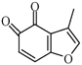 的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:_______________。
的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:_______________。
①能与FeCl3溶液发生显色反应; ②能发生银镜反应;
③核磁共振氢谱中有4个吸收峰,峰面积比为1:1:2:2。
(5)请补全以![]() 和
和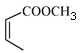 为原料制备
为原料制备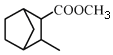 的合成路线流程图(无机试剂任用)。
的合成路线流程图(无机试剂任用)。
![]() 中间产物①__________
中间产物①__________![]() 中间产物②__________
中间产物②__________![]() 中间产物③__________反应物④ _______反应条件⑤__________
中间产物③__________反应物④ _______反应条件⑤__________![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫及其化合物在工农业生产中有着重要作用.回答下列问题
(1)工业制硫酸,接触室中发生反应的化学方程式为___________。下列可提高SO2平衡转化率的措施是___________。(填标号)
A.降低温度 B.减小压强 C.延长反应时间 D.增大O2的投料
(2)工业上可用Fe2(SO4)3溶液吸收SO2,该过程的离子方程式为________。为实现吸收液的再生,可通入_________。
(3)用如图装置脱除废烟气中的SO2和废水中的Cu2+,该方法总反应的化学方程式为___________。含Cu2+的废水应置于___________室(填“a”或“b”)。
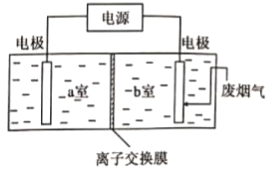
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在![]() 溶液中逐滴加入
溶液中逐滴加入![]() 溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示
溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示![]() 因逸出未画出,忽略因气体逸出引起的溶液体积变化
因逸出未画出,忽略因气体逸出引起的溶液体积变化![]() ,下列说法正确的是
,下列说法正确的是![]()
![]()
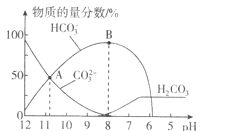
A.在![]() 溶液中:
溶液中:![]()
B.当溶液的pH为7时,溶液的总体积为![]()
C.在B点所示的溶液中,离子浓度最大的是![]()
D.在A点所示的溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】38.4 mg铜跟适量的浓硝酸反应,铜全部作用后,共收集到22.4 mL(标准状况下)气体,反应消耗的HNO3的物质的量可能是 ( )
A.1.0×10-3 molB.1.6×10-3 molC.2.2×10-3 molD.2.4×10-3 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L恒容密闭容器中,发生反应A(g)+B(g) ![]() 2C(g)+D(s) △H=-akJ·mol-1,有关实验内容和结果分别如表和如图所示。下列说法正确的是( )
2C(g)+D(s) △H=-akJ·mol-1,有关实验内容和结果分别如表和如图所示。下列说法正确的是( )
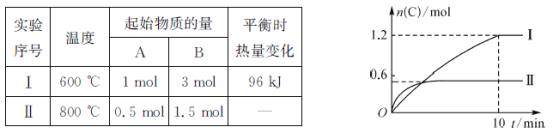
A.实验I中,10 min内平均速率υ(B)=0.06mol·L-1·min-1
B.600℃时,上述热化学方程式中a=160
C.600℃时,该反应的平衡常数K=0.45
D.向实验II的平衡体系中再充入0.5molA和1.5molB,A的转化率增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com