
【题目】下列做法不能减少大气污染的是
A.大力发展清洁能源,烟气脱硫
B.大力发展私家车,减少公共交通
C.利用太阳能、风能等替代化石能源
D.提倡多使用自行车
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案科目:高中化学 来源: 题型:
【题目】电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。
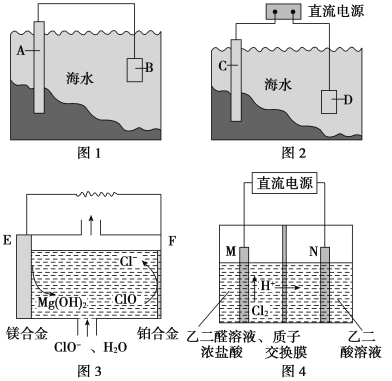
(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择____________(填字母序号)。
a.碳棒 b.锌板 c.铜板
用电化学原理解释材料B需定期拆换的原因:_________________________。
(2)图2中,钢闸门C做____________极。用氯化钠溶液模拟海水进行实验,D为石墨块,则D上的电极反应式为____________,检测该电极反应产物的方法是___________________。
(3)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁﹣次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①E为该燃料电池的__________极(填“正”或“负”)。F电极上的电极反应式为________________________。
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因_______________________。
(4)乙醛酸(HOOC-CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图4所示,该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
①N电极上的电极反应式为____________________________。
②若有2 mol H+通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为____________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一可逆反应2A(g)+3B(g)![]() 4C(g)+D(g),已知起始浓度c(A)=2mol/L,c(B)=3mol/L,c(C)=c(D)=0,反应开始20min后达到平衡状态,此时D的平衡浓度为0.5mol/L,则下列说法不正确的是
4C(g)+D(g),已知起始浓度c(A)=2mol/L,c(B)=3mol/L,c(C)=c(D)=0,反应开始20min后达到平衡状态,此时D的平衡浓度为0.5mol/L,则下列说法不正确的是
A.前20 min的平均反应速率v(C)=0.1 mol/(Lmin) B.A的转化率为50%
C.C的平衡浓度c(C)=4 mol/L D.B的平衡浓度c(B)=1.5 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,N2(g)和H2(g)反应生成2molNH3(g)放出92.4kJ热量。在相同条件下向密闭容器中通入1molN2和3molH2,达到平衡时放出热量为Q1kJ;向另一体积相同的密闭容器中通入0.5molN2、1.5molH2和1molNH3,相同条件下达到平衡时放出热量为Q2kJ。则下列关系式正确的是
A. 2Q2=Q1=92.4 B. Q2<Q1<92.4
C. Ql<Q2<92.4 D. Ql=Q2<92.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温下,0.1mol/L 的CH3COOH溶液中有l%的CH3COOH分子发生电离,则溶液的pH= ;可以使0.10 mol·L-1 CH3COOH的电离程度增大的是
a.加入少量0.10 mol·L-1的稀盐酸
b.加热CH3COOH溶液
c.加水稀释至0.010 mol·L-1
d.加入少量冰醋酸
e.加入少量氯化钠固体
f.加入少量0.10 mol·L-1的NaOH溶液
(2)将等质量的锌投入等体积且pH均等于3的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积:V(盐酸)_________V(醋酸)(填“>”、“<”或“=”)。
(3)0.1mol/L的某酸H2A的pH=4,则H2A的电离方程式为 。
(4)25℃时,将pH=9的NaOH溶液与pH=4的盐酸溶液混合,若所得混合溶液的pH=6,则NaOH溶液与盐酸溶液的体积比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图X是直流电源。Y槽中c、d为石墨棒,Z槽中e、f是质量相同的铜棒。接通电路后,发现d附近显红色。
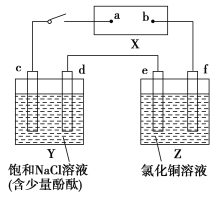
(1)①电源上b为____________极(用“正”、“负”、“阴”或“阳”填空)。
②Z槽中e为____________极(同上)。
③连接Y、Z槽线路中,电子流动的方向是d____________e(用“→”或“←”填空)。
(2)①写出c极上反应的电极反应式:_______________________________。
②写出Y槽中总反应的化学方程式:________________________________。
③写出Z槽中e极上反应的电极反应式:_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】基态Fe原子有________个未成对电子。Fe3+的电子排布式为________。可用硫氰化钾检验Fe3+,形成的配合物的颜色为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列做法不正确的是( )
A. Na2O2用作呼吸面具的供氧剂
B. NaHCO3的热稳定性大于Na2CO3
C. 乙醇可与金属钠反应放出氢气
D. 金属钠着火时,用细沙覆盖灭火
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com