
����Ŀ��I��ͨ��״���£�X��Y��Z��������̬���ʣ�X�����Ԫ���ǵ�������ԭ�Ӱ뾶��С��Ԫ�أ�ϡ������Ԫ�س��⣩��Y��Z����Ԫ��R��ɣ�Y��Ҫ�ֲ���ƽ��������У��ǵ���ı���ɡ��
��1��Y��Z�Ĺ�ϵ�ǣ�ѡ����ĸ��__________��
a��ͬλ�� b��ͬϵ�� c��ͬ�������� d��ͬ���칹��
��2����Y�Ͷ�������ֱ�ͨ��Ʒ����Һ������ʹƷ����ɫ����������ɫ����Һ������ߵ�ʵ�鷽��___________��
��3��ʵ�����Ʊ�X�Ļ�ѧ����ʽ_____________________________��
II�����ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�á���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺

��4����X��Y���Ƕ��Ե缫��a�DZ���NaCl��Һ��ʵ�鿪ʼʱ��ͬʱ�����߸����뼸�η�̪��Һ����
�ٵ�����X���ϵĵ缫��ӦʽΪ_____________����X�������۲쵽��������_________��
�ڣٵ缫�ϵĵ缫��ӦʽΪ_________________������õ缫��Ӧ����ķ�����___________��
��5����Ҫ�õ�ⷽ��������ͭ�����Һaѡ��CuSO4��Һ����
��X�缫�IJ�����__________���缫��ӦʽΪ________________________________��
��Y�缫�IJ�����__________���缫��ӦʽΪ________________________________����˵�������ʷ����ĵ缫��Ӧ����д����
���𰸡� c ������ɫ�����Һ������Һ�ָ���ɫ����ԭͨ������ΪSO2������Һ����죬��ԭͨ��������O3 MnO2+4HCl(Ũ) ![]() MnCl2+Cl2��+2H2O 2H++2e��==H2�� �ų����壬��Һ��� 2Cl����2e��==Cl2�� ��ʪ��ĵ⻯�ص�����ֽ����Y�缫��������ֽ����ɫ ��ͭ Cu2++2e��==Cu ��ͭ Cu��2e��==Cu2+
MnCl2+Cl2��+2H2O 2H++2e��==H2�� �ų����壬��Һ��� 2Cl����2e��==Cl2�� ��ʪ��ĵ⻯�ص�����ֽ����Y�缫��������ֽ����ɫ ��ͭ Cu2++2e��==Cu ��ͭ Cu��2e��==Cu2+
��������I��ͨ��״���£�X��Y��Z��������̬���ʣ�X�����Ԫ���ǵ�������ԭ�Ӱ뾶��С��Ԫ�أ�ϡ������Ԫ�س��⣩��X��Cl��Y��Z����Ԫ��R��ɣ�Y��Ҫ�ֲ���ƽ��������У��ǵ���ı���ɡ�����Y�dz�������Z��������R����Ԫ�ء�
��1�������ͳ���������Ԫ���γɵĵ��ʣ�����Ϊͬ�������壬��ѡc����2���������������ԣ�ʹƷ����Һ��ɫ����ɫ�Dz�����ġ�SO2ʹƷ����Һ��ɫ�ǿ���ģ���������ߵ�ʵ�鷽���Ǽ�����ɫ�����Һ������Һ�ָ���ɫ����ԭͨ������ΪSO2������Һ����죬��ԭͨ��������O3����3��ʵ�����Ʊ������Ļ�ѧ����ʽΪMnO2+4HCl(Ũ)![]() MnCl2+Cl2��+2H2O��
MnCl2+Cl2��+2H2O��
II����4����X�缫���Դ�ĸ�������������������Һ�е������ӷŵ磬��˵�����X���ϵĵ缫��ӦʽΪ2H++2e��==H2���������ӷŵ��ƻ���ˮ�ĵ���ƽ�⣬X�缫������������Ũ�ȴ��������ӣ���Һ�Լ��ԣ�������X�������۲쵽�������Ƿų����壬��Һ��졣�ڣٵ缫����������Һ�е������ӷŵ磬�缫��ӦʽΪ2Cl����2e��==Cl2������������ǿ�����ԣ�����õ缫��Ӧ����ķ����ǰ�ʪ��ĵ⻯�ص�����ֽ����Y�缫��������ֽ����ɫ����5���ٴ�ͭ����ʱ��ͭ����������ͭ�����������Դ����������������X�缫�IJ����Ǵ�ͭ���缫��ӦʽΪCu2++2e��==Cu����Y�缫�IJ����Ǵ�ͭ���缫��ӦʽΪCu��2e��==Cu2+��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼���γɻ�������������Ԫ�أ��䵥�ʼ������������������������Ҫ��Դ���ʡ�
��ش��������⣺
(1)�л���M����̫������տ�ת����N��ת���������£�
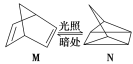 ��H����88.6 kJ��mol��1
��H����88.6 kJ��mol��1
��M��N��ȣ����ȶ����� ��
(2)��֪CH3OH(l)��ȼ����Ϊ238.6 kJ��mol��1��CH3OH(l)��![]() O2(g)=CO2(g)��2H2(g) ��H����a kJ��mol��1����a 238.6(�����������������)��
O2(g)=CO2(g)��2H2(g) ��H����a kJ��mol��1����a 238.6(�����������������)��
(3)ʹCl2��H2O(g)ͨ�����ȵ�̿�㣬����HCl��CO2������1 mol Cl2���뷴Ӧʱ�ͷų�145 kJ������д���÷�Ӧ���Ȼ�ѧ����ʽ�� ��
(4)����͵�������ı������������ʡ���ʯī�����ۺͶ������Ѱ�һ����������ڸ��������գ��������ʿ������²��ϣ�4Al(s)��3TiO2(s)��3C(s)=2Al2O3(s)��3TiC(s)����H����1 176 kJ��mol��1����Ӧ�����У�ÿת��1 mol���ӷų�������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������⣺�����£���20.0g 14%��NaCl��Һ��30.0g 24%��NaCl��Һ��ϣ���Ϻ�õ��ܶ�Ϊ1.17g/cm3����Һ������㣺
�ٻ�Ϻ���Һ��NaCl������������
�ڻ�Ϻ���Һ��NaCl�����ʵ���Ũ�ȣ�
����1000gˮ�мӶ��� mol NaCl������ʹ��Ũ��ǡ����������Ϻ���Һ��Ũ����ȣ��������һλС������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ҫ�����ȶ��ĸ߷е�Һ̬�л���͵ͷе�����ʵĻ��������ᴿһ��ʹ�õķ����ǣ� ��
A.����
B.�ؽᾧ
C.����
D.��ȡ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����4.0gNaOH��������ˮ���100mL��Һ�����ܶ�Ϊ0.20g/mL��
��1������Һ��NaOH �����ʵ���Ũ��Ϊ
��2������Һ��NaOH����������Ϊ
��3���Ӹ���Һ��ȡ��10mL������NaOH�����ʵ���Ũ��Ϊ �� ��NaOH������Ϊ ��
��4����ȡ����10mL��Һ��ˮϡ�͵�100mL��ϡ�ͺ���Һ��NaOH�����ʵ���Ũ��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������NaOH��������250mL 1.25mol/L��NaOH��Һ����ղ��ش����⣺
��1������ʱ�����õ������У��ձ����������� ��
��2������ʱ������ȷ�IJ���˳���ǣ���ĸ��ʾ��ÿ����ĸֻ����һ�Σ���
A����30mLˮϴ���ձ�2��3�Σ�ϴ��Һ��ע������ƿ����
B������ƽȷ��ȡ�����NaOH����������������ˮ��Լ30mL�����ò���������������ʹ�����ܽ�
C��������ȴ��NaOH��Һ�ز�����ע��250mL������ƿ��
D��������ƿ�ǽ����ߵ�ҡ��
E�����ý�ͷ�ιܼ�ˮ��ʹ��Һ����ǡ����̶�����
F������������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶�1��2cm��
��3���������Ƶ���ҺŨ��ƫ�͵��� ��
A.����NaOHʱ���������������
B.������ƿ��ת����Һʱ��ʵ�鲽��C��������Һ����������ƿ����
C.������ˮʱ���������˿̶���
D.����ʱ���ӿ̶���
E.����ǰ������ƿ������������ˮ
��4��ijͬѧ���ù���Na2CO3������������Һͬ�����ͬŨ�ȵ���Һ������ͼ��ʾ�����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ���о�С����̽��CuSO4��Һ��Na2CO3��Һ��ϲ���������ɫ������ɣ�С���������ʵ��̽����
��������衿
����1������ΪCu(OH)2
����2������Ϊ
����3������Ϊ��ʽ̼��ͭ[��ѧʽ�ɱ�ʾΪnCuCO3mCu(OH)2]
���������ϡ���������һ�ֳ������Ⱦ��ֽ⣨����������ᾧˮ����
�����ʳɷ�̽����
����1������������Һ���ˣ�������ˮϴ�ӣ�������ˮ�Ҵ�ϴ��
����2����ͬѧȡһ�������壬�����������õ���ͼװ�ã��г�����δ���������ж���ʵ�顣

��ش��������⣺
��1������2�еij���Ϊ ��
��2������1�г���ΪCu(OH)2������������ ��
��3����ˮ�Ҵ�ϴ�ӵ�Ŀ��____ __��
��4������Ӧ��A������ɫ�����ڣ�C������������֤������______����д��ţ�������
��5����ͬѧ��ΪֻҪ����ͼ��Bװ�õ��Լ����� �Լ������֤�������м��衣
��6����ͬѧ����B�Լ�����֤����3������ʵ�������� ��
��7���ڼ���3������ǰ���£�ijͬѧ������Ba(OH)2����Ca(OH)2���ⶨ����ɫ����Ļ�ѧʽ������ȡ����ɫ��������Ϊ27.1g��ʵ�������װ��B����������2.7g��C�еIJ�������������Ϊ19.7g���������ɫ����Ļ�ѧʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ϊһ������ԴӦ�ù㷺����ش��������⣺
��1����¯ұ�������У������ڴ���Ӧ���в���ˮú����CO��H2����ԭ���������йط�ӦΪ��
CH4��g��+CO2(g) =2CO��g��+2H2��g�� ��H=260kJ��mol-1
2CO(g)+O2(g) = 2CO2��g�� ��H= -566kJ��mol-1
��CH4��O2��Ӧ����CO��H2���Ȼ�ѧ����ʽΪ____________________
��2������ͼ��ʾ��װ�â�Ϊ����ȼ�ϵ�أ��������ҺΪKOH��Һ��ͨ��װ�â�ʵ�������϶�ͭ

��a��Ӧͨ��_________(��CH4��O2)��b���缫�Ϸ����ĵ缫��Ӧʽ��______��
�ڵ�ƽ�����װ�â�����Һ��pH______������д���С�䣬��ͬ����װ�â���Cu2+�����ʵ�����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ȷ�Ӧ���ǣ� ��
A. ����ȼ�� B. �������������Ƶ��кͷ�Ӧ
C. �ڻ�ҩ��ը D. Ba(OH)2��8H2O��NH4Cl��Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com