
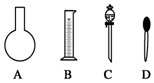
 ʵ����Ҫ0.80mol•L-1 NaOH��Һ475mL��0.40mol•L-1������Һ500mL��������������Һ����������ش��������⣺
ʵ����Ҫ0.80mol•L-1 NaOH��Һ475mL��0.40mol•L-1������Һ500mL��������������Һ����������ش��������⣺���� ��1������ʵ������IJ��裨���㡢��������ȡ�����ܽ⣨ϡ�ͣ�����ȴ����Һ��ϴ�ӡ����ݡ�ҡ�ȵȲ�����ѡ����Ҫ�����������жϲ���Ҫ��������ȱ�ٵ�������
��2������ƿΪ�����ض������һ�����ʵ���Ũ����Һ��ר������������ϡ��Ũ��Һ�����������ܽ���塢������Һ�ȣ�
��3������n=cVm������Ҫ���������������������������ʵ����ʵ�������Һ�����Ӱ�죬����C=$\frac{n}{V}$������������
��4������C=$\frac{1000�Ѧ�}{M}$����Ũ��������ʵ���Ũ�ȣ�������Һϡ���������ʵ����ʵ������������ҪŨ����������ݴ���ѡ����Ͳ���
��� �⣺��1������ʵ������IJ��裺���㡢��������ȡ�����ܽ⣨ϡ�ͣ�����ȴ����Һ��ϴ�ӡ����ݡ�ҡ�ȵȲ������ù�������һ�����ʵ���Ũ����Һ�õ���������������ƽ��Կ�ס��ձ���������������ƿ����ͷ�ιܣ�
��Ũ��Һ����һ�����ʵ���Ũ��ϡ��Һ�õ�����������Ͳ���ձ���������������ƿ����ͷ�ιܣ�����500mL��ҺӦѡ��500mL����ƿ��
���Կ϶�����Ҫ����AԲ����ƿ��C��Һ©������ȱ�ٵ��������ձ�����������500mL����ƿ��
�ʴ�Ϊ��AC���ձ�����������500mL����ƿ��
��2������ƿֻ����������һ�����ȷŨ�ȵ���Һ���������ƻ��������ƿ������µ����������Һ�壬����ϡ�ͻ��ܽ�ҩƷ���������������ܽ�������ʣ�
�ʴ�Ϊ��BCEF��
��3����Ҫ0.80mol•L-1 NaOH��Һ475mL��Ӧѡ��500mL����ƿ��ʵ������500mL��Һ����Ҫ������������Ϊ��0.8mol/L��0.5L��40g/mol=16.0g��
������ʱ���ӿ̶��ߣ�������Һ���ƫС����������ҺŨ�ȴ���0.8mol•L-1��������ʱ������������ˮ����������ƿ�⣬�����ʵ����ʵ�������Һ������������Ӱ�죬��������ҺŨ�� ����0.8mol•L-1��
�ʴ�Ϊ��16.0�����ڣ����ڣ�
��4����������Ϊ98%�ܶ�Ϊ1.84g/mL���������ʵ���Ũ��C=$\frac{1000��1.84��98%}{98}$=18.4mol/L������ҪŨ�������ΪV����������Һϡ���������ʵ����ʵ�������ã�18.4mol/L��V=500mL��0.40mol/L�����V=10.9mL����ȡ10.9mLŨ���ᣬӦѡ��15mL��Ͳ��
�ʴ�Ϊ��10.9��15��
���� ���⿼����һ�����ʵ���Ũ����Һ�����ƣ��Ѷ��еȣ���ȷ����ԭ�������������ǽ���ؼ���ע�����c=$\frac{n}{V}$�����������ķ����ͼ��ɣ����ؿ���ѧ��ʵ���������������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��� | ʵ����� | ʵ������ | ��������� |
| A | ��Ũ�Ⱦ�Ϊ0.1mol•L-1 NaCl��NaI�����Һ�еμ�����AgNO3��Һ | ���ֻ�ɫ���� | Ksp��AgCl����Ksp��AgI�� |
| B | ��������Һ�м�������NaCl��Һ���ټ�KI��Һ | �ȵõ���ɫ�������Ϊ��ɫ���� | Ksp��AgCl����Ksp��AgI�� |
| C | �����pH=3��HA��HB������ֱ���������п��Ӧ����ˮ���ռ����� | ��ͬʱ���ڣ�HA�ռ����������� | HA������ |
| D | �ýྻ�IJ�˿պ����Һ������ɫ��Ӧ | ����ʻ�ɫ | ��Һ�к�Na+������K+ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ˮ����Fe3++H2O?Fe��OH��3+3H+ | |
| B�� | ������ӡˢ��·�ĸ�ʴҺ��2Fe3++Cu�T2Fe2++Cu2+ | |
| C�� | ��С�մ���Һ��Ӧ��Fe3++3HCO3-�TFe��OH��3��+3CO2�� | |
| D�� | ��KSCN ��Һ���ɫ��Fe3++3SCN-�TFe��SCN��3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
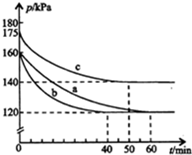 ���ݻ�Ϊ2L���ܱ������н��з�Ӧ��AX3��g��+X2��g��?AX5��g����H=QkJ/mol����ʼʱAX3��X2��Ϊ1.0mol����Ӧ�ڲ�ͬ�����½��У���Ӧ��ϵ��ѹǿ��ʱ��ı仯��ͼ��ʾ�������й�˵������ȷ���ǣ�������
���ݻ�Ϊ2L���ܱ������н��з�Ӧ��AX3��g��+X2��g��?AX5��g����H=QkJ/mol����ʼʱAX3��X2��Ϊ1.0mol����Ӧ�ڲ�ͬ�����½��У���Ӧ��ϵ��ѹǿ��ʱ��ı仯��ͼ��ʾ�������й�˵������ȷ���ǣ�������| A�� | Q��0 | |
| B�� | ��ʵ��a��ȣ�ʵ��b�����˴��� | |
| C�� | ʵ��b�����£��÷�Ӧ��ƽ�ⳣ��K=2 | |
| D�� | ʵ��c�ӷ�Ӧ��ʼ���ﵽƽ��ʱ��ƽ����Ӧ����Ϊv��AX5��=4.0��10-3mol/��L•min�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
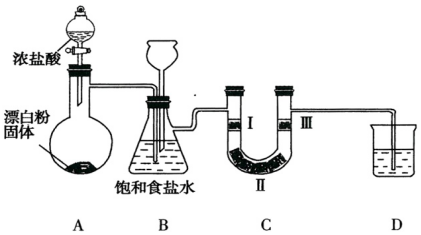
| ��� | I | II | III |
| a | �������ɫ���� | ��ʯ�� | ʪ�����ɫ���� |
| b | �������ɫ���� | ��ˮ����ͭ | ʪ�����ɫ���� |
| c | ʪ�����ɫ���� | Ũ���� | �������ɫ���� |
| d | ʪ�����ɫ���� | ��ˮ�Ȼ��� | �������ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com