
【题目】反应N2O4(g) ![]() 2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是( )
2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是( )

A. A、C两点的反应速率:A>C
B. A、C两点气体的颜色:A深,C浅
C. A、B两点气体的平均相对分子质量:A>B
D. B、C两点化学平衡常数:B<C
【答案】D
【解析】A、A、C两点温度相同,C点压强大于A点,所以C点反应速率大于A点反应速率,A错误;B、C点压强大于A点压强,所以C点容器体积小于A 点容器体积,所以C点NO2的浓度大于A点NO2的浓度,C点颜色深,A点浅,B错误;C、A、B两点压强相同,B点到A点NO2体积分数增大,平衡正向移动,气体的总物质的量增大,又由于气体的总质量不变,所以混合气体的平均相对分子质量减小,即A、B两点气体的平均相对分子质量:B > A,C错误;D、A、B两点压强相同,B点到A点NO2体积分数增大,平衡正向移动,所以B点的平衡常数小于A点的平衡常数,A、C两点温度相同,A、C两点平衡常数相同,所以B点的平衡常数小于C点的平衡常数,D正确。正确答案为D。


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:
【题目】25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( ) 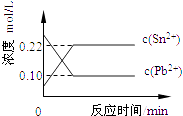
A.往平衡体系中加入金属铅后,c(Pb2+)增大
B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小
C.升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0
D.25℃时,该反应的平衡常数K=2.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,2.0×10﹣3molL﹣1氢氟酸的水溶液中,调节溶液pH(忽略溶液体积变化)得到的[HF]、[F﹣]与溶液pH的变化关系如下图.下列叙述不正确的是( ) (提示:Ka(CH3COOH)=1.8×10﹣5molL﹣1 , Ksp(CaF2)=1.5×10﹣10mol3L﹣3)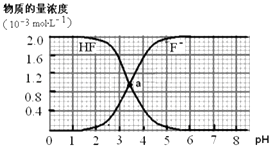
A.两条曲线交点a对应溶液的[F﹣]=[HF]
B.加入NaOH溶液至pH=7,溶液中[F﹣]=[Na+]
C.常温下HF的电离常数Ka(HF)>Ka(CH3COOH)
D.pH=4时,加入CaCl2固体使[Ca2+]=2.0×10﹣3molL﹣1 , 无CaF2沉淀析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与有机物的结构、性质的有关叙述中正确的是( )
A.天然油脂的主要成分是高级脂肪酸
B.分馏、干馏都是物理变化,裂化、裂解都是化学变化
C.乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色
D.乙酸与乙醇可以发生酯化反应,又均可与金属钠发生置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.2molL﹣1的一元酸HA与等浓度NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度所示,下列说法正确的是( ) 
A.HA为强酸
B.该混合溶液pH=7.0
C.该混合溶液中:c(A﹣)+c(Y)=c(Na+)
D.图中X表示HA,Y表示OH﹣ , Z表示H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时在10mL 0.1molL﹣1Na2CO3溶液中逐滴加入0.1molL﹣1HCl溶液20mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示.下列说法不正确的是( ) 
A.Na2CO3溶液中c(Na+)═2[c(CO32﹣)+c(HCO3﹣)+c(H2CO3)]
B.a、b曲线分别代表的是HCO3﹣、H2CO3量的变化情况
C.A点时:c(Na+)>c(CO32﹣)═c(HCO3﹣)>c(H+)>c(OH﹣)
D.B点时加入盐酸的体积为10mL,两者恰好完全反应生成NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质转化在一定条件下不能一步实现的是
A. Na→Na2O2→Na2CO3 B. Cu→CuO→CuSO4
C. Al2O3→Al(OH)3→Al3+ D. Fe(OH)3→Fe2O3→ Fe3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com