
【题目】有一无色透明溶液,欲确定是否含有下列离子:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,取该溶液的实验如下:
,取该溶液的实验如下:
实验步骤 | 实验现象 |
| 溶液变红色 |
| 有无色气体产生,气体遇空气可以变成红棕色 |
| 有白色沉淀生成 |
| 有稳定的白色沉淀生成,且不溶于稀硝酸 |
| 有白色沉淀生成,当NaOH过量时,沉淀部分溶解 |
由此判断,下列说法正确的是![]()
A.根据实验![]() 可以确定溶液中不含有
可以确定溶液中不含有![]() 和
和![]() ,因为这二个离子相对应的酸为弱酸
,因为这二个离子相对应的酸为弱酸
B.溶液中一定存在的离子是![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ;溶液中肯定不存在的离子是:
;溶液中肯定不存在的离子是:![]() 、
、![]() 、
、![]() 、
、![]()
C.为进一步确定其它离子,应该补充焰色反应的实验来检验![]() 就可以
就可以
D.通过实验![]() 和
和![]() 就可以确定溶液中一定含有
就可以确定溶液中一定含有![]() ,一定不含有
,一定不含有![]() 、
、![]() 、
、![]() ,所以实验步骤
,所以实验步骤![]() 的设计是错误的
的设计是错误的
【答案】D
【解析】
因是一无色透明溶液,则不含有![]() ,由
,由![]() 取少量该溶液,加几滴甲基橙,溶液显红色,说明溶液显示酸性,所以
取少量该溶液,加几滴甲基橙,溶液显红色,说明溶液显示酸性,所以![]() 不存在;由
不存在;由![]() 取少量该溶液加热浓缩,加Cu片和浓硫酸,加热有无色气体产生,气体
取少量该溶液加热浓缩,加Cu片和浓硫酸,加热有无色气体产生,气体![]() 遇空气可以变成红棕色
遇空气可以变成红棕色![]() 二氧化氮
二氧化氮![]() ,说明溶液中含有
,说明溶液中含有![]() ,则一定不含有
,则一定不含有![]() ;由
;由![]() 取少量该溶液,加
取少量该溶液,加![]() 溶液,有白色沉淀生成,则含有
溶液,有白色沉淀生成,则含有![]() ;由
;由![]() 取
取![]() 中的上层清液,加
中的上层清液,加![]() 溶液,有稳定的白色沉淀生成,且不溶于稀硝酸,则含有
溶液,有稳定的白色沉淀生成,且不溶于稀硝酸,则含有![]() ,由于实验(3)所加的氯化钡溶液中含有
,由于实验(3)所加的氯化钡溶液中含有![]() ,所以原溶液中的
,所以原溶液中的![]() 是否存在不确定;由
是否存在不确定;由![]() 取少量该溶液,加入NaOH溶液有白色沉淀生成,当NaOH过量时,沉淀部分溶解,则含有铝离子、镁离子。则
取少量该溶液,加入NaOH溶液有白色沉淀生成,当NaOH过量时,沉淀部分溶解,则含有铝离子、镁离子。则
A、根据实验![]() 可以确定溶液中不含有
可以确定溶液中不含有![]() ,HI是强酸,不能确定I-是否存在,故A错误;
,HI是强酸,不能确定I-是否存在,故A错误;
B、溶液中一定存在的离子是![]() 、
、![]() 、
、![]() ,溶液中肯定不存在的离子是
,溶液中肯定不存在的离子是![]() 、
、![]() 、
、![]() 、
、![]() ,Cl-不能确定,故B错误;
,Cl-不能确定,故B错误;
C、钾离子、氯离子都是无法判断的离子,为进一步确定钾离子,应该补充焰色反应的实验来检验,但是氯离子的检验需要沉淀法,故C错误;
D、通过实验![]() 和
和![]() 就可以确定溶液中一定含有
就可以确定溶液中一定含有![]() ,和其反应的离子不存在,即一定不含有
,和其反应的离子不存在,即一定不含有![]() 、
、![]() 、
、![]() ,实验
,实验![]() 加了氯化钡溶液,含有氯离子,实验
加了氯化钡溶液,含有氯离子,实验![]() 再加硝酸银溶液检验氯离子是无效的,故D正确。
再加硝酸银溶液检验氯离子是无效的,故D正确。
故选D。


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】在一定条件下,将3mol A和1mol B两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g) + B(g) ![]() xC(g) + 2D(g)。2min末该反应达到平衡,生成0.8mol D,并测得C的浓度为0.2mol·L-1。下列判断错误的是
xC(g) + 2D(g)。2min末该反应达到平衡,生成0.8mol D,并测得C的浓度为0.2mol·L-1。下列判断错误的是
A. x=1
B. B的转化率为50%
C. 2min内A的反应速率为0.3mol·L-1·min-1
D. 若混合气体的平均相对分子质量不变,则表明该反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() ,
,![]() 。下列关于难溶物之间转化的说法中错误的是
。下列关于难溶物之间转化的说法中错误的是
A.AgCl不溶于水,不能转化为AgI
B.两种难溶物的![]() 相差越大,难溶物就越容易转化为更难溶的物质
相差越大,难溶物就越容易转化为更难溶的物质
C.AgI比AgCl更难溶于水,所以AgCl可以转化为AgI
D.常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于![]() ×10-11
×10-11
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W的原子序数依次增大.X原子核内没有中子;Z与W在周期表中同主族,且Y、Z和W三种元素的原子最外层电子数之和为17;X、Y形成的化合物M的水溶液呈碱性.则下列说法不正确的是![]()
A.原子半径:![]()
B.标准状况下的![]() LM溶于水,所得溶液
LM溶于水,所得溶液![]()
C.![]() 能使湿润的淀粉KI试纸变蓝
能使湿润的淀粉KI试纸变蓝
D.一定条件下,Cu可与W的最高价氧化物对应水化物发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:2NO2(g)![]() 2NO(g)+O2(g)在密闭容器中反应,达到平衡状态的标志是( )
2NO(g)+O2(g)在密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时,生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
A. ①④⑥B. ②③⑤C. ①③④D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是应用广泛的金属。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:

注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为_____________________。
(2)向“过滤Ⅰ”所得滤液中加入NaHCO3溶液,溶液的pH_________ (填“增大”、“不变”或“减小”)。
(3)“电解Ⅰ”是电解熔融Al2O3,电解过程中作阳极的石墨易消耗,原因是___________。
(4)“电解Ⅱ”是电解Na2CO3溶液,原理如图所示。阳极的电极反应式为_____________________,阴极产生的物质A的化学式为____________。

(5)铝粉在1000℃时可与N2反应制备AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.02mol·L—1的HCN溶液与0.02mol·L—1的NaCN溶液等体积混合,已知混合溶液中C(CN-)<C(Na+),则下列关系中,正确的是:
A.C(Na+)>C(CN-)>C( H+)>C(OH-)
B.C(HCN)+C (CN-)=0.04mol·L-1
C.C(CN-)>C(HCN)
D.C(Na+)+C(H+)= C(CN-)+C(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是一种新型的绿色能源,又是一种重要的化工原料。以生物材质(以C计)与水蒸气反应制取H2是一种低耗能,高效率的制H2方法。该方法由气化炉制造H2和燃烧炉再生CaO两步构成。气化炉中涉及的反应有:
Ⅰ.C(s)+H2O(g)![]() CO(g)+H2(g) K1;
CO(g)+H2(g) K1;
Ⅱ.CO(g)+H2O(g)![]() CO2(g)+H2(g) K2;
CO2(g)+H2(g) K2;
Ⅲ.CaO(s)+CO2(g)![]() CaCO3(s) K3;
CaCO3(s) K3;
燃烧炉中涉及的反应为:
Ⅳ.C(s)+O2(g)=CO2;
Ⅴ.CaCO3(s)=CaO(s)+CO2(g)。
(1)氢能被视为最具发展潜力的绿色能源,该工艺制H2总反应可表示为C(s)+2H2O(g)+CaO(s)![]() CaCO3(s)+2H2(g),其反应的平衡常数K=____(用K1、K2、K3的代数式表示)。
CaCO3(s)+2H2(g),其反应的平衡常数K=____(用K1、K2、K3的代数式表示)。
(2)在一容积可变的密闭容器中进行反应Ⅰ,恒温恒压条件下,向其中加入1.0mol炭和1.0mol水蒸气,达到平衡时,容器的体积变为原来的1.25倍,平衡时水蒸气的平衡转化率为_____;向该容器中补充amol炭,水蒸气的转化率将_____(填“增大”、“减小”或“不变”)。
(3)对于反应Ⅲ,若平衡时再充入CO2,使其浓度增大到原来的2倍,则平衡_____移动( 填“向右”、“向左”或“不”);当重新平衡后,CO2浓度___(填“变大”、“变小”或“不变”)。
(4)一种新型锂离子二次电池——磷酸铁锂(LiFePO4)电池。作为正极材料的磷酸铁锂在充、放电时的局部放大示意图如图,写出该电池充电时的阳极电极反应式:______。
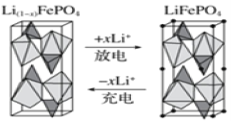
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作或方法正确的是( )
A.用湿润的蓝色石蕊试纸检验![]()
B.烧碱属于离子化合物,熔点较高,实验室中可选用石英坩埚熔化烧碱
C.滴定时,左手控制滴定管活塞,右手摇动锥形瓶,眼睛注视滴定管中液面变化
D.用![]() 从碘水中萃取碘,有一步操作为“将分液漏斗倒转过来振荡,使两种液体充分接触”
从碘水中萃取碘,有一步操作为“将分液漏斗倒转过来振荡,使两种液体充分接触”
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com