
【题目】在密闭容器中,一定量混合气体发生反应xA(g)+yB(g)![]() pC(g)+qD(g),平衡时测得B的浓度为1.0 mol·L-1。保持温度不变,将容器的体积压缩到原来的一半,再次达到平衡时,测得B的浓度为1.5 mol·L-1。下列有关判断正确的是
pC(g)+qD(g),平衡时测得B的浓度为1.0 mol·L-1。保持温度不变,将容器的体积压缩到原来的一半,再次达到平衡时,测得B的浓度为1.5 mol·L-1。下列有关判断正确的是
A.x+y<p+qB.气体的平均摩尔质量增大
C.压缩体积时,平衡向逆反应方向移动D.体系中混合气体的平均密度不变
科目:高中化学 来源: 题型:
【题目】某温度时,在一个2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
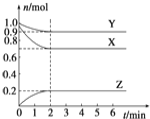
(1)该反应的化学方程式为_____________________ ;
(2)反应开始至2 min,气体Z的平均反应速率为_________;
(3)当反应达平衡时后:若X、Y、Z均为气体,若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应为_____反应(填放热或吸热)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究化合物A(仅含三种短周期元素)的组成和性质,设计并完成如下实验:
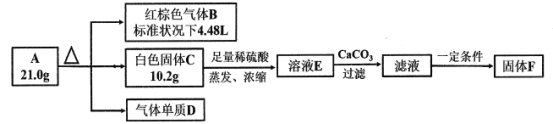
已知:白色固体C既能与强酸反应,也能与强碱反应。
请回答:
(1)写出A受热分解的化学方程式为___________________________________________。
(2)请设计实验方案检验溶液E中所含的阳离子_________________________________。
(3)若固体F中金属元素的百分含量为19.29%,硫为22.86%,氧为57.14%,且300 g/mol<MF<450 g/mol,则F的化学式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,是原电池的装置图。请回答:
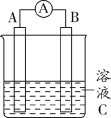
(1)若C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为_____________;反应进行一段时间后溶液C的pH将_____(填“升高”“降低”或“基本不变”)。
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(负极)极材料为____,B(正极)极材料为______,溶液C为_______。
(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如下:
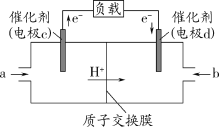
电池总反应为2CH3OH+3O2=2CO2+4H2O,则c电极是____(填“正极”或“负极”),c电极的反应方程式为______________。若线路中转移2mol电子,则上述CH3OH燃料电池,消耗的O2在标准状况下的体积为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子反应方程式书写正确的是
A.往稀盐酸中逐滴加入Na2CO3溶液,开始时:H++CO![]() =HCO
=HCO![]()
B.草酸(H2C2O4,弱酸)溶液中加入酸性KMnO4溶液: 2MnO![]() +5C2O
+5C2O![]() +16H+=2Mn2++10CO2↑+8H2O
+16H+=2Mn2++10CO2↑+8H2O
C.往少量澄清石灰水中加入Ca(HCO3)2溶液: Ca2++OH-+HCO![]() =CaCO3↓+H2O
=CaCO3↓+H2O
D.用HI溶液溶解Fe2O3固体:Fe2O3+6H+=2Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】饱和BaCO3溶液中存在平衡:BaCO3(s)![]() Ba2+(aq)+CO32-(aq)。当碳酸钡固体在水中达到溶解平衡后,为使溶液中Ba2+的物质的量浓度增大,下列操作不可行的是
Ba2+(aq)+CO32-(aq)。当碳酸钡固体在水中达到溶解平衡后,为使溶液中Ba2+的物质的量浓度增大,下列操作不可行的是
A.加入少量0.1 mol·L-1盐酸B.加入少量硝酸钡固体
C.加入少量0.1 mol·L-1硫酸D.加入少量氢氧化钡固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素的单质和常见的化合物在工、农业生产中用途广泛。
(1)工业上利用分离空气的方法得到氮气.空气各主要成分的沸点如下:
N2 | O2 | Ar | CO2 |
-196℃ | -183℃ | -186℃ | -78℃ |
现将空气深度冷却液化,然后缓慢升温,则最先分离出来的气体是______.
(2)雷雨时空气中的N2转化为NO,生成物NO是______色的气体,______(填“易”或“难”)溶于水;NO在空气中很容易被氧化成NO2,NO2能与水发生化学反应,写出NO2与水反应的化学方程式为__________________.
(3)实验室可用固体NH4Cl与固体Ca(OH)2加热反应制取氨气;
①制取氨气的化学方程式为__________________;
②要制取标准状况下4.48L的氨气,至少需要称取固体NH4Cl的质量为______g;
(4)已知:4NH3+6NO![]() 5N2+6H2O化学研究性学习小组的同学在技术人员的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能;
5N2+6H2O化学研究性学习小组的同学在技术人员的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能; ![]()
若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同);
①NH3与稀硫酸溶液反应的离子方程式为__________________;
②为了比较不同催化剂的催化性能,需要测量并记录的数据是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】针对如图所示乙醇分子结构,下述关于乙醇在各种化学反应中化学键断裂情况的说法不正确的( )
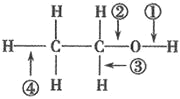
A.与金属钠反应时,①键断裂
B.与浓硫酸共热至170℃时,②、④键断裂
C.在 Ag 催化下与O2反应时,①、③键断裂
D.与醋酸、浓硫酸共热时,②键断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年 IUPAC将第117号元素命名为Ts(中文名![]() ,音tian),TS是第七周期第ⅦA族元素。下列说法中,不正确的是
,音tian),TS是第七周期第ⅦA族元素。下列说法中,不正确的是
A.Ts的最外层电子数是7
B.Ts原子原子半径比At原子大
C.Ts在同族元素中非金属性最弱
D.中子数为176的Ts,其核素符号是![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com