


科目:高中化学 来源:不详 题型:单选题
| A.0.02mol | B.0.08mol | C.0.10mol | D.0.16mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.5 mol/L | B. l mol/L | C.2 mol/L | D.3mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.3/8 mol | B.3/2 mol | C.2 mol | D.0.5 mol |
查看答案和解析>>
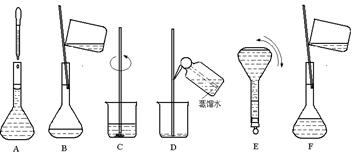
科目:高中化学 来源:不详 题型:实验题
| A.使用容量瓶前检查它是否漏水 |
| B.容量瓶用蒸馏水洗净后,再用待配液润洗 |
| C.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀 |
| D.将准确量取的18.4 mol·L-1的硫酸,注入已盛有30 mL水的100 mL的容量瓶中,加水至刻度线 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验步骤 | 有关问题 |
| ①计算所需Na2SO4的质量 | 需要称量Na2SO4的质量为 克 |
| ②称量Na2SO4固体 | |
| ③将Na2SO4加入100mL烧杯中,并加入适量水溶解 | |
| ④将烧杯中溶液转移至500mL容量瓶中 | 为了防止溶液溅出,应采取什么措施: |
| ⑤向容量瓶中加蒸馏水至刻度线 | 在进行此操作时当加水至刻度线1—2厘米处应如何操作: |
| ⑥摇匀 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.含NA个分子的二氧化硫 | B.0.5mol氧气 |
| C.标准状况下5.6L氢气 | D.9g水(水的摩尔质量为18g·mol-1) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.标准状况下,0.56 L丙烷中含有共价键的数目为0.2NA |
| B.常温常压下,6.4 g氧气和臭氧中含有的分子总数为0.2NA |
| C.一定条件下,5.6 g铁与浓硫酸恰好反应,转移的电子数目一定为0.2NA |
| D.常温下,20 L pH=12的Na2CO3溶液中含有的OH-离子数为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com