
有关物质间转化关系如下图,试回答:
(1)转化①的反应条件为 .
(2)转化②的化学方程式为 .转化③的离子方程式为 .
(3)若转化⑤用于实验室制Al(OH)3,则试剂A宜选择 (填名称).
(4)向50 mL 3 mol·L-1 AlCl3溶液中滴加1 mol·L-1 NaOH溶液,结果Al3+离子有1/3转化为Al(OH) 3沉淀,则加入的NaOH溶液的体积可能为 或 mL。
(1)电解
(2)2Al+2NaOH+2H2O=2NaAlO2+3H2↑,MnO2+4H++2Cl- Cl2↑+Mn2++2H2O
Cl2↑+Mn2++2H2O
(3)氨水
(4)150ml、550ml
解析试题解析:(1)由氧化铝制取铝单质,通过电解的方法。
(2)转化②是指铝和氢氧化钠溶液的反应,所以方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,转化③是指二氧化锰与浓盐酸反应制取氯气,所以离子方程式为MnO2+4H++2Cl- Cl2↑+Mn2++2H2O。
Cl2↑+Mn2++2H2O。
(3)因为氢氧化铝易溶解于强碱溶液,所以制备氢氧化铝时常用弱碱溶液氨水。
(4)由题意可知氯化铝的物质的量为0.15mol, Al3+离子有1/3转化为Al(OH) 3时,有两种情况:一、NaOH不足,这时有0.05mol的Al(OH) 3生成则需要NaOH0.15mol,体积为150ml;二、NaOH过量时,生成0.15mol的Al(OH) 3需要0.45mol的NaOH,再溶解0.1mol的Al(OH) 3需要0.1mol的NaOH,所以共需要0.55mol的NaOH,体积为550ml。
考点:考查铝单质的制取、铝的化合物的化学性质、实验室制氯气的方法及简单计算


科目:高中化学 来源: 题型:填空题
目前世界上60%的镁是从海水中提取的。海水提镁的主要流程如下: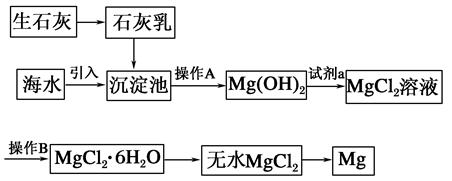
请回答下列问题:
(1)从离子反应的角度思考,在海水中加入石灰乳的作用是________,写出在沉淀池中发生反应的离子方程式:_________________________________________________。
(2)石灰乳是生石灰与水形成的化合物,从充分利用海洋化学资源,提高经济效益的角度考虑,生产生石灰的主要原料来源于海洋中的________。
(3)操作A是________,操作B是________。
(4)加入的足量试剂a是________(填化学式)。
(5)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为________,从考虑成本和废物循环利用的角度,副产物氯气可以用于________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某地有丰富的铝土矿和石灰石资源,拟用铝土矿(主要成分是Al2O3,还有少量的Fe2O3、SiO2)为原料冶炼铝,工艺流程如下图所示: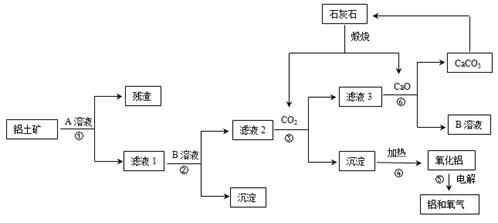
(1)原料A的名称是 ,可循环使用的物质的化学式式为 。
(2)如果省去步骤①,即溶解铝土矿从直接加入B溶液开始,则最终会对氧化铝的生产产生的影响是 。
(3)写步骤③的离子方程式 。
(4)步骤⑤是在铝电解槽中进行,电解槽的两极材料均用石墨,写出阴极的电极反应方程式 。
(5)工业常用阳极氧化法使铝的表面生成致密的氧化膜。如右图是铝阳极氧化实验装置图:a端是电源的 极。铝片表面形成氧化铝的原理是(用电极方程式表示) , (填“能”或“不能”)用较浓NaCl溶液代替20%H2SO4作电解液进行铝的阳极氧化,若不能,请说明理由 。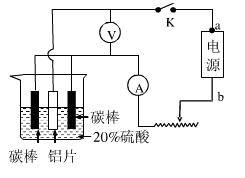
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
由铝土矿(主要成分是Al2O3)炼制铝的工艺流程示意图如下: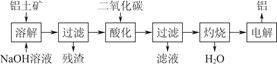
(1)电解生成的铝在熔融液的 (填“上层”或“下层”),电解时不断消耗的电极是 (填“阴极”或“阳极”)。
(2)写出通入过量二氧化碳酸化时反应的离子方程式
。
(3)电解制备铝时,需加入冰晶石(Na3AlF6),其作用是 ,工业上可以用氟化氢气体、氢氧化铝和纯碱在高温条件下发生反应来制取冰晶石,写出该反应的化学方程式 。
(4)上述工艺所得铝中往往含有少量Fe和Si等杂质,可用电解方法进一步提纯,该电解池的阴极材料是 (填化学式),阳极的电极反应式为 。
(5)对金属制品进行抗腐蚀处理,可延长其使用寿命。
①控制一定条件进行电解(见图),此时铝表面可形成耐酸的致密氧化膜,其电极反应式为 ;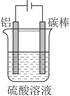
②钢材镀铝后,能防止钢材腐蚀,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A~G各物质间的关系如图,其中B、D为气态单质。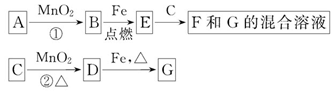
请回答下列问题。
(1)物质C和E的名称分别为_______、_______;
(2)可选用不同的A进行反应①,若能在常温下进行,其化学方程式为_________;若只能在加热情况下进行,则反应物A应为______________;
(3)MnO2在反应①和反应②中的作用分别是_______、_______;
(4)新配制的F溶液应加入_______以防止其转化为G。检验G溶液中阳离子的常用试剂是_______,实验现象为________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某同学实验探究氨气的还原性并进行系列实验。
(1)将光亮的紫红色铜丝绕几圈后,在酒精灯火焰上加热,等铜丝变黑后,趁热将铜丝插入疏松的氯化铵晶体里,即刻发现有白色烟雾生成,拿出铜丝后,铜丝又转变为光亮的紫红色。在焊接铜器时用氯化铵除去铜器表面的氧化铜即利用了该原理,请完成该反应:
(2)利用下列装置,进行与金属氧化物MxOy反应生成M、H2、H2O,通过测量生成水的质量来测定M的相对原子质量。a中试剂是浓氨水。
①仪器a的名称为__________,仪器b中装人的试剂可以是____________.
②按气流方向正确的装置连接顺序为(填序号,装置可重复使用):___________。
③实验结束时,应首先__________(填序号)。
I.熄灭A装置的酒精灯
II.停止从a中滴加液体
④若实验中准确称取金属氧化物的质量为mg,完全反应后,测得生成水的质量为ng,则M的相对原子质量为__________(用含X、y、m、n的式子表示)。
(3)若金属氧化物MxOy为Fe2O3,将反应后固体溶于稀硫酸,然后滴加KSCN溶液没发生明显变化。推测该固体成分可能是(将化学式填人下表,你认为有几种可能填几种)。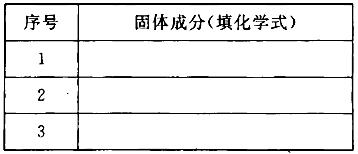
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组的同学欲测定该补血剂中铁元素的含量。实验步骤如下: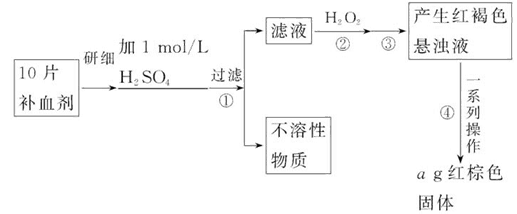
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是:取样,先滴加KSCN溶液,再滴加_______,该过程的现象为:__________________________________________。
(2)步骤②加入过量H2O2的目的是:____________________________________。
(3)步骤③中反应的离子方程式是:_____________________________________。
(4)步骤④中一系列处理的操作步骤:过滤、_______、灼烧、_______、称量。
(5)若实验中铁无损耗,则每片补血剂中含铁元素的质量为_______g。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知A~K均为中学化学中的常见物质,它们之间的转化关系如图所示,其中A、D为金属单质,反应过程中生成的水及其他部分产物已略去。
请回答以下问题:
(1)A与B反应的化学方程式是:______________________________________。
(2)向F中通入足量CO2生成K的离子方程式为:_________________________。
(3)A与NaOH溶液反应的离子方程式是:_________________________________________________。
(4)①检验物质J的溶液中金属离子的方法是:_______________________________________________。
②将物质E溶于水,其溶液呈酸性,原因是(用离子方程式表示)____________。
③某高效净水剂是由D(OH)SO4聚合得到的。工业上以DSO4、稀硫酸和亚硝酸钠为原料来制备D(OH)SO4,反应中有NO生成,该反应的化学方程式是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
铁单质及其化合物在生活、生产中应用广泛。请回答:
(1)钢铁在空气中发生吸氧腐蚀时,正极的电极反应是 。
(2)由于氧化性Fe3+>Cu2+氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式是 。
(3)硫酸铁可作絮凝剂,常用于净水,其原理是 (用离子方程式表示)。在使用时发现硫酸铁不能将酸性废水中的悬浮物沉降除去,其原因是 。
(4)磁铁矿是工业上冶炼铁的原料之一,其原理是Fe3O4十4CO 3Fe+4CO2,若有1.5 mol Fe3O4参加反应,转移电子的物质的量是 。
3Fe+4CO2,若有1.5 mol Fe3O4参加反应,转移电子的物质的量是 。
(5)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是 (填字母)。
| | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铁是地壳中含量最高的金属元素 | 铁是人类最早使用的金属材料 | Ⅰ对;Ⅱ对;有 |
| B | 常温下铁与稀硫酸反应生成氢气 | 一定温度下氢气能还原氧化铁得到铁 | Ⅰ对;Ⅱ对;无 |
| C | 铁属于过渡元素 | 铁和铁的某些化合物可用作催化剂 | Ⅰ错;Ⅱ对;无 |
| D | 在空气中铁表面形成致密氧化膜 | 铁不能与氧气反应 | Ⅰ对;Ⅱ对;有 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com