
| c4(NO)?c6(H2O) |
| c4(NH3)?c5(O2) |
| c4(NO)?c6(H2O) |
| c4(NH3)?c5(O2) |
| c4(NO)?c6(H2O) |
| c4(NH3)?c5(O2) |
| c4(NO)?c6(H2O) |
| c4(NH3)?c5(O2) |


 ��������������������ϵ�д�
��������������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| ||
| ||
| C4(NO)?C6(H2O) |
| C4(NH3)?C5(O2) |
| C4(NO)?C6(H2O) |
| C4(NH3)?C5(O2) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| c2(NH3) |
| c3(H2)c(N2) |
| c2(NH3) |
| c3(H2)c(N2) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
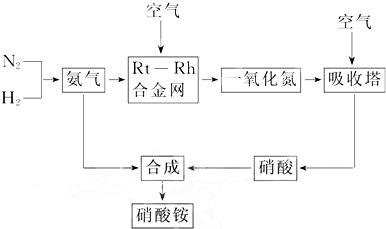
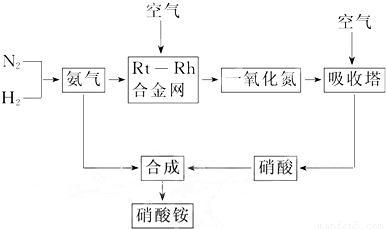
������ڹ�ũҵ����������ռ�м�Ϊ��Ҫ��λ�ã����������ͼ������淋Ĺ�ҵ�������չ��̣�
��1����֪N2��g��+3H2��g��?2NH3��g����H=-92.4 kJ/mol����ش�
����500�桢1.01��105 kPa��������������һ�ܱ������г���1 mol N2��3 mol H2����ַ�Ӧ�ų�������С��92.4 kJ�����ɣ�
��Ϊ��Ч���������ת���ʣ�ʵ���������˲�ȡ�Ĵ�ʩ��______��
A������ѹǿ B�����ʺϴ������Ե��ʵ����� C������ѹǿ D����ʱ�Ƴ���E��ѭ�����úͲ��ϲ��䵪��
��2�����������Ļ�ѧ����ʽΪ4NH3��g��+5O2��g��?4NO��g��+6H2O��g����H��0��
�÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽK=______�����¶�����ʱ��Kֵ______���������С������Ӱ�족����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013�꼪��ʡ�ӱ��ݰ�ͼ�س���ɽһ�и߿���ѧ���ָ�ϰ�Ծ���һ���������棩 ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com