
下列说法正确的是
A.常温下,反应2A (s)+B (g)=2C (g)+D (g)不能自发进行,则该反应△H一定大于0
B.铅蓄电池在放电过程中,负极质量增加,正极质量减少
C.其他条件不变,向纯水中加入盐酸或氢氧化钠都能抑制水的电离,降低水的离子积
D.常温下,向饱和碳酸钠溶液中加入过量碳酸钡粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,则常温下Ksp(BaCO3)<Ksp(BaSO4)
A
【解析】
试题分析:A、根据△G=△H-T·△S可知,反应的自发性与焓变、熵变均有关系。常温下,反应2A (s)+B (g)=2C (g)+D (g)是熵值增加的反应,若不能自发进行,则该反应△H一定大于0,A正确;B、铅蓄电池在放电过程中,负极和正极均有硫酸铅生成,电极均是质量增加的,B不正确;C、水的离子积常数只与温度有关系,因此其他条件不变,向纯水中加入盐酸或氢氧化钠都能抑制水的电离,但水的离子积不变,C不正确;D、碳酸钡是过量的,所以沉淀中一定含有碳酸钡,与盐酸反应放出CO2气体,不能证明碳酸钡的溶度积常数小于硫酸钡的溶度积常数,D不正确,答案选A。
考点:考查反应自发性、铅蓄电池、水的电离平衡以及溶度积常数的有关判断与应用等


科目:高中化学 来源: 题型:阅读理解

| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol CH3OCH3、1mol H2O | 2mol CH3OH | 1mol CH3OH |
| CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 吸收a kJ | 放出b kJ | 放出c kJ |
| 平衡时体积(L) | V1 | V2 | V3 |
| 反应物转化率 | α 1 | α 2 | α 3 |

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 非金属元素氮有多种氧化物,如NO、NO2、N2O4等.
非金属元素氮有多种氧化物,如NO、NO2、N2O4等.| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
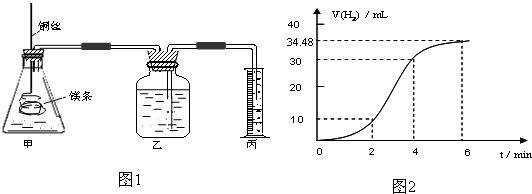
| 实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 10%H2O2的体积/mL | 5.0 | 5.0 | V1 | V2 |
| 20%硫酸的体积/mL | 0 | 0.5 | 1.0 | V3 |
| 水的体积/mL | 15 | 14.5 | V4 | 13.5 |
| 所需时间t/s | t1 | t2 | t3 | t4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com