
【题目】可以证明可逆反应N2+3H2![]() 2NH3已达到平衡状态的是( )
2NH3已达到平衡状态的是( )
①一个N≡N键断裂的同时,有3个H—H键断裂;
②一个N≡N键断裂的同时,有2个N—H键断裂;
③N2、H2、NH3浓度比为1:3:2
④保持其它条件不变时,体系压强不再改变;
⑤NH3、N2、H2的体积分数都不再改变
⑥恒温恒容时,混合气体的密度保持不变;
⑦正反应速率v(H2)=0.6mol/(L·min),逆反应速率v(NH3)=0.4mol/(L·min)
A.②⑤⑥ B.①④⑤ C.④⑤⑦ D.③⑥⑦
【答案】C
【解析】
试题分析:①一个N≡N键断裂的同时,3个H—H键断裂均表示正反应速率,不能说明达到平衡状态,错误;②一个N≡N键断裂,2个N—H键断裂,均表示正反应速率,不能说明达到平衡状态,错误;③N2、H2、NH3浓度比为1:3:2,不能表示浓度是否变化,能说明达到平衡状态,错误;④该反应属于气体体积变化的反应,当体系压强不再改变,说明达到了平衡状态,正确;⑤NH3、N2、H2的体积分数都不再改变,表示浓度均不再改变,说明达到了平衡状态,正确;⑥容器的体积不变,气体的质量不变,混合气体的密度始终保持不变,不能说明达到平衡状态,错误;⑦正反应速率v(H2)=0.6mol/(L·min),逆反应速率v(NH3)=0.4mol/(L·min) ,表示正逆反应速率相等,说明达到了平衡状态,正确;故选C。


 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
【题目】课外学习小组为检验溶液中是否含有常见的四种无机离子,进行了如图所示的实验操作。其中操作过程中产生的气体能使红色石蕊试纸变蓝,由该实验能得到的正确结论是( )
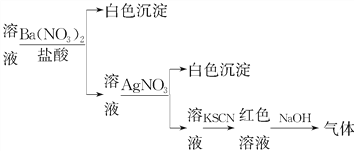
A. 溶液中一定含有SO![]()
B. 溶液中一定含有NH![]()
C. 溶液中一定含有Cl-
D. 溶液中一定含有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验验证元素周期律。
(Ⅰ)甲同学在a、b、c三只烧杯里分别加入50 mL水,再分别滴加几滴酚酞溶液,依次加入大小相近的锂、钠、钾块,观察现象。
甲同学设计实验的目的是 , 烧杯 (填字母)中的反应最剧烈。
(Ⅱ)乙同学设计实验验证非金属元素的非金属性越强,对应的最高价含氧酸的酸性就越强。他设计了下图装置以验证氮、碳、硅元素的非金属性强弱。

乙同学设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,常温下可与铜反应;B是块状固体;打开分液漏斗的活塞后,C中可观察到有白色沉淀生成。
(1)写出所选用物质的化学式:A: ;B: ; C: 。
(2)写出烧杯中发生反应的离子方程式:
(3)该装置存在着某个缺陷,改进的方法是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于取代反应的是( )
A. 淀粉在一定条件下水解生成葡萄糖
B. 苯与浓硝酸、浓硫酸混合共热制取硝基苯
C. 在催化剂存在条件下,乙烯与水反应制乙醇
D. 油脂在碱性条件下水解制肥皂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中没有颜色变化的是( )
A. 葡萄糖溶液与新制的Cu(OH)2悬浊液混合加热
B. 木板上涂抹浓硫酸
C. 淀粉溶液中加入碘酒
D. 苯加入到酸性高锰酸钾溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器,发生反应:C(s)+2H2O(g) ![]() CO2(g)+2H2(g),其相关数据如下表所示:
CO2(g)+2H2(g),其相关数据如下表所示:
容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | |
C(s) | H2O(g) | H2(g) | ||||
甲 | 2 | T1 | 2 | 4 | 3.2 | 2.8 |
乙 | 1 | T2 | 1 | 2 | 1.2 | 3.0 |
(1)T1 _________T2 (填“>”、“<”或“=”)
(2)达到平衡后,保持温度和体积不变,向甲容器内再充入0.8molH2O和3.2molH2,则此时V正________V逆(填“>”、“<”或“=”)
(3)在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是_______________.
A.V逆(CO2)=2V正(H2)
B混合气体的密度保持不变
C.c(H2O):c(CO2):c(H2)=2:1:2
D.混合气体的平均相对分子质量保持不变
(4)某同学为了研究反应条件对化学平衡的影响,测得逆反应速率与时间的关系如图所示:

可见在t1、t3、t5、t7时反应都达了到平衡状态,如果t2、t4、t6、t8时都只改变了一个反应条件,则t6时刻改变的条件是_______________,则从t1到t8哪个时间段H2O (g)的平衡转化率最低_________,(填“t1~t2,以此类推”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是(设阿伏加德罗常数的数值为NA)( )
A. 在标准状况下,22.4L水所含分子数目为NA
B. 1mol·L-1K2SO4溶液所含K+数目为2NA
C. 1 mol钠与氧气反应生成Na2O或Na2O2时,失电子数目均为NA
D. O2的摩尔体积约为22.4 L·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右下表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素的核电荷数为X元素的2倍。下列说法正确的是( )
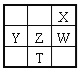
A. X、W、Z元素的原子半径及它们的气态氢化物的热稳定性均依次递增
B. Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增
C. 根据元素周期律,可以推测T元素的单质具有半导体特性,T2X3具有氧化性和还原性
D. YX2晶体熔化、液态WX3气化均需克服分子间作用力
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com