
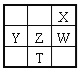
����Ŀ�����±�ΪԪ�����ڱ���һ���֣�����X��Y��Z��WΪ������Ԫ�أ�WԪ�صĺ˵����ΪXԪ�ص�2��������˵����ȷ���ǣ� ��
A. X��W��ZԪ�ص�ԭ�Ӱ뾶�����ǵ���̬�⻯������ȶ��Ծ����ε���
B. Y��Z��WԪ������Ȼ���о�����������̬���ڣ����ǵ�����������ˮ������������ε���
C. ����Ԫ�������ɣ������Ʋ�TԪ�صĵ��ʾ��а뵼�����ԣ�T2X3���������Ժͻ�ԭ��
D. YX2�����ۻ���Һ̬WX3��������˷����Ӽ�������
���𰸡�C
�����������������X��Y��Z��WΪ������Ԫ�أ���Ԫ�����ڱ���֪��XӦλ�ڵڶ����ڣ���Ӧ�������ڱ����Ұ벿�֣�W��X����ͬһ���壬��WԪ��ԭ�ӵĺ˵����ΪXԪ�ص�2������ôXΪO��WΪS����ôZΪP��TΪAs��YΪSi��A��Ԫ�صķǽ�����Խǿ������̬�⻯��Խ�ȶ������ڷǽ�����O��S��P����H2O��H2S��H3P��A����B��SԪ������Ȼ���д�������̬���ʣ����ڻ�ɽ�ڸ�����B����C��As����Ԫ�����ڱ��Ľ�����ǽ����ֽ����ϣ����а뵼������ܣ�T2X3ΪAs2O3��As�Ļ��ϼ�Ϊ+3�������м�ۣ��ʼ���������Ҳ�л�ԭ�ԣ�C��ȷ��D��YX2ΪSiO2������ԭ�Ӿ��壬�ù����ۻ��˷����ǹ��ۼ���û�з��Ӽ���������D����ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������֤�����淴ӦN2+3H2![]() 2NH3�Ѵﵽƽ��״̬������ ��
2NH3�Ѵﵽƽ��״̬������ ��
��һ��N��N�����ѵ�ͬʱ����3��H��H�����ѣ�
��һ��N��N�����ѵ�ͬʱ����2��N��H�����ѣ�
��N2��H2��NH3Ũ�ȱ�Ϊ1��3��2
������������������ʱ����ϵѹǿ���ٸı䣻
��NH3��N2��H2��������������ٸı�
�����º���ʱ�����������ܶȱ��ֲ�����
������Ӧ����v��H2��=0.6mol/��L��min�����淴Ӧ����v��NH3��=0.4mol/��L��min��
A���ڢݢ� B���٢ܢ� C���ܢݢ� D���ۢޢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʯӢ����̿Ϊԭ�ϵIJ��ֻ���������ͼ��ʾ��

�ش��������⣺
(1)��ӦI�ڹ�ҵ�ϵ������������ֹ裬Ϊ������ƷR���Ƿ������������ʣ�ȡ����R����ϡ�����ܽ⣬ȡ�ϲ���Һ�����ټ�����Լ���______������ĸ����
a����ˮ b����ˮ c��KSCN��Һ d��NaCl��Һ
(2)��Ӧ��Ҫ�ڸ��ﻷ���±��У���ԭ����______���������õ���SiHCl3���е�Ϊ33.0�棩�к�������SiCl4�е�Ϊ57.6�棩��HC1���е�Ϊ- 84.7�棩�����ᴿSiHCl3�ķ���Ϊ______________��
(3)��ˮ����ͨ�����ȵ�ú�ۿɲ���ˮú��������Ҫ�ɷ���CO��H2����ҵ�Ͻ�ˮú��Һ�����Ƶõ�CH3OH�к��еĻ�ѧ������Ϊ________������Ӽ������ۼ�����������ͼ�еķ�Ӧ��Ϊ������ԭ��Ӧ���仯ѧ����ʽΪ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��COCl2��g��![]() CO��g����Cl2��g�� ��H>0������Ӧ�ﵽƽ��ʱ�����д�ʩ�������� ������ͨ��������� ������CO��Ũ�� ����ѹ ���Ӵ��� ����ѹͨ��������� ������ͨ��COCl2���壬�����COCl2ת���ʵ����� ��
CO��g����Cl2��g�� ��H>0������Ӧ�ﵽƽ��ʱ�����д�ʩ�������� ������ͨ��������� ������CO��Ũ�� ����ѹ ���Ӵ��� ����ѹͨ��������� ������ͨ��COCl2���壬�����COCl2ת���ʵ����� ��
A���٢ܢޢ� B���٢ܢ� C���٢ڢܢ� D���ۢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A�Ļ�ѧʽΪNH5����������ԭ�ӵ�����㶼������Ӧϡ�������������Ӳ�ṹ���������й�˵������ȷ���ǣ� ��
A. 1 mol NH5�к���5 NA��N��H����NA��ʾ�����ӵ�������
B. NH5�м��й��ۼ��������Ӽ�
C. NH5�ĵ���ʽΪ![]()
D. ����ˮ��Ӧ�����ӷ���ʽΪNH4++H��+H2O=NH3H2O+H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ú��ܷ��ϣ���Ҫ�ɷ�ΪCo������һ������Ni��Al203��Fe��SiO2�ȣ��Ʊ������ܾ��壨CoC2O4��2H2O���Ĺ�ҵ������ͼ����֪���ٲ����ܾ���������ˮ��RHΪ�л���(�ѵ��룩

��1������I����Ҫ�ɷ���______���ѧʽ����д��һ�������������ʵĴ�ʩ_______��
��2�������� �õ�����Ҫ������________________��
��3��H2O2��һ����ɫ��������д������H2O2������Ӧ�����ӷ���ʽ__________��
��4�����������ܵ�Ŀ����__________��
��5�������ܾ���ֽ����Եõ������ܵ����������Co�Ļ��ϼ�Ϊ��2����3����ȡһ�����ܵ��������280mL 5mol/L����ǡ����ȫ�ܽ⣬���õ�CoCl2��Һ��2.24L����״��������ɫ���壬�ɴ˿�ȷ��������������Co��O�����ʵ���֮��Ϊ_________��
��6��ʵ���ҿ���������KMnO4��Һ�ζ���������ӣ�C2O42-�����ⶨ��Һ��C2O42-��Ũ�ȣ�д���˷�Ӧ�����ӷ���ʽ_________��KMnO4 ����Һ���������ữ�����������ữ����ʹ�ⶨ���________���ƫ�ߡ�����ƫ�͡�����Ӱ�족����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н�����ұ�������У�����뻹ԭ������(����)
A. HgO�D��Hg B. Al2O3�D��Al
C. Ag2O�D��Ag D. CuSO4�D��Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���У��������
A. ����ˮ������Եõ���ˮ
B. ��ȡʵ������Ҫ��Һ����
C. �����ù��˵ķ�������NaCl��Һ��ֲ����
D. ��ȥ����ع����е������Ȼ��ƿ��Խ�������Ƴ��ȱ�����Һ����ȴ�ᾧ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ú�������Ƕ�ú������ӹ�����Ҫ����������Ҫ��Ӧ��̼��ˮ������Ӧ����ˮú����
��1����֪��101KPa��150��ʱ����1mol��̼��һ����̼���������������������ȼ�ղ��ָ���ԭ�¶ȣ����ų��������ֱ�Ϊ393.7kJ/mol��283.0kJ/mol��242.0 kJ/mol����д��ú��������Ӧ���Ȼ�ѧ����ʽ__________________���������ѧ�Ƕȼ����÷�Ӧ��ij�������ܹ�������е�ԭ����_______________��
��2���ں����ܱ�����������ʵ�����1:1����һ������̼��ˮ������Ӧ����ˮú����һ�������´ﵽƽ�⣬���ı䷴Ӧ��ijһ����ʱ�����б仯��˵��ƽ��һ��������Ӧ�����ƶ�����_________��������ţ�
A.����Ӧ�������������� B.��ѧƽ�ⳣ��K����
C.��������ƽ����Է����������� D.��Ӧ�����������������
��3��һ��������ú���������ﻹ���Է�����Ӧ��700��ʱ�����ݻ�Ϊ2L���ܱ������г���һ������CO��H2O��������Ӧ��CO(g)+H2O(g)![]() CO2(g)+ H2(g) ��Ӧ�����вⶨ�IJ������ݼ��±���
CO2(g)+ H2(g) ��Ӧ�����вⶨ�IJ������ݼ��±���
��Ӧʱ��/ min | n(CO)/ mol | n(H2O)/ mol |
0 | 1.20 | 0.60 |
5 | 0.80 | |
10 | 0.20 |
����ݱ���ش��������⣺
�ټ��㷴Ӧ��5min����������ʾ��ƽ������Ϊ��_____________��
����ʽ������÷�Ӧ��700��ʱ�Ļ�ѧƽ�ⳣ��K=__________������¶�����800�棬������Ӧƽ�ⳣ��Ϊ0.64��������ӦΪ___________������ȡ����ȡ�����Ӧ��
�۽��ϱ��д�ƽ���Ļ������ָ������£���200mL2mol/LNaOH��Һ�������գ���ַ�Ӧ�������Һ������䣬����˵������ȷ���ǣ�����֪HCO3-���볣��ԼΪ4![]() 10-11��CaCO3���ܶȻ�����ԼΪ3
10-11��CaCO3���ܶȻ�����ԼΪ3![]() 10-9��___________
10-9��___________
A.c��Na+��+c��H+��=c��OH-��+c��HCO3-��+2c��CO32-��
B.c��H2CO3����c��CO32-��
C.c��Na+��+c��OH-��=c��H+��+c��HCO3-��+2c��H2CO3��
D.�����Һ�м���������Ũ�ȵ�CaCl2��Һ������ɫ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com