
| A、50mL 0.5 mol?L-1的NaCl溶液 |
| B、0.5 L含0.2 mol?L-1的MgCl2溶液 |
| C、10mL0.4 mol?L-1的AlCl3溶液 |
| D、100mL1.0 mol?L-1的KCl溶液 |


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
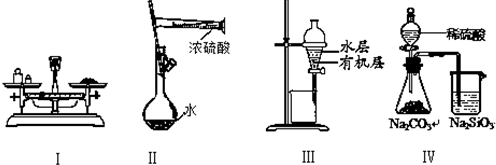
| A、实验Ⅰ:用托盘天平称量一定质量的氯化钠固体 |
| B、实验Ⅱ:配制一定物质的量浓度的硫酸 |
| C、实验Ⅲ:用苯萃取溴水中的溴后进行分液 |
| D、实验Ⅳ:比较硫酸、碳酸和硅酸酸性强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应物总能量小于成物总能量 |
| B、断键和成键过程中都释放能量 |
| C、断键过程中吸收能量,成键过程中释放能量 |
| D、断键过程中释放能量,成键过程中吸收能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、-319.68kJ?mol-1 |
| B、-417.91kJ?mol-1 |
| C、+546.69kJ?mol-1 |
| D、-448.46kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25mL | B、5mL |
| C、10mL | D、50mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4+、K+、OH-、NO3- |
| B、Fe2+、H+、Cl-、NO3- |
| C、K+、Al3+、F-、CO32- |
| D、NH4+、Na+、Cu2+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是用未知浓度的NaOH溶液来滴定10mL盐酸(标准液)所得的曲线(25℃),则下列说法不正确的是( )
如图是用未知浓度的NaOH溶液来滴定10mL盐酸(标准液)所得的曲线(25℃),则下列说法不正确的是( )| A、标准液盐酸的浓度为0.1 mol/L |
| B、NaOH溶液的浓度为0.05 mol/L |
| C、滴定终点时,俯视碱式滴定管读数,所测NaOH溶液浓度会偏高 |
| D、指示剂变色时,说明盐酸与NaOH恰好完全反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com