
【题目】已知反应A2(g)+2B2(g)![]() 2AB2(g)△H <0,下列说法正确的( )
2AB2(g)△H <0,下列说法正确的( )
A. 升高温度有利于反应速率增加,从而缩短达到平衡的时间
B. 升高温度,正向反应速率增加,逆向反应速率减小
C. 达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
D. 达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
科目:高中化学 来源: 题型:
【题目】新型锂-空气电池具有能量密度高的优点,有望成为新能源汽车的电源,其结构如右图所示,其中固体电解质只允许Li+通过。下列说法正确的是

A. 放电时,负极反应式:Li-e-+OH-=LiOH
B. 放电时,当外电路中有1 mol e-转移时,水性电解液离子总数增加NA
C. Li+穿过固体电解质向正极移动而得到LiOH溶液
D. 应用该电池电镀铜,阴极质量增加64 g,理论上将消耗11.2 L O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰化钠是一种重要的基本化工原料,同时也是一种剧毒物质,严重危害人类健康。一旦泄露需要及时处理,一般可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻环境污染。
I.已知:氰化钠化学式为NaCN,氰化钠是一种白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,
易水解生成氰化氢。
(1)CN-中C元素显+2价,N元素显-3价,则非金属性N_______C(填“<”“>”或“==”),请设计实验证明:___________________________________________________________________________。
(2)NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,该反应的离子方程式是________________________________________________________。
I.硫代硫酸钠的工业制备的反应原理为2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2。某化学兴趣小组用上述原理实验室制备硫代硫酸钠,并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放。
【查阅资料】
ⅰ.Na2S2O3易溶于水,其稀溶液与BaCl2溶液混合物有沉淀生成。
ⅱ.Na2S2O3易被氧化;BaSO3难溶于水,可溶于稀盐酸。
【实验一】实验室通过如下图所示装置制备Na2S2O3。
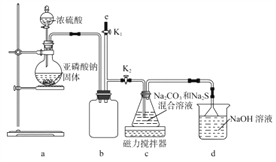
(1)实验中要控制SO2生成速率,可采取的措施有____________(写出一条)。
(2))b装置的作用是____________________________。
(3)反应开始后,c中先有淡黄色浑浊产生,后又变为澄清,此浑浊物为________(填化学式)。
(4)实验结束后,在e处最好连接盛__________(填“NaOH溶液”、“水”、“CCl4”中的一种)的注射器,接下来的操作为__________,最后拆除装置。
(5)为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。(所需试剂从稀HNO3、稀H2SO4、稀HCl、蒸馏水中选择)取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,_____________________________________。若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
【实验二】测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。
已知:
①废水中氰化钠的最高排放标准为0.50 mg·L-1;
②Ag++2CN-=[Ag(CN)2]-,Ag++I-=AgI↓,AgI呈黄色,且CN-优先于Ag+反应。
实验如下:取20.00mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4mol·L-1的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50mL。
(6)滴定时1.000×10-4mol·L-1的标准AgNO3溶液应用_______(填仪器名称)盛装;滴定终点时的现象是_______。
(7)处理后的废水是否达到排放标准:_______ (填“是”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器里,A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)表示,已知3v(B)=2v(A)、2v(C)=3v(B),则此反应可表示为( )
A.2A+3B=2CB.A+3B=2CC.3A+2B=3CD.A+B=C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应CO(g)+H2O![]() CO2+H2 H<0。在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述错误的是( )
CO2+H2 H<0。在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述错误的是( )
A. 充入一定量的氮气,n(H2)不变 B. 减小压强,c(CO2)减小
C. 升高温度,![]() 减小 D. 更换高效催化剂,α(CO)增大
减小 D. 更换高效催化剂,α(CO)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应A(g)+B![]() C(g)+D,达到平衡时,下列说法不正确的是
C(g)+D,达到平衡时,下列说法不正确的是
A. 若B是气体,增大A的浓度会使B转化率增大
B. 若增大A的浓度,平衡体系颜色加深,D不一定是有颜色的气体
C. 升高温度,C百分含量减少,说明正反应是放热反应
D. 增大压强,平衡不移动,说明B是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 12gC所含的原子数就是阿伏加德罗常数 B. 4.9 g H2SO4是0.05 mol H2SO4
C. 氢原子的摩尔质量是1.008 g D. 1 mol氧的质量是32 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.研究CO2、CO的利用对促进低碳社会的构建具有重要意义,CO2、CO都可用于合成甲醇。CO2用于合成甲醇的热化学方程式为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H
CH3OH(g)+H2O(g) △H
①该反应的平衡常数表达式为K=____________________。
②取一定体积CO2和H2的混合气体(物质的量之比为1∶3),加入恒容密闭容器中发生上述反应,反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如右图所示,则该反应的ΔH_______0(填“>”、“<”或“=”)。

Ⅱ.甲醇是结构最为简单的饱和一元醇,又称“木醇”或“木精”。甲醇是一碳化学基础的原料和优质的燃料,主要应用于精细化工、塑料、能源等领域。
已知甲醇制备的有关化学反应如下
反应①:CO(g)+2H2(g)=CH3OH(g) △H1=﹣90.77kJmol—1
反应②:CO2(g)+H2(g)=CO(g)+H2O(g) △H2=+41.19kJmol—1
反应③:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H3
(1)反应③的△H3=__________________。
(2)若500℃时三个反应的平衡常数依次为K1、K2与K3,则K3=_____(用K1、K2表示)。已知500℃时K1、K2的值分别为2.5、1.0,并测得该温度下反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O (g)的浓度(mol/L)分别为0.8、0.1、0.3、0.15,则此时 V正_____ V逆(填“>”、“=”或“<”).
(3)在3L容积可变的密闭容器中发生反应②,c(CO)随反应时间t变化如图中曲线Ⅰ所示。若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。

当曲线Ⅰ变为曲线Ⅱ时,改变的条件是_______。当通过改变压强使曲线Ⅰ变为曲线Ⅲ时,曲线Ⅲ达到平衡时容器的体积为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(6分)分离沸点不同但又互溶的液体混合物,常用的方法是 ;分离不溶性固体和液体混合物的常用的方法是 ;分离两种溶解度相差很大的溶质的溶液时,常用的方法是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com