
面对目前世界范围内的能源危机,甲醇作为一种较好的可再生能源,具有广泛的应用前景。
(1)已知在常温常压下反应的热化学方程式:
①CO(g)+2H2(g)  CH3OH(g) ΔH1=-90 kJ·mol-1
CH3OH(g) ΔH1=-90 kJ·mol-1
②CO(g)+H2O(g)  CO2(g)+H2(g)ΔH2=-41 kJ·mol-1
CO2(g)+H2(g)ΔH2=-41 kJ·mol-1
写出由二氧化碳、氢气制备甲醇的热化学方程式:_______________________。
(2)在容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡时的转化率与温度、压强的关系如图所示。
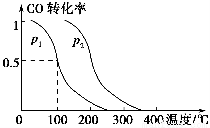
①p1________p2(填“大于”、“小于”或“等于”);
②在其他条件不变的情况下,再增加a mol CO与2a mol H2,达到新平衡时,CO的转化率________(填“增大”、“减小”或“不变”,下同),平衡常数________。
(3)已知在T ℃时,CO(g)+H2O(g)??CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1 mol·L-1,c始(H2O)=1 mol·L-1,某时刻经测定CO的转化率为10%,则该反应________(填“已经”或“没有”)达到平衡,原因是___________________________________________。此时刻v正________v逆(填“>”或“<”)。
(1)CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH=-49 kJ·mol-1 (2)①小于 ②增大 不变 (3)没有 此时
CH3OH(g)+H2O(g) ΔH=-49 kJ·mol-1 (2)①小于 ②增大 不变 (3)没有 此时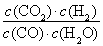 =
=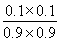 =0.012 3<0.32 >
=0.012 3<0.32 >
【解析】(1)由盖斯定律,热化学方程式①-②得CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH=ΔH1-ΔH2=-90 kJ·mol-1-(-41 kJ·mol-1)=-49 kJ·mol-1。(2)由图像可知,相同温度下,p2下CO的转化率大于p1下CO的转化率,由热化学方程式①可知,增大压强平衡右移,故p1<p2;在其他条件不变的情况下,再增加a mol CO与2a mol H2,相当于增大压强,平衡右移,故CO的转化率增大;由于温度不变,故其平衡常数不变。(3)
CH3OH(g)+H2O(g) ΔH=ΔH1-ΔH2=-90 kJ·mol-1-(-41 kJ·mol-1)=-49 kJ·mol-1。(2)由图像可知,相同温度下,p2下CO的转化率大于p1下CO的转化率,由热化学方程式①可知,增大压强平衡右移,故p1<p2;在其他条件不变的情况下,再增加a mol CO与2a mol H2,相当于增大压强,平衡右移,故CO的转化率增大;由于温度不变,故其平衡常数不变。(3)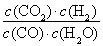 =
=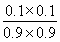 =0.012 3<K=0.32,故反应未达到平衡。此时反应向正反应方向进行,故v正>v逆。
=0.012 3<K=0.32,故反应未达到平衡。此时反应向正反应方向进行,故v正>v逆。


科目:高中化学 来源:2014年高二人教化学选修五2-1-2脂肪烃炔烃脂肪烃来源及应用练习卷(解析版) 题型:选择题
某气态烃1 mol能和2 mol HCl加成,其饱和产物又能和6 mol Cl2完全取代,则该烃是( )
A.C2H6 B.C2H2 C.C3H4 D.C4H6
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上专题1物质组成分类性质及化学用语练习卷(解析版) 题型:选择题
下列叙述正确的是( )。
A.盐酸和食醋既是化合物又是酸
B.纯碱、CuSO4·5H2O和生石灰分别属于盐、混合物和氧化物
C.胶体处于介稳定状态,所以放置一会便会有沉淀生成
D.胶体区别于其他分散系的本质特征是分散质粒子直径的大小
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题7电解质溶液练习卷(解析版) 题型:填空题
请回答有关滴定过程中的相关问题。
(1)用已知浓度的氢氧化钠溶液滴定未知浓度的盐酸,滴定曲线如图所示。
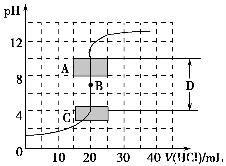
①在图中A的pH范围使用的指示剂是________;
C的pH范围使用的指示剂是________。
②下列关于上述中和滴定过程中的操作,正确的是________(填序号)。
A.用碱式滴定管量取已知浓度的烧碱溶液
B.滴定管和锥形瓶都必须用待装液润洗
C.滴定过程中始终注视锥形瓶中溶液颜色变化
D.锥形瓶中的待测液可用量筒量取
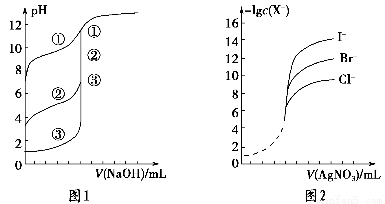
(2)如图1表示用相同浓度的NaOH溶液分别滴定浓度相同的3种一元酸,由图可确定酸性最强的是________。如图2表示用相同浓度的硝酸银标准溶液分别滴定浓度相同的含Cl-、Br-及I-的混合溶液,由图可确定首先沉淀的是 ________。
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题7电解质溶液练习卷(解析版) 题型:选择题
下列关于电解质溶液的叙述正确的是 ( )。
A.常温下,同浓度的Na2CO3与NaHCO3溶液相比,Na2CO3溶液的pH大
B.常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)>c(NH4+)>c(H+)=c(OH-)
C.中和pH与体积均相同的盐酸和醋酸,消耗NaOH溶液的物质的量相同
D.将pH=4的盐酸稀释后,溶液中所有离子的浓度均降低
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题6化学反应速率和化学平衡练习卷(解析版) 题型:选择题
一定条件下,在密闭容器中,能表示反应X(g)+2Y(g) 2Z(g)一定达到化学平衡状态的是 ( )。
2Z(g)一定达到化学平衡状态的是 ( )。
①X、Y、Z的物质的量之比为1∶2∶2 ②X、Y、Z的浓度不再发生变化 ③容器中的压强不再发生变化 ④单位时间内生成n mol Z,同时生成2n mol Y
A.①② B.①④ C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题5化学反应与能量变化练习卷(解析版) 题型:选择题
有关热化学方程式书写与对应表述均正确的是 ( )。
A.稀醋酸与0.1 mol·L-1 NaOH溶液反应:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1
B.密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成硫化亚铁17.6 g时,放出19.12 kJ热量,则Fe(s)+S(s)=FeS(s) ΔH=-95.6 kJ·mol-1
C.氢气的燃烧热为285.5 kJ·mol-1,则水电解的热化学方程式为2H2O(l)=2H2(g)+O2(g) ΔH=+285.5 kJ·mol-1
D.已知2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1,则可知C的燃烧热为110.5 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题4物质结构与元素周期律练习卷(解析版) 题型:选择题
下列说法正确的是 ( )。
A.原子核都是由质子和中子构成的
B.同位素的化学性质基本相同,其物理性质不一定相同
C.第ⅠA族元素铯的两种同位素,137Cs比133Cs多4个质子
D.质子数相同的微粒都属于同种元素
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题13化学实验综合应用练习卷(解析版) 题型:实验题
固体硝酸盐加热易分解且产物较复杂。某学习小组以Mg(NO3)2为研究对象,拟通过实验探究其热分解的产物,提出如下4种猜想:
甲:Mg(NO2)2、NO2、O2
乙:MgO、NO2、O2
丙:Mg3N2、O2
丁:MgO、NO2、N2
(1)实验小组成员经讨论认定猜想丁不成立,理由是______________________________。
查阅资料得知:2NO2+2NaOH=NaNO3+NaNO2+H2O
针对甲、乙、丙猜想,设计如下图所示的实验装置(图中加热、夹持仪器等均省略):
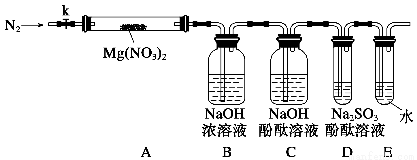
(2)实验过程
①仪器连接后,放入固体试剂之前,关闭k,微热硬质玻璃管(A),观察到E中有气泡连续放出,表明__________。
②称取Mg(NO3)2固体3.7 g置于A中,加热前通入N2以驱尽装置内的空气,其目的是________;关闭k,用酒精灯加热时,正确操作是先________,然后固定在管中固体部位下加热。
③观察到A中有红棕色气体出现,C、D中未见明显变化。
④待样品完全分解,A装置冷却至室温、称量,测得剩余固体的质量为1.0 g。
⑤取少量剩余固体于试管中,加入适量水,未见明显现象。
(3)实验结果分析讨论
①根据实验现象和剩余固体的质量经分析可初步确认猜想______是正确的。
②根据D中无明显现象,一位同学认为不能确认分解产物中有O2,因为若有O2,D中将发生氧化还原反应:______________(填写化学方程式),溶液颜色会褪去;小组讨论认定分解产物中有O2存在,未检测到的原因是_____________________________________。
③小组讨论后达成的共识是上述实验设计仍不完善,需改进装置进一步探究。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com