
固体硝酸盐加热易分解且产物较复杂。某学习小组以Mg(NO3)2为研究对象,拟通过实验探究其热分解的产物,提出如下4种猜想:
甲:Mg(NO2)2、NO2、O2
乙:MgO、NO2、O2
丙:Mg3N2、O2
丁:MgO、NO2、N2
(1)实验小组成员经讨论认定猜想丁不成立,理由是______________________________。
查阅资料得知:2NO2+2NaOH=NaNO3+NaNO2+H2O
针对甲、乙、丙猜想,设计如下图所示的实验装置(图中加热、夹持仪器等均省略):
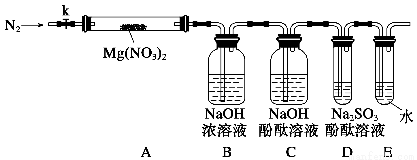
(2)实验过程
①仪器连接后,放入固体试剂之前,关闭k,微热硬质玻璃管(A),观察到E中有气泡连续放出,表明__________。
②称取Mg(NO3)2固体3.7 g置于A中,加热前通入N2以驱尽装置内的空气,其目的是________;关闭k,用酒精灯加热时,正确操作是先________,然后固定在管中固体部位下加热。
③观察到A中有红棕色气体出现,C、D中未见明显变化。
④待样品完全分解,A装置冷却至室温、称量,测得剩余固体的质量为1.0 g。
⑤取少量剩余固体于试管中,加入适量水,未见明显现象。
(3)实验结果分析讨论
①根据实验现象和剩余固体的质量经分析可初步确认猜想______是正确的。
②根据D中无明显现象,一位同学认为不能确认分解产物中有O2,因为若有O2,D中将发生氧化还原反应:______________(填写化学方程式),溶液颜色会褪去;小组讨论认定分解产物中有O2存在,未检测到的原因是_____________________________________。
③小组讨论后达成的共识是上述实验设计仍不完善,需改进装置进一步探究。
(1)不符合氧化还原反应原理(或其他合理答案)
(2)①装置气密性良好 ②避免对产物O2的检验产生干扰(或其他合理答案) 移动酒精灯预热硬质玻璃管
(3)①乙 ②2Na2SO3+O2=2Na2SO4 O2在通过装置B时已参与反应(或其他合理答案)
【解析】(1)丁中产物中只有N的化合价降低,没有化合价升高的,不符合电子得失守恒规律。(2)在做有关气体多步连续实验时,首先应检查装置的气密性,还要考虑装置中的空气对产物的生成及检验是否会产生影响,若有干扰必须先排净干扰气体。对玻璃加热时要先均匀预热,再集中加热。(3)①不可能是甲,因为甲中Mg(NO2)2可溶于水。不可能是丙,因为丙中Mg3N2能与水反应产生NH3和Mg(OH)2沉淀。
只能是乙,Mg(NO3)2 ~ MgO
148 40
3.7 g m
m=40×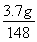 =1.0 g
=1.0 g
氧化镁难溶于水,且符合质量变化。
②Na2SO3具有还原性,能被O2氧化;NO2和O2可被NaOH共同吸收。


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源:2014年高中化学二轮创新训练上 专题6化学反应速率和化学平衡练习卷(解析版) 题型:填空题
面对目前世界范围内的能源危机,甲醇作为一种较好的可再生能源,具有广泛的应用前景。
(1)已知在常温常压下反应的热化学方程式:
①CO(g)+2H2(g)  CH3OH(g) ΔH1=-90 kJ·mol-1
CH3OH(g) ΔH1=-90 kJ·mol-1
②CO(g)+H2O(g)  CO2(g)+H2(g)ΔH2=-41 kJ·mol-1
CO2(g)+H2(g)ΔH2=-41 kJ·mol-1
写出由二氧化碳、氢气制备甲醇的热化学方程式:_______________________。
(2)在容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡时的转化率与温度、压强的关系如图所示。
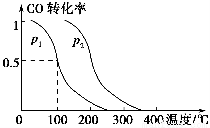
①p1________p2(填“大于”、“小于”或“等于”);
②在其他条件不变的情况下,再增加a mol CO与2a mol H2,达到新平衡时,CO的转化率________(填“增大”、“减小”或“不变”,下同),平衡常数________。
(3)已知在T ℃时,CO(g)+H2O(g)??CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1 mol·L-1,c始(H2O)=1 mol·L-1,某时刻经测定CO的转化率为10%,则该反应________(填“已经”或“没有”)达到平衡,原因是___________________________________________。此时刻v正________v逆(填“>”或“<”)。
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题2常用化学计量-物质的量练习卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )。
A.将NA个HCl分子溶于500 mL水中得到2.0 mol·L-1的盐酸
B.在加热条件下,100 mL 18.4 mol·L-1的浓硫酸与足量金属铜反应得到的SO2的分子数为0.92NA
C.密闭容器中,1 mol SO2与0.5 mol O2充分反应,转移的电子数小于2NA
D.用惰性电极电解AgNO3溶液,产生11.2 L O2时,转移2 mol电子
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题15有机化学基础选考练习卷(解析版) 题型:填空题
聚-3-羟基丁酸酯(PHB)常用于制造可降解塑料等。PHB是由3-羟基丁酸[CH3CH(OH)CH2COOH]分子聚合而成。合成聚-3-羟基丁酸酯的途径很多,其中有一种途径的副产物少、污染小、原子利用率高,其合成路线如下:
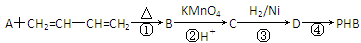
已知: 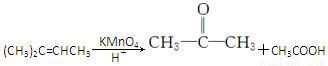
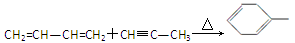
请回答下列问题。
(1)写出C中含有的官能团的名称:____________。
(2)上述转化过程中属于加成反应的是________(填序号)。
(3)反应②符合绿色化学思想(碳原子的有效利用率为100%),则A的结构简式为__________________。
(4)写出反应④的化学方程式:_____________________________________
_______________________________________________________________。
(5)写出与C互为同分异构体,能发生银镜反应,且核磁共振氢谱有两组吸收峰的有机物的结构简式:____________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题14物质结构与性质选考练习卷(解析版) 题型:填空题
钾、镁、氟、硼等元素在每升海水中的含量都大于1毫克,属于海水中的常量元素。
(1)钾、镁、氟、硼电负性从大到小的排列顺序是__________________________。
(2)镓与硼同主族,写出镓元素原子的价电子排布式(即外围电子排布式):________________。
(3)用价层电子对互斥模型推断BF3和NF3的空间构型分别为________、________。
(4)钾、镁、氟形成的某化合物的晶体结构为K+在立方晶胞的中心,Mg2+在晶胞的8个顶角,F-处于晶胞的棱边中心。由钾、镁、氟形成的该化合物的化学式为________,每个K+与________个F-配位。
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题12化学实验基础练习卷(解析版) 题型:选择题
用下列实验装置进行相应实验,能达到实验目的的是( )。
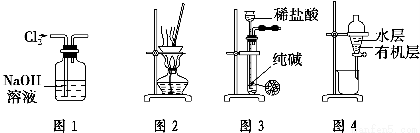
A.用图1所示装置除去Cl2中含有的少量HCl
B.用图2所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C.用图3所示装置制取少量纯净的CO2气体
D.用图4所示装置分离CCl4萃取碘水后已分层的有机层和水层
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题12化学实验基础练习卷(解析版) 题型:选择题
为证明稀硝酸与铜反应产物中气体为NO,设计如图实验(实验过程中活塞2为打开状态),下列说法中不正确的是 ( )。
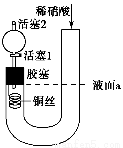
A.关闭活塞1,加入稀硝酸至液面a处
B.在装置左侧稍加热可以加快稀硝酸与铜的反应速率
C.通过关闭或开启活塞1可以控制反应的进行
D.反应开始后,胶塞下方有无色气体生成,还不能证明该气体为NO
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题11常见有机化合物及其应用练习卷(解析版) 题型:选择题
下列化合物的分子中,所有原子都处于同一平面的有( )。
①乙烷 ②甲苯 ③氟苯 ④四氯乙烯
A.①④ B.②③ C.③④ D.①②
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 4-1-2海水资源的开发利用练习卷(解析版) 题型:选择题
从海水中可以提取溴,但得到的液溴中常常溶有少量氯气,除去氯气应该采用的方法是( )
A.加入适量的Na2CO3溶液
B.通入溴蒸气
C.加入适量的NaOH溶液
D.加入适量的NaBr溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com