
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
已知:HCN(aq)与NaOH(aq)反应的ΔH=-12.1kJ·mol-1;
HCl(aq)与NaOH(aq)反应的ΔH=-55.6kJ·mol-1。
则HCN在水溶液中电离的ΔH等于( )
A.+43.5kJ·mol-1 B.-43.5kJ·mol-1 C.+67.7kJ·mol-1 D.-67.7kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是
A.原子核内有10个中子的氧原子:18O B.乙烯的结构简式: CH2CH2

 C.CH4 分子的比例模型: D.-CH3(甲基)的电子式为:
C.CH4 分子的比例模型: D.-CH3(甲基)的电子式为:
查看答案和解析>>
科目:高中化学 来源: 题型:
为了证明(NH4)2Fe(SO4)2·6H2O(硫酸亚铁铵晶体)的成分中含有NH4+、Fe2+、SO42-和H2O,下列实验叙述中不正确的是
A.取少量样品放入试管中,加热,试管口放一团蘸有无水硫酸铜粉末的棉花团,变蓝则可证明晶体的成分中含有结晶水
B.取少量样品溶于水,得淡绿色溶液,滴入2滴KSCN溶液,溶液不显红色,再滴入几滴新制氯水,溶液变为红色,则可证明晶体的成分中含有Fe2+
C.取少量样品溶于水,加少量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO42-
D.取少量样品放入试管中,加入少量稀NaOH溶液,在试管口用湿润的红色石蕊试纸检验,则可证明晶体的成分中是否含有NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学为探究铜跟浓硫酸的反应情况,用下图所示装置进行了有关实验
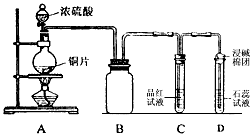
(1)B是用来收集实验中生成的气体的装置,但未将导管画全,请在答题卷上把导管补充
完整 ▲ 。
(2)请写出铜跟浓硫酸反应的化学方程式 ▲ 。
(3)实验中D中的现象 ▲ 。
(4)实验中,该同学取6.4g铜片和12mL 18mol·L-1H2SO4溶液放在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有铜片剩余;该同学根据所学的化学知识判断还会有一定量H2SO4的剩余,下列药品中能够用来验证反应停止后的烧瓶中确有剩余的H2SO4的是 ▲ 填字母编号)。
a.BaCl2溶液 b.Ba(NO3)2溶液 c.银粉 d.Na2CO3粉末
(5)若将16g铜与50mLH2SO4物质的量浓度为一定值的浓硫酸反应,铜完全溶解。请回答:
①反应中产生的气体在标准状况下的体积为 ▲ L。
②该反应中被还原的H2SO4的物质的量为 ▲ mol。
③待产生的气体全部释放后,向溶液中滴加VmL a mol·L-1NaOH溶液,恰好使溶液中
的Cu2+全部转化为沉淀,则原浓硫酸中H2SO4的物质的量浓度= ▲ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
以下有机物既能发生消去反应生成相应的烯烃,又能氧化生成相应的醛的是 ( )
A.CH3OH B.HOCH2CH(CH3)2
C.(CH3)3COH D.CH3CHOHCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.在某盐溶液中加入浓NaOH溶液,加热后如果生成气体使湿润的红色石蕊试纸变蓝,则原溶液一定是铵盐溶液
B.浓硝酸中的HNO3见光会分解,故有时在实验室看到的浓硝酸呈黄色
C.在某溶液中加入盐酸酸化的BaCl2溶液,如果生成白色沉淀,则原溶液中一定
有SO42—
D.除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学模拟工业“折点加氯法”处理氨氮废水的原理,进行如下研究。
| 装置(气密性良好,试剂已添加) | 操作 | 现象 |
|
| 打开分液漏斗活塞,逐滴加入浓氨水 | ⅰ.C中气体颜色变浅 ⅱ.稍后,C中出现白烟并逐渐增多 |
浓氨水分解可以制氨气,写出A中反应的化学方程式是 。
是从平衡移动的角度分析NaOH固体在氨水分解中的作用
。
(2)现象ⅰ,C中发生的反应为:2NH3(g)+3Cl2(g)= N2(g)+6HCl(g) H= —456 kJ·mol-1
已知:
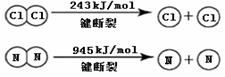
①NH3的电子式是 。
②断开1mol H-N键与断开1molH-Cl键所需能量相差约为 ,
(3)现象ⅱ中产生白烟的化学方程式是 。
(4)为避免生成白烟,该学生设计了下图装置以完成Cl2和NH3的反应。
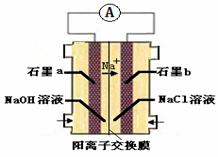
若该装置能实现设计目标,则①石墨b电极上发生的是 反应(填“氧化”或“还原”)
②写出石墨a电极的电极反应式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com