
��12�֣��������洦����Ƥ�����ơ�ӡȾ�ȶ�������ɸ���Ⱦ�����۸������۸����Ըߣ����ױ����������������������
��1����ҵ�ϴ������Ժ�Cr2O72����ˮ�ķ������£�
����Cr2O72�������Է�ˮ�м���FeSO4��Һ��ʹCr2O72��ȫ��ת��ΪCr3+��д���÷�Ӧ�����ӷ���ʽ�� ��
�ڵ�����Һ��pH��ʹCr3����ȫ������ʵ���Ҵ��Բⶨ��ҺpH�ķ���Ϊ
��25�棬��������Һ��pH��8������Һ�в���Cr3+�����ʵ���Ũ��Ϊ mol/L������֪25��ʱ��Ksp[Cr(OH)3]��6.3��10��31��
��2����Ԫ����Ũ�ȵIJⶨ��ȷ��ȡ25.00mL��Cr2O72����Cr3+�����Է�ˮ�������м���������(NH4)2S2O8��Һ��Cr3+������Cr2O72������г�ȥ������(NH4)2S2O8����������Һ�м��������KI��Һ����ַ�Ӧ���Ե���Ϊָʾ���������еμ�0.015mol/L��Na2S2O3����Һ���յ�ʱ����Na2S2O3��Һ20.00mL��
�����ˮ�и�Ԫ����Ũ�ȣ���λ��mg��L��1��д��������̣���
��֪�ⶨ�����з����ķ�Ӧ���£�
��2Cr3+ + 3S2O82�� + 7H2O Cr2O72�� + 6SO42�� + 14H+
Cr2O72�� + 6SO42�� + 14H+
��Cr2O72�� + 6I�� + 14H+ 2Cr3+ + 3I2 + 7H2O
2Cr3+ + 3I2 + 7H2O
��I2 + 2S2O32�� 2I�� + S4O62��
2I�� + S4O62��
��1����Cr2O72����6Fe2����14H����2Cr3����6Fe3����7H2O��2�֣�
�ڽ�pH��ֽ���ڽྻ�ı������ϣ��ò�����պȡ��Һ�� ����pH��ֽ�ϣ��������ɫ�����գ�2�֣�
6.3��10��13��2�֣�
��2���ɷ���ʽ��֪��Cr~3Na2S2O3
n(Na2S2O3)��20.00mL��0.015mol/L��3��10��4mol
n(Cr)��1��10��4mol
m(Cr)��1��10��4mol��52g��mol��1��5.2��10��3 g��5.2mg
��ˮ�и�Ԫ����Ũ�ȣ�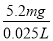 ��208 mg��L��1��6�֣�
��208 mg��L��1��6�֣�
��������
�����������1����Cr2O72�������������°�Fe2+����ΪFe3+����ƽ�ɵ����ӷ���ʽ��Cr2O72����6Fe2����14H����2Cr3����6Fe3����7H2O��
��ʵ������pH��ֽ���Բⶨ��ҺpH���ⶨ����Ϊ����pH��ֽ���ڽྻ�ı������ϣ��ò�����պȡ��Һ�� ����pH��ֽ�ϣ��������ɫ�����գ�����Ksp[Cr(OH)3]��6.3��10��31��c��Cr3+��?c��OH?��3=6.3��10��31��pH��8��c��OH?��=10-6mol?L?1������ɵ�c��Cr3+��=6.3��10��13mol?L?1��
��2������Ŀ������ѧ����ʽ��֪��Ӧ��ϵ��Cr~3Na2S2O3
n(Na2S2O3)��20.00mL��0.015mol/L��3��10��4mol
n(Cr)��1/3 n(Na2S2O3)=1��10��4mol
m(Cr)��1��10��4mol��52g��mol��1��5.2��10��3 g��5.2mg
��ˮ�и�Ԫ����Ũ�ȣ�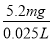 ��208 mg��L��1
��208 mg��L��1
���㣺���⿼�����ӷ���ʽ����д��pH�IJⶨ����ѧ���㡣


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡտ���и�һ��һѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
��10�֣�ij��ѧ����С�齫�Ȼ��ƹ����л��е������ơ�̼��������ʳ�ȥ���õ��Ȼ�����Һ����������·�����

��1�������ٵ�Ŀ���ǣ� ��
��2���������Ƿ�ɸ�Ϊ�����ᱵ��Һ��Ϊʲô�� ��
��3�����в����ں�����ж�SO42���ѳ����������ǣ� ��
��4���ڲ�������Ϊʲô���ڼ�Na2CO3��Һ֮ǰ�ȹ��ˣ������ǣ� ��
��5�������ܵ�Ŀ���ǣ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�γ��С��������и�һ��ѧ������������ѧ�Ծ��������棩 ���ͣ�ѡ����
��״���£�112 mLij�����������0.17g�������������
A��O2 B��N2 C��H2S D��CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�����и�����ѧ�ڵ�һ�ν��Բ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
Mg-H2O2��ؿ������������˼�ʻ��DZ�������õ���Ժ� ˮΪ�������Һ��ʾ��ͼ���¡�
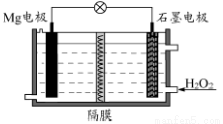
�õ�ع���ʱ������˵������ȷ����
A��Mg�缫�Ǹõ�صĸ���
B��H2O2��ʯī�缫�Ϸ�����ԭ��Ӧ
C��ʯī�缫������Һ��pH����
D����Һ��Cl���������ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�����и�����ѧ�ڵ�һ�ν��Բ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����йػ�ѧ������ȷ����
A��NH4Cl�ĵ���ʽ��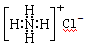
B����18�����ӵ���ԭ�ӵĺ��ط��ţ�1735Cl
C��S2���Ľṹʾ��ͼ��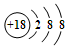
D��������Ľṹʽ:H��O��Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������һ�С�������ѧ�������ϵ��л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʱ�����������Ļ����Һ20mL������������μ���0.05mol��L��1Ba(OH)2��Һʱ�����ɵ�BaSO4��pH�ı仯��ͼ��ʾ����������Һ���ʱ����ı仯��������˵����ȷ����

A��ͼ��A���Ӧ��Һ��pH��a��1
B�����ɳ������������m��2.33g
C��ԭ���Һ���������ʵ���Ũ��Ϊ0.1mol��L��1
D����V[Ba(OH)2(aq)]��10mLʱ��������Ӧ�����ӷ���ʽΪ��Ba2+ + SO42�� BaSO4��
BaSO4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������һ�С�������ѧ�������ϵ��л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����أ�NiMH��Ŀǰ�Ѿ���Ϊ��϶���������һ����Ҫ������͡�NiMH�е�M��ʾ���������Ͻ𡣸õ���ڳ������е��ܷ�Ӧ����ʽ�ǣ�Ni(OH)2 + M NiOOH + MH
NiOOH + MH
��֪��6NiOOH + NH3 + H2O + OH�� 6Ni(OH)2 + NO2����
6Ni(OH)2 + NO2����
����˵����ȷ����
A��NiMH ��طŵ�����У������ĵ缫��ӦʽΪ��NiOOH + H2O + e�� Ni(OH)2 + OH��
Ni(OH)2 + OH��
B����������OH�����Ӵ�����������Ǩ��
C���������������ĵ缫��Ӧʽ��H2O + M + e�� MH + OH����H2O�е�H��M��ԭ
MH + OH����H2O�е�H��M��ԭ
D��NiMH����п�����KOH��Һ����ˮ����Ϊ�������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ̩���н������߶���ѧ���п��Ի�ѧ�Ծ���ѡ�ޣ��������棩 ���ͣ�ѡ����
�������ʵ��ʾ��ͼ���ܴﵽʵ��Ŀ�ĵ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������ѧ�ڵ�һ�ν��Լ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
���и���Ӧ���У������˹�Ԫ�صĻ�ԭ�Ե���
A���ù����켯�ɵ�·������ܵȰ뵼������
B����Ұ�⣬�ù衢ʯ�ҡ��ռ�Ļ������ȡ������Si + Ca (OH)2 + 2NaOH = Na2SiO3 + CaO +2H2��
C����HF���ʴ������SiO2+4HF=SiF4��+2H2O
D�����ʹ���Ʊ��� SiO2 + 2C Si + 2CO��
Si + 2CO��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com