
【题目】医疗上常用硫酸钡作X射线透视肠胃的内服药剂,俗称“钡餐”,碳酸钡却不能作“钡餐”,这是因为
A. 硫酸钡不溶于水,碳酸钡溶于水
B. 硫酸钡是强酸盐,碳酸钡是弱酸盐
C. 硫酸钡不溶于水但溶于酸,碳酸钡不溶于水也不溶于酸
D. 硫酸钡不溶于水也不溶于酸,碳酸钡不溶于水但能溶于酸
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】将纯水加热至较高温度,下列叙述正确的是( )
A.水的离子积变大、pH变小、呈酸性B.水的离子积不变、pH不变、呈中性
C.水的离子积变小、pH变大、呈碱性D.水的离子积变大、pH变小、呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 水玻璃可用作建筑黏合剂 B. 硫酸亚铁可用于生产防治缺铁性贫血的药剂
C. 碳酸钠可用于治疗胃酸过多 D. 碘化银可用于人工降雨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下转化关系中,元素X、Y是短周期同主族元素,元素Z是过渡元素。

已知:①Z2X、Z2Y不溶于水
②浓硝酸具有强氧化性,反应中常被还原成二氧化氮气体
下列说法不正确的是
A. Z2X是Cu2S、Z2Y是Cu2O
B. 步骤①发生的反应,其离子方程式可能为Cu2S+12H++10NO3ˉ = 2Cu2++10NO2↑+SO42ˉ+6H2O
C. 步骤②发生的反应,其离子方程式为H++OHˉ=H2O、Cu2++2OHˉ=Cu(OH)2↓
D. 步骤③发生的反应,说明葡萄糖具有氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正丁醚(CH3CH2CH2CH2OCH2CH2CH2CH3)是一种化工原料,常温下为无色液体,不溶于水,沸点为142.4℃,密度比水小。某实验小组利用如下装置合成正丁醚(其它装置均略去),发生的主要反应为:
![]()
实验过程如下:在容积为l00mL的三颈烧瓶中将5mL浓硫酸、14.8g正丁醇和几粒沸石混合均匀,再加热回流一段时间,收集到粗产品,精制得到正丁醚。回答下列问题:
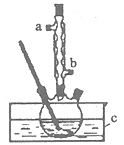
(1)合成粗产品时,液体试剂加入顺序是_________________。
(2)实验中冷凝水应从____口流出(填“a”或‘‘b”)。
(3)为保证反应温度恒定在135°C,装置C中所盛液体必须具有的物理性质为________。
(4)加热时间过长或温度过高,反应混合液会变黑,写出用浓NaOH溶液吸收有毒尾气的离子方程式________________。
(5)得到的正丁醚粗产品依次用8 mL50%的硫酸、10 mL水萃取洗涤。该步骤中需要的属于硅酸盐材质的实验仪器是烧杯、玻璃棒、________________________。
(6)本实验最终得到6.50g正丁醚,则正丁醚的产率是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完全沉淀相同体积的NaCl、MgCl2、AlCl3溶液中的Cl-,消耗相同浓度的AgNO3溶液的体积之比为3:2:1,则NaCl、MgCl2、AlCl3溶液的物质的量浓度之比为( )
A. 1:2:3 B. 3:2:1 C. 6:3:2 D. 9:3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气体的摩尔质量为M g/mol,NA表示阿伏加德罗常数,在一定的温度和压强下,体积为V L的该气体所含有的分子数为X。则 ![]() 表示的是( )
表示的是( )
A. V L该气体的质量(以g为单位) B. 1 L该气体的质量(以g为单位)
C. 1 mol该气体的体积(以L为单位) D. 1 L该气体的物质的量(以mol为单位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【广州市2017届4月综合测试(二)】硼及其化合物应用广泛。回答下列问题:
(1)基态B原子的价电子轨道表达式为________,其第一电离能比Be ________(填“大”或“小”)。
(2)氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是________,写出一种与氨硼烷互为等电子体的分子________(填化学式)。

(3)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如图a。
① B原子的杂化方式为________。从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大:________。
② 路易斯酸碱理论认为,任何可接受电子对的分子或离子叫路易斯酸,任何可给出电子对的分子或离子叫路易斯碱。从结构角度分析硼酸是路易斯酸:________。
(4)立方氮化硼(BN)是特殊的耐磨和切削材料,其晶胞结构与金刚石相似,如图b所示。
① 与氮原子直接连接的硼原子构成的几何形状为________。硼原子和氮原子所连接的最小环为________元环。
② 晶胞有两个基本要素:
原子坐标参数,表示晶胞内部各原子的相对位置。如图b所示,其中原子坐标参数X为(0,0,0),Y原子的坐标参数为(1/2,0,1/2),则Z原子的坐标参数为________。
晶胞参数,描述晶胞的大小和形状。已知立方氮化硼的密度为d gcm-3,阿伏加德罗常数值为NA,则晶胞参数a=________nm。(列出计算式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【厦门第一中学2017届考前模拟】氯化铵俗称卤砂,主要用于干电池、化肥等。某化学研究小组设计如下实验制备卤砂并进行元素测定。
I.实验室制备卤砂:所需装置如下,装置可重复选用。

(1)装置接口连接顺序是_________→a;b←_________。
(2)C装置的作用是___________,D装置盛装的物质是_________________。
(3)写出用上述装置制备氨气的一组试剂:_________________。
Ⅱ.测定卤砂中C1元素和N元素的质量之比。
该研究小组准确称取ag卤砂,与足量氧化铜混合加热,充分反应后把气体产物按下图装置进行实验。收集装置收集到的气体为空气中含量最多的气体,其体积换算成标准状况下的体积为VL,碱石灰增重bg。

(4)E装置内的试剂为________________。
卤砂与氧化铜混合加热反应的化学方程式为________________。
(5)卤砂中Cl元素和N元素的质量之比为_________(用含b、v的式子表示)。
(6)为了测定卤砂中氯元素的质量,他们设计的实验方案是将a g卤砂完全溶解于水,加入过量AgNO3溶液,然后测定生成沉淀的质量。请你评价该方案是否合理,并说明理由:_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com