
 和碳酸氢钠的物质的量分别是x、y
和碳酸氢钠的物质的量分别是x、y

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源:不详 题型:单选题
| A.p(H2)>p(O2)>p(N2) | B.p(O2)>P(N2)>p(H2) |
| C.p(H2)>P(N2)>p(O2) | D.P(N2)>p(O2)>p(H2) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1mol羟基与17gNH3所含电子数都为NA |
| B.12.4g白磷(分子式为P4)中含有P—P共价键0.6 NA |
| C.电解精炼铜的过程中,每转移NA个电子时,阳极溶解铜的质量为32g |
| D.适量铜粉溶解于1L0.5mol·L-1稀硝酸中,当生成2.24LNO时,溶液中氮原子数为0.4 NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.n(H2SO4)=0.1mol | B.n(H2SO4)=0.2mol |
| C.0.1mol<n(H2SO4) <0.2mol | D.0.1mol≤n(H2SO4)≤0.2mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
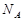 表示阿伏加德罗常数,下列说法正确的是
表示阿伏加德罗常数,下列说法正确的是A.23 g钠与足量氧气充分反应,转移的电子个数为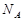 |
B.1mol Cl2与水充分反应,转移的电子个数为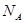 |
| C.1mol Na2O2与水完全反应时转移电子数为2NA |
| D.18 g H2O含有的电子数为18NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SO2的摩尔质量是64g |
| B.18g H2O在标准状况下的体积是22.4L |
| C.在标准状况下,20mL NH3与60mL O2所含的分子数比为1:3。 |
| D.将40g NaOH溶于1L水中,所得溶液的物质的量浓度为1mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解精炼铜时,当阴极析出32g铜时,转移电子数小于NA |
| B.常温下,1.0L 1.0 mol/LNaAlO2溶液中含有的氧原子数为2NA |
| C.等物质的量的干冰和葡萄糖中所含碳原子数之比为1∶6,氧原子数之比为1∶3 |
| D.0.10 mol Fe粉与足量水蒸气反应生成的H2分子数为0.10NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.22.4L H2中含有氢分子的个数为NA |
| B.24g Mg变为Mg2+时失去的电子数为2NA |
| C.32g O2中含有氧原子的个数为2NA |
| D.1L 1mol/L NaCl溶液中含有钠离子的个数为NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.等于0.92 | B.小于0.92 | C.大于0.92 | D.等于1.84 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com