
【题目】在一定温度下,将一定量的气体通入体积为2L的密闭容器中,使其发生反应,,有关物质X、Y、Z的物质的量的变化如图所示。则下列有关推断正确的是( )

A. 该反应的化学方程式为: 3Z = 3X+2Y
B. t0时,X、Y、Z的质量不再改变
C. t0时,Z的浓度为1.2 mol/L
D. t0时,反应停止,反应速率为0
【答案】B
【解析】
A.根据X、Y、Z物质的量的变化判断反应物、产物,利用物质的量之比等于化学计量数之比确定化学计量数,据此书写化学方程式;
B.化学平衡时的特征作判断;
C.根据物质的量与体积计算浓度;
D.根据可逆反应的特征判断。
A.由图可知,X、Y的物质的量增大,X、Y为生成物,Z物质的量减小,Z为反应物,到平衡后,X生成1.8mol,Y生成1.2mol,Z反应1.8mol,X、Y、Z的化学计量数之比=1.8:1.2:1.8=3:2:3,此后任何物质的物质的量不变,则反应为可逆反应,因此该反应的化学方程式为:3Z![]() 3X+2Y,A错误;
3X+2Y,A错误;
B.化学平衡时各组分的浓度不再随时间变化而变化, X、Y、Z的质量也不再改变,B正确;
C.根据图象可知平衡时Z的浓度c(Z)=![]() =0.6mol/L,C错误;
=0.6mol/L,C错误;
D.根据可逆反应平衡的特征可知,反应处于平衡时正、逆反应速率相等,但不等于零,D错误;
故合理选项是B。


科目:高中化学 来源: 题型:
【题目】下列表示式错误的是( )
A. Na+的轨道表示式:![]() B. Na+的结构示意图:
B. Na+的结构示意图:![]()
C. Na的电子排布式:1s22s22p63s1 D. Na的外围电子排布式:3s1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如下能量关系示意图分析,下列说法正确的是( )
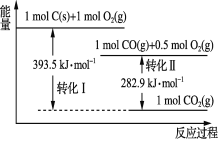
A.1 mol C(g)与1 mol O2(g)的能量之和为393.5 kJ
B.反应2CO(g)+O2(g)=2CO2(g)中,反应物的总键能小于生成物的总键能
C.C→CO的热化学方程式为2C(s)+O2(g)=2CO(g) ΔH=-110.6 kJ·mol-1
D.热值是指一定条件下单位质量的物质完全燃烧所放出的热量,则CO的热值为282.9 kJ·g-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列分析正确的是
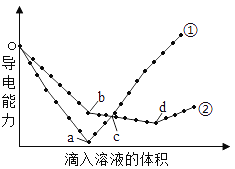
A.b→d反应的离子方程式为:H++OH-=H2O
B.o→a反应的离子方程式为:Ba2++OH-+H++SO42-=BaSO4↓+H2O
C.c点导电能力相同,所以两溶液中含有相同量的OH–
D.a、b两点Ba2+均沉淀完全,所以对应的溶液均显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在10L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化下表中数据
t/min | X/mol | Y/mol | Z/mol |
0 | 1.00 | 2.00 | 0.00 |
1 | 0.90 | 1.80 | 0.20 |
3 | 0.75 | 1.50 | 0.50 |
5 | 0.65 | 1.30 | 0.70 |
9 | 0.55 | 1.10 | 0.90 |
10 | 0.55 | 1.10 | 0.90 |
14 | 0.55 | 1.10 | 0.90 |
(1)体系中发生反应的化学方程式____________;
(2)列式计算该反应在0~3 min时间内产物Z的平均反应速率:________;
(3)该反应达到平衡时反应物X的转化率α等于________;
(4)如果该反应是放热反应,改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线1、2、3(如下图所示)则曲线1、2、3所对应的实验条件改变分别是:1____________,2______________,3______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒鼓回收料含硒约![]() ,其余为约
,其余为约![]() 的碲和微量的氯.从该回收料中回收硒的工艺流程如图所示
的碲和微量的氯.从该回收料中回收硒的工艺流程如图所示![]() 已知煅烧过程中,回收料中的硒、碲被氧化成
已知煅烧过程中,回收料中的硒、碲被氧化成![]() 和
和![]() :
:
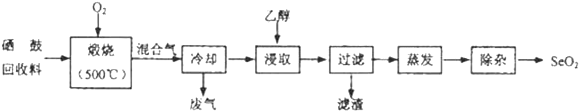
部分物质的物理性质如表:
物质 | 熔点 | 沸点 | 溶解度 |
|
|
| 易溶于水和乙醇 |
|
|
| 微溶于水,不溶于乙醇 |
回答下列问题:
(1)![]() 与S是同族元素,比S多1个电子层,Se在元素周期表的位置为______;
与S是同族元素,比S多1个电子层,Se在元素周期表的位置为______;![]() 的热稳定性比
的热稳定性比![]() 的热稳定性______
的热稳定性______![]() 填“强”或“弱”
填“强”或“弱”![]() .
.
(2)乙醇浸取后过滤所得滤渣的主要成分是______![]() 蒸发除去溶剂后,所得固体中仍含有少量
蒸发除去溶剂后,所得固体中仍含有少量![]() 杂质,除杂时适宜采用的方法是______.
杂质,除杂时适宜采用的方法是______.
(3)![]() 易溶于水得到
易溶于水得到![]() 溶液,向溶液中通入HI气体后,再加入淀粉溶液,溶液变蓝色,同时生成Se沉淀,写出反应的化学方程式______.
溶液,向溶液中通入HI气体后,再加入淀粉溶液,溶液变蓝色,同时生成Se沉淀,写出反应的化学方程式______.
(4)已知![]() 的电离常数
的电离常数![]() 、
、![]() ,回答下列问题:
,回答下列问题:
![]() 溶液呈______性,原因是
溶液呈______性,原因是![]() 用离子方程式表示
用离子方程式表示![]() ______;
______;
![]() 在
在![]() 溶液中,下列关系式正确的是______:
溶液中,下列关系式正确的是______:
A.![]()
B.![]()
C.![]()
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.在醋酸溶液的![]() ,将此溶液稀释1倍后,溶液的
,将此溶液稀释1倍后,溶液的![]() ,则
,则![]()
B.在滴有酚酞溶液的氨水里,加入![]() 至溶液恰好无色,则此时溶液的
至溶液恰好无色,则此时溶液的![]()
C.![]() 盐酸的
盐酸的![]() ,
,![]() 盐酸的
盐酸的![]()
D.若1mL![]() 的盐酸与100mL
的盐酸与100mL![]() 溶液混合后,溶液的
溶液混合后,溶液的![]() 则
则![]() 溶液的
溶液的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其理由是_______________(用必要的化学用语和相关文字说明)。
(2)相同条件下,0.1 mol/L NH4Al(SO4)2中的c(NH![]() )________(填“等于”“大于”或“小于”)0.1 mol/L NH4HSO4中的c(NH
)________(填“等于”“大于”或“小于”)0.1 mol/L NH4HSO4中的c(NH![]() )。
)。
(3)如图是0.1 mol/L电解质溶液的pH随温度变化的图像。

①其中符合0.1 mol/L NH4Al(SO4)2的pH随温度变化的曲线是________(填写字母),导致pH随温度变化的原因是___________________;
②20℃时,0.1 mol/L NH4Al(SO4)2中2c(SO![]() )-c(NH
)-c(NH![]() )-3c(Al3+)=________。
)-3c(Al3+)=________。
(4)室温时,向100 mL 0.1 mol/L NH4HSO4溶液中滴加0.1 mol/L NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
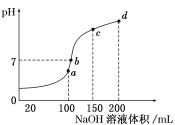
试分析图中a、b、c、d四个点,水的电离程度最大的是________;在b点,溶液中各离子浓度由大到小的排列顺序是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项表达正确的是( )
A.用电子式表示CaCl2的形成过程:![]()
B.硫酸与氢氧化钡溶液反应的离子方程式:Ba2++SO42-=BaSO4↓
C.金属钠在空气中受热燃烧:4Na+O2=2Na2O
D.铁丝与稀硫酸反应的离子方程式:2Fe+6H+=2Fe3++3H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com