
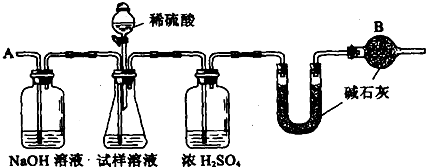
已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。

上所述主要步骤如下:
①按图组装仪器,并检查装置的气密性
②将ag试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰的U型管的质量,得到bg
④从分液漏斗滴入6mol·L-1的硫酸,直到不再产生气体时为止
⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U型管的质量,得到cg
⑦重复步骤⑤和⑥的操作,直到U型管的质量基本不变,为dg
请填空和回答问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明 。
(2)装置中干燥管B的作用是 。
(3)如果将分液漏斗中的疏酸接成浓度相同的盐酸,测试的结果 (填偏高、偏低可不变)。
(4)步骤⑤的目的是 。
(5)步骤⑦的目的是 。
(6)该试样中纯碱的质量分数的计算式为 。
(7)还可以用其他实验方法测定试样中纯碱的质量分数。请简述一种不同的实验方法。
(1)样品重,砝码轻。(2)防止空气中的CO2和水气进入U型管中。(3)偏高
(4)把反应产生的CO2全部导入U型管中
(5)判断反应产生的CO2是否全部排出,并被U型管中的碱石灰吸收
(6) [106(d-b)/44a]×100% (7)Na2CO3能与BaCl2反应而NaCl不会,因此选用BaCl2作试剂、通过测定两者反应产生的碳酸钡的质量来确定碳酸钠的质量。
本实验目的是测定试样中纯碱的质量分数。实验时,采用测定碳酸钠与硫酸反应产生二氧化碳的质量来求算。根据实验目的和原理,实验过程应该准确测定样品的质量和二氧化碳的质量。样品的质量可以直接称量,但二氧化碳的质量则需通过间接称量。实验过程中,通过操作③和⑤来测定,其依据是碱石灰充分吸收二氧化碳,干燥管吸收二氧化碳前后的质量差即为二氧化碳的质量。由于该实验属于定量实验,应重复称重操作,以减小甚至避免误差。因此实验安排了操作⑦。
实验过程中,在称量时,天平的指针向左转,说明左盘重,根据“物左码右”的放置原则,因此样品重,砝码轻;由于空气中存在水蒸汽和二氧化碳,而该实验又是通过盛碱石灰的干燥管来吸收反应产生的二氧化碳,因此要避免空气的CO2和水气的干扰而要安装B干燥管;实验采用硫酸与碳酸钠反应产生二氧化碳,如果改为盐酸,反应虽然可以发生,但由于盐酸会挥发,HCl进入干燥管被吸收,将导致干燥管增重,因此实验结果将偏高;由于装置体系中各容器有较大的空间,会滞留部分二氧化碳,给测量带来影响,因此要在A处缓缓鼓入一定量的空气,将滞留在各容器中的CO2排出,全部导入U型管中;安排操作⑦的目的在于判断反应产生的CO2是否全部排出,并被U型管中的碱石灰吸收;由步骤③和⑤可知,产生二氧化碳的质量为(d-b)g,根据化学方程式可知,碳酸钠的质量分数为106(d-b)/44a×100%。
问题(7)要求重新设计实验方案。作为定量实验方案的设计,解答的关键在于根据实验目的和实验原理确定实验过程中的“可测量”(即能够通过实验可以测定的量——常见的可测量为物质的质量或体积)。题目已经给出了实验目的,由于碳酸钠和氯化钠存在很多方面的性质差异,解答时就可以根据它们性质的差异来确定实验原理和测量方法。例如,Na2CO3能与BaCl2反应而NaCl不会,因此选用BaCl2作试剂、通过测定两者反应产生的碳酸钡的质量来确定碳酸钠的质量。


科目:高中化学 来源: 题型:

| 106(d-b) |
| 44a |
| 106(d-b) |
| 44a |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
- 3 |
- 3 |
| ||
| 106(d-b) |
| 44a |
| 106(d-b) |
| 44a |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 106(d-b) |
| 44 |
| 106(d-b) |
| 44 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 106(d-b) |
| 44a |
| 106(d-b) |
| 44a |
查看答案和解析>>
科目:高中化学 来源:2014届黑龙江大庆铁人中学高一上学期期末考试化学试卷 题型:实验题
(10分).已知某纯碱试样中含有杂质氯化钠,为测定试样中纯碱的质量分数,可用下图装置进行实验。

主要步骤如下,请填空:
① 按图组装仪器,并检查装置的气密性② 将a g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液;③ 称量盛有碱石灰的U形管的质量为b g;④ 从分液漏斗中滴入6mol/L的稀硫酸,直到不再产生气体为止,⑤ 从导管A处缓缓鼓入一定量的空气;⑥ 再次称量盛有碱石灰的U形管的质量为c g;⑦ 重复⑤和⑥的操作,直到U形管的质量基本不变,测得质量为d g。
回答下列问题:(碱石灰是一种干燥剂,不能干燥酸性气体)
(1)装置中干燥管B的作用是
(2)如果将分液漏斗中的硫酸换成同浓度的盐酸,测试的结果将 (填偏高.偏低或不变)
(3)步骤⑤的目的是
(4)步骤⑦的目的是
(5)该试样中纯碱的质量分数的计算式为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com