
将X逐滴加入到Y溶液中,生成沉淀的物质的量n与所加的X的物质的量m的关系如下图A~F所示,那么请将能正确表示反应过程的图像填在下表中。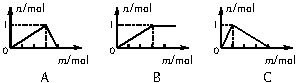

见分析
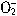 +H++H2O=Al(OH)3↓(沉淀量由0增至最大)。
+H++H2O=Al(OH)3↓(沉淀量由0增至最大)。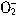 +4H+=Al3++2H2O,反应过程中Al
+4H+=Al3++2H2O,反应过程中Al 转化成最大沉淀时消耗的盐酸的量与沉淀全部溶解时消耗的盐酸的量之比为1∶3,其过程如右图所示。所以图像中的C选项符合表中第(5)组的变化过程。
转化成最大沉淀时消耗的盐酸的量与沉淀全部溶解时消耗的盐酸的量之比为1∶3,其过程如右图所示。所以图像中的C选项符合表中第(5)组的变化过程。 (沉淀量由0增至最大)。
(沉淀量由0增至最大)。

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
| 元素代号 | 相关信息 |
| X | X的原子最外层电子数是其内层电子数的三倍 |
| Y | 在第三周期的所有金属离子中,Y的离子半径最小 |
| Z | Z与Y同周期,是所在周期中原子半径最小的元素 |
| T | T的单质能与冷水剧烈反应,生成的强碱电离出两种电子数相等的阴、阳离子 |


查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | T | X | Y | Z | W |
| 原子半径(nm) | 0.037 | 0.075 | 0.099 | 0.102 | 0.143 |
| 最高或最低化合价 | +1 | +5 -3 |
+7 -1 |
+6 -2 |
+3 |



 NH3?H2O
NH3?H2O NH4++OH-,NaOH溶于水电离出OH-,使平衡向左移动,且溶解时放出热量,使NH3的溶解度减小
NH4++OH-,NaOH溶于水电离出OH-,使平衡向左移动,且溶解时放出热量,使NH3的溶解度减小 NH3?H2O
NH3?H2O NH4++OH-,NaOH溶于水电离出OH-,使平衡向左移动,且溶解时放出热量,使NH3的溶解度减小
NH4++OH-,NaOH溶于水电离出OH-,使平衡向左移动,且溶解时放出热量,使NH3的溶解度减小查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 元素代号 | 相关信息 |
| T | T的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 |
| X | X的原子最外层电子数是其内层电子数的三倍 |
| Y | 在第三周期元素中,Y的简单离子半径最小 |
| Z | T、X、Z组成的36电子的化合物A是家用消毒剂的主要成分 |
查看答案和解析>>
科目:高中化学 来源:河北省石家庄市重点中学2012-2013学年高一下学期期末考试化学试题 题型:022
下表为部分短周期主族元素的相关信息.

请回答下列问题:
(1)Z元素在元素周期表中的位置是第________周期第________族.
(2)元素T与X按原子个数比1∶1形成的化合物B所含的化学键有________(填化学键类型).已知在通常状况下,39 g B与足量H2O反应放出Q kJ的热量,写出该反应的热化学方程式:________.
(3)将T的最高价氧化物对应水化物的溶液,逐滴加入到Y与Z形成的化合物的水溶液中,直至过量(边滴加边振荡),此过程中的现象是________.
(4)已知1 mol化合物A与足量Na2SO3在溶液中发生反应时,转移2 mol电子,写出该反应的离子方程式:________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com