
【题目】下列反应对应的离子方程式书写正确的是( )
A.Na2O2溶于水产生O2:Na2O2+H2O=2Na++2OH-+O2↑
B.向次氯酸钙溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
C.电解饱和食盐水获取烧碱和氯气:2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
D.将1molCl2通入含1molFeI2的溶液中:2Fe2++2I-+2Cl2=2Fe3++4Cl-+I2
科目:高中化学 来源: 题型:
【题目】科学家用氮化镓(GaN)材料与铜作电极组装如图所示的人工光合系统,成功地实现了以CO2和H2O合成CH4。下列说法不正确的是( )
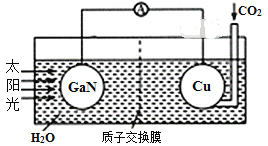
A.电子由GaN沿着导线流向Cu
B.电解液中H+从质子交换膜右侧向左侧迁移
C.GaN表面发生氧化反应,有O2产生
D.Cu表面电极反应式:CO2+8e-+8H+=CH4+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将29.6g碳酸钠和碳酸氢钠的混合物加热到质量不再减少为止,冷却,称得固体质量为26.5g。问:
(1)原固体混合物中碳酸氢钠的质量是多少? ____________
(2)原固体混合物中碳酸钠的物质的量是多少?_____________
(3)把原固体混合物与足量盐酸完全反应生成的CO2在标准状况下的体积是多少?__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.2mol·L-1Na2CO3溶液250mL和0.5mol·L-1盐酸溶液450mL。根据这两种溶液的配制情况回答下列问题:
(1)如图是某同学用Na2CO3·10H2O配制0.2mol·L-1Na2CO3溶液250mL的过程,其中错误的步骤有___。(填实验操作序号)
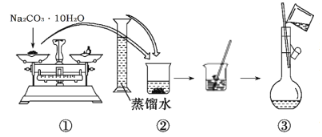
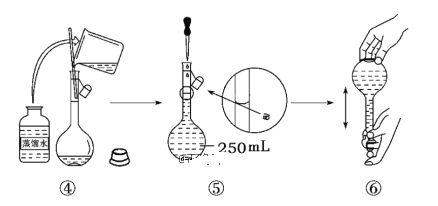
(2)根据计算,用托盘天平称取Na2CO3·10H2O的质量为__g。若定容时液面高于刻度线,应采取的措施是___。
(3)配制0.5mol·L-1盐酸溶液450mL 溶液需要玻璃仪器除烧杯、胶头滴管、量筒外还需要___。
(4)由计算知,该实验中配制0.5mol·L-1盐酸时需用量筒量取质量分数为36.5%、密度为1.2g/cm3的浓盐酸___mL。在实验中其它操作均正确,若定容时俯视刻度线,则所得盐酸溶液浓度___0.5mol·L-1(填“大于”、“等于”或“小于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用密度为1.25 gmL﹣1、质量分数为36.5%的浓盐酸配制240 mL 0.1 molL﹣1的盐酸,请回答下列问题:
(1)浓盐酸的物质的量浓度为________________________。
(2)配制240 mL 0.1 molL﹣1的盐酸
应量取浓盐酸体积/mL | 应选用容量瓶的规格/mL |
__________ | __________ |
(3)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次)__________。
A.用30 mL水洗涤烧杯内壁和玻璃棒23次,洗涤液均注入容量瓶,振荡
B.用量筒淮确量取所需的浓盐酸的体积,倒入烧杯中,再加入少量水(约30 mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线12 cm处
(4)若实验中遇到下列情况,对配制盐酸的物质的量浓度有何影响(填“偏高”“偏低”或“不变”)
①用于稀释盐酸的烧杯未洗涤__________________________________________;
②容量瓶中原有少量蒸馏水____________________________________________;
③定容时俯视观察液面________________________________________________。
(5)若实验过程中出现如下情况如何处理?
①定容时加蒸馏水时超过了刻度________________________________________;
②向容量瓶中转移溶液时不慎有溶液溅出________________________________;
③定容摇匀后发现液面下降____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
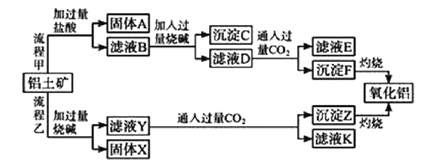
请回答下列问题:
(1)固体A的主要成分是______________(写名称)。
(2)铝土矿与过量烧碱反应的离子方程式为______________、________________。
(3)滤液D中的溶质有______________(填化学式)。
(4)指出流程乙的一个缺点是____________。
(5)氧化铝与焦炭的混合物在氮气中高温加热反应,制得新型非金属材料AlN与一种中学常见气体X。已知每转移6.02×1023个电子,有0.5mol化合物X生成,此反应的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用下列装置进行有关Cl2的实验。下列说法不正确的是


A. Ⅰ图中:实验现象证明氯气无漂白作用,氯水有漂白作用
B. Ⅱ图中:闻Cl2的气味
C. Ⅲ图中:生成棕黄色的烟
D. Ⅳ图中:若气球干瘪,证明Cl2可与NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产Na2S2O5,通常是由NaHSO3过饱和溶液经结晶脱水制得。利用烟道气中的SO2生产Na2S2O5的工艺为:
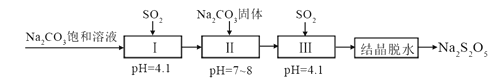
下列说法正确的是( )
A.pH=4.1时,Ⅰ中为Na2SO3溶液
B.Na2S2O5用作食品的抗氧化剂和SO2作漂白剂时,均表现还原性
C.工艺中加入Na2CO3固体、并再次充入SO2的目的是得到NaHSO3过饱和溶液
D.葡萄酒中Na2S2O5用作食品的漂白剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com