
0.5 mol·L―1的NaCl溶液中混有Na2CO3,向该溶液中滴加适量的BaCl2。滤液中NaCl的物质的量浓度为( )
A.小于0.5 mol·L―1 B.等于0.5 mol·L―1
C.大于0.5 mol·L―1 D.无法确定
 名师点拨卷系列答案
名师点拨卷系列答案科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.化学反应除了生成新物质外,还伴随着能量的变化
B.对于ΔH>0的反应,反应物的能量小于生成物的能量
C.放热反应都不需要加热就能发生
D.吸热反应在一定条件(如常温、加热等)下也能发生
查看答案和解析>>
科目:高中化学 来源: 题型:
在一固定容积的密闭容器中,保持一定温度,在一定条件下进行 反应:
A(g)+2B(g)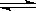 3C(g),已知加入1molA和3molB且达到平衡后生成了
3C(g),已知加入1molA和3molB且达到平衡后生成了
a mol C, 请填写下列空白:
(1)平衡时C在混合气体中的体积分数是______________(用字母a表示)。
(2)在相同实验条件下,若在同一容器中改为加入2 mol A和6 mol B,达到
平衡后,C的物质的量为______ mol(用字母a表示)。此时C在反应混合
气体中的体积分数______(填“增大”、“减少”或“不变”)。
(3)在相同实验条件下,若在同一容器中改为加入2 mol A和8 mol B,若要
求平衡后C在反应混合气体中的体积分数不变,则还应加入C___ mol。
(4)在同一容器中加入n mol A和3n mol B,达到平衡时C的物质的量为m mol,
若改变实验条件,可以使C的物质的量在m mol~2m mol之间变化,那么
n与m的关系应是____________(用字母“m”、“n”表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
某工厂采用硫酸和氢氟酸的溶液作为矿物中稀有元素的萃取液,生产要求该萃取液中的硫酸的浓度为3 mol·L-1,氢氟酸的浓度为8 mol·L-1。现有一批回收酸液共400 L,经测定其中氢氟酸浓度为12 mol·L-1,硫酸的浓度为1 mol·L-1。
现要用此回收酸液配制上述萃取液,400 L回收酸液经稀释可以得到____L 8 mol·L-1的氢氟酸。在400 L回收酸液中加入____L密度为1.84 g·cm-3、浓度为98%的浓硫酸,然后________,即可得到符合要求的萃取液。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组溶液,不用其他试剂就可以将它们区别开的是( )
A.HCl、KOH、K2SO4、K2CO3
B.NaNO3、BaCl2、Na2CO3、NaOH
C.BaCl2、CaCl2、Na2SO4、KNO3
D.KOH、K2CO3、MgSO4、H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
有八种物质:①甲烷②苯③聚乙烯④聚异戊二烯⑤2-丁炔⑥环己烷⑦邻二甲苯⑧环己烯,既能使KMnO4酸性溶液褪色,又能与溴水反应使之褪色的是
A.①④⑤⑧ B.④⑤⑧
C.②⑤⑦⑧ D.③④⑤⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2 ,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氧化钠辖液电解实验,如图所示。
 回答下列问题:
回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为 、 。
(2)闭合K开关后,a、b电极上均有气体产生.其中b电极上得到的是 ,电解氯化钠溶液的总反应方程式为 ;
(3)若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上最多能产生的氯气体积为 L(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有下列物质:
①金刚石②干冰③氯化铵④氖⑤金属锌⑥石英⑦硫化氢
(1)通过非极性键形成原子晶体的是 ;属于分子晶体,且分子为直线型的是 ;由单原子分子构成的分子晶体是 ;含有极性键的离子化合物是 ;能导电且为金属晶体的是 。(均填序号)
(2)有下列粒子:
①CCl4 ②SO3 ③P4 ④H3O+ ⑤CO32- ⑥PH3
其中属于非极性分子的是 ;粒子立体构型为平面三角形的是 ;粒子立体构型为三角锥形的是 ;粒子立体构型为四面体的是 。(均填序号)
(3)某+3价离子的电子排布式为1s22s22p63s23p63d5,则该元素在周期表中的位置是在 周期 族,画出该元素的原子结构示意图 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com