
某工厂采用硫酸和氢氟酸的溶液作为矿物中稀有元素的萃取液,生产要求该萃取液中的硫酸的浓度为3 mol·L-1,氢氟酸的浓度为8 mol·L-1。现有一批回收酸液共400 L,经测定其中氢氟酸浓度为12 mol·L-1,硫酸的浓度为1 mol·L-1。
现要用此回收酸液配制上述萃取液,400 L回收酸液经稀释可以得到____L 8 mol·L-1的氢氟酸。在400 L回收酸液中加入____L密度为1.84 g·cm-3、浓度为98%的浓硫酸,然后________,即可得到符合要求的萃取液。
科目:高中化学 来源: 题型:
下列离子方程式表达正确的是
A.向氯化铁溶液中滴加HI溶液:2Fe3++2HI==2Fe2++2H++I2
B.向NH4Al(SO4)2溶液中滴入Ba(0H)2恰好使反应完全:2Ba2++4OH-+Al3++2SO42-==2BaSO4+AlO2-+2H2O
C.1mol/L的NaAlO2溶液和2.5 mol/L的HCl等体积均匀混合2AlO2-+5H+==Al(OH)3+Al3++H2O
D.用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2==I2+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气
中的氧气与铝反应产生电流。电池总反应为:4A1+3O2+6H2O=4A1(OH)3,
下列说法不正确的是( )
A.正极反应式为:O2+2H2O+4e--=4OH--
B.电池工作时,电流由铝电极沿导线流向铂电极
C.以网状的铂为正极,可增大与氧气的接触面积
D.该电池通常只需更换铝板就可继续使用
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,在l00g饱和CuSO4溶液中加入5g无水CuSO4粉末,其结果是( )
A.溶液的质量减小 B.硫酸铜的溶解度增大
C.溶液的浓度减小 D.溶液的蓝色加深
查看答案和解析>>
科目:高中化学 来源: 题型:
现有三组溶液:①汽油和氯化钠溶液 ②75%的乙醇溶液 ③氯化钠和单质溴的水溶液(分离出溴单质),分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
0.5 mol·L―1的NaCl溶液中混有Na2CO3,向该溶液中滴加适量的BaCl2。滤液中NaCl的物质的量浓度为( )
A.小于0.5 mol·L―1 B.等于0.5 mol·L―1
C.大于0.5 mol·L―1 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于常温下电解质溶液的叙述中,正确的是( )
A.碳酸氢铵溶液和足量的氢氧化钠溶液混合的离子反应:HCO3-+OH-=CO32-+H2O
B.等物质的量浓度、等体积的氨水和盐酸混合后,c(H+)+ c(NH4+)= c(Cl-)+ c(OH-)
C.等物质的量浓度的NH4Cl溶液和NH3·H2O溶液,溶液中c(NH4+)前者小于后者
D.25℃时,pH=8的0.1mol·L-1NaX溶液中由水电离出的c (OH-)=1×10-8mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
(一) A、B、C、D是按原子序数由小到大排列的第二、三周期元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素与金属元素的原子个数比为1∶2。在一定条件下,各物质之间的相互转化关系如下图(图中部分产物未列出):
请填写下列空白:
(1)G是 。(用化学式填写)
(2)E与F反应的化学反应方程式是 。
(3)F与G的水溶液的反应生成I和D的离子方程式是 。
 (4)将2.5 g H、I和碳酸氢钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol·L-1的盐酸,所加入盐酸
(4)将2.5 g H、I和碳酸氢钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol·L-1的盐酸,所加入盐酸 的体积与产生CO2的体积(标准状况)关系如下图所示:
的体积与产生CO2的体积(标准状况)关系如下图所示:
则物质I的物质的量为_______________mol。
(二)工业上采用乙苯与CO2脱氢生产重要化工原料苯乙烯
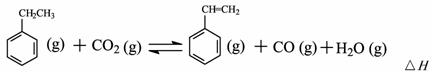 = -166KJ/mol
= -166KJ/mol
(1)在3L密闭容器内,乙苯与CO2的反应在三种不同的条件下进行实验,乙苯、CO2的起始浓度分别为1.0mol/L和3.0mol/L,其中实验Ⅰ在T1℃,0.3MPa,而实验II、III分别改变了实验其他条件;乙苯的浓度随时间的变化如图Ⅰ所示。
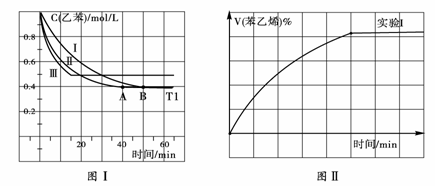
① 实验I乙苯在0—50min时的反应速率为
② 实验Ⅱ可能改变条件的是
③图II是实验Ⅰ中苯乙烯体积分数V%随时间t的变化曲线,请在图II中补画实验Ⅲ中苯乙烯体
积分数V%随时间t的变化曲线。
(2)若实验Ⅰ中将乙苯的起始浓度改为1.2 mol/L,其他条件不变,乙苯的转化率将 (填“增大”、“减小”或“不变”),计算此时平衡常数为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com