
(一) A、B、C、D是按原子序数由小到大排列的第二、三周期元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素与金属元素的原子个数比为1∶2。在一定条件下,各物质之间的相互转化关系如下图(图中部分产物未列出):
请填写下列空白:
(1)G是 。(用化学式填写)
(2)E与F反应的化学反应方程式是 。
(3)F与G的水溶液的反应生成I和D的离子方程式是 。
 (4)将2.5 g H、I和碳酸氢钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol·L-1的盐酸,所加入盐酸
(4)将2.5 g H、I和碳酸氢钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol·L-1的盐酸,所加入盐酸 的体积与产生CO2的体积(标准状况)关系如下图所示:
的体积与产生CO2的体积(标准状况)关系如下图所示:
则物质I的物质的量为_______________mol。
(二)工业上采用乙苯与CO2脱氢生产重要化工原料苯乙烯
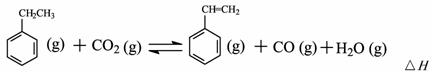 = -166KJ/mol
= -166KJ/mol
(1)在3L密闭容器内,乙苯与CO2的反应在三种不同的条件下进行实验,乙苯、CO2的起始浓度分别为1.0mol/L和3.0mol/L,其中实验Ⅰ在T1℃,0.3MPa,而实验II、III分别改变了实验其他条件;乙苯的浓度随时间的变化如图Ⅰ所示。
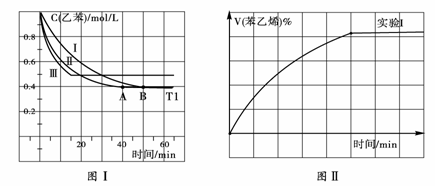
① 实验I乙苯在0—50min时的反应速率为
② 实验Ⅱ可能改变条件的是
③图II是实验Ⅰ中苯乙烯体积分数V%随时间t的变化曲线,请在图II中补画实验Ⅲ中苯乙烯体
积分数V%随时间t的变化曲线。
(2)若实验Ⅰ中将乙苯的起始浓度改为1.2 mol/L,其他条件不变,乙苯的转化率将 (填“增大”、“减小”或“不变”),计算此时平衡常数为 。
科目:高中化学 来源: 题型:
某工厂采用硫酸和氢氟酸的溶液作为矿物中稀有元素的萃取液,生产要求该萃取液中的硫酸的浓度为3 mol·L-1,氢氟酸的浓度为8 mol·L-1。现有一批回收酸液共400 L,经测定其中氢氟酸浓度为12 mol·L-1,硫酸的浓度为1 mol·L-1。
现要用此回收酸液配制上述萃取液,400 L回收酸液经稀释可以得到____L 8 mol·L-1的氢氟酸。在400 L回收酸液中加入____L密度为1.84 g·cm-3、浓度为98%的浓硫酸,然后________,即可得到符合要求的萃取液。
查看答案和解析>>
科目:高中化学 来源: 题型:
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2 ,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氧化钠辖液电解实验,如图所示。
 回答下列问题:
回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为 、 。
(2)闭合K开关后,a、b电极上均有气体产生.其中b电极上得到的是 ,电解氯化钠溶液的总反应方程式为 ;
(3)若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上最多能产生的氯气体积为 L(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
粗盐中除含有钙离子、镁离子、硫酸根离子等可溶性杂质外,还含有泥沙等不溶性杂质。我们食用的精盐是用粗盐提纯而得到的。通过教材中“粗盐的提纯”及你做过的该实验回答下列问题。
(1)如何运用最简方法检验溶液中有无SO42—?____________________________。如果有,应该如何除去SO42—? ___________________________________________________
(2)在粗盐经过溶解→过滤后的溶液中滴加饱和Na2CO3溶液,直至不再产生沉淀为止。请问这步操作的目的是________________________________________________________。
(3)将经过操作(2)后的溶液过滤。请问这一操作能除掉哪些杂质?
________________________________________________________________________。
(4)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的:
溶解时:_____________________; 过滤时:_________________; 蒸发时:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
向某浓度的铬酸(H2CrO4)溶液中滴加NaOH溶液,各粒子浓度(mol/L)与pH的关系如下表,下列说法不正确的是
| pH | c(CrO42-) | c(HCrO4-) | c(Cr2O72-) | c(H2CrO4) |
| 4 | 0.0003 | 0.1030 | 0.4480 | 0 |
| 6 | 0.0319 | 0.0899 | 0.4370 | 0 |
| 7 | 0.2645 | 0.0860 | 0.3195 | 0 |
| 9 | 0.8960 | 0.0031 | 0.0004 | 0 |
A.铬酸的第一步电离方程式为:H2CrO4 = H+ + HCrO4-
B.该铬酸溶液的物质的量浓度约为1.00 mol/L
C. pH越大,HCrO4-越容易电离出CrO42-
D. NaHCrO4溶液中:c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
元素的性质呈周期性变化的根本原因是
A、原子半径呈周期性变化
B、元素的化合价呈周期性变化
C、第一电离能呈周期性变化
D、元素原子的核外电子排布呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
现有下列物质:
①金刚石②干冰③氯化铵④氖⑤金属锌⑥石英⑦硫化氢
(1)通过非极性键形成原子晶体的是 ;属于分子晶体,且分子为直线型的是 ;由单原子分子构成的分子晶体是 ;含有极性键的离子化合物是 ;能导电且为金属晶体的是 。(均填序号)
(2)有下列粒子:
①CCl4 ②SO3 ③P4 ④H3O+ ⑤CO32- ⑥PH3
其中属于非极性分子的是 ;粒子立体构型为平面三角形的是 ;粒子立体构型为三角锥形的是 ;粒子立体构型为四面体的是 。(均填序号)
(3)某+3价离子的电子排布式为1s22s22p63s23p63d5,则该元素在周期表中的位置是在 周期 族,画出该元素的原子结构示意图 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列所作出的结论中一定正确的是( )
A.无色试液使红色石蕊试纸变蓝,结论:该试液一定是碱溶液
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO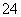
C.无色试液焰色反应呈黄色,结论:试液中一定含有Na+
D.无色试液加入碳酸钠溶液产生白色沉淀,结论:试液中含氢氧化钙
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)分别取W g钠、镁、铝与足量的盐酸反应,在相同条件下产生氢气的体积比是________。
(2)分别取0.1 mol钠、镁、铝与足量的盐酸反应,在相同条件下产生氢气的体积比是________。
(3)若产生相同物质的量的氢气,所需钠、镁、铝的质量比为________。
(4)若产生相同体积(同温同压下)的氢气,所需钠、镁、铝的物质的量比为________。
(5)若将0.2 mol钠、镁、铝分别投入到10 mL 1 mol·L-1的盐酸中,在标准状况下,产生氢气体积的大小顺序是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com