
��1���ֱ�ȡW g�ơ�þ���������������ᷴӦ������ͬ�����²����������������________��
��2���ֱ�ȡ0.1 mol�ơ�þ���������������ᷴӦ������ͬ�����²����������������________��
��3����������ͬ���ʵ����������������ơ�þ������������Ϊ________��
��4����������ͬ�����ͬ��ͬѹ�£��������������ơ�þ���������ʵ�����Ϊ________��
��5������0.2 mol�ơ�þ�����ֱ�Ͷ�뵽10 mL 1 mol��L��1�������У��ڱ�״���£�������������Ĵ�С˳����________��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(һ) A��B��C��D�ǰ�ԭ��������С�������еĵڶ���������Ԫ�صĵ��ʡ�B��E��Ϊ��ɿ����ijɷ֡�F����ɫ��Ӧ�ʻ�ɫ����G�У��ǽ���Ԫ�������Ԫ�ص�ԭ�Ӹ�����Ϊ1��2����һ�������£�������֮����ת����ϵ����ͼ��ͼ�в��ֲ���δ�г�����
����д���пհף�
��1��G�� �����û�ѧʽ��д��
��2��E��F��Ӧ�Ļ�ѧ��Ӧ����ʽ�� ��
��3��F��G��ˮ��Һ�ķ�Ӧ����I��D�����ӷ���ʽ�� ��
 ��4����2.5 g H��I��̼�����ƵĹ���������ȫ�ܽ���ˮ���Ƴ�ϡ��Һ��Ȼ�������Һ����μ���1mol��L��1�����ᣬ����������
��4����2.5 g H��I��̼�����ƵĹ���������ȫ�ܽ���ˮ���Ƴ�ϡ��Һ��Ȼ�������Һ����μ���1mol��L��1�����ᣬ���������� ����������CO2���������״������ϵ����ͼ��ʾ��
����������CO2���������״������ϵ����ͼ��ʾ��
������I�����ʵ���Ϊ_______________mol��
(��)��ҵ�ϲ����ұ���CO2����������Ҫ����ԭ�ϱ���ϩ
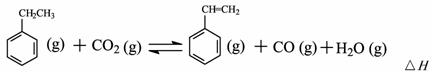 = -166KJ/mol
= -166KJ/mol
��1����3L�ܱ������ڣ��ұ���CO2�ķ�Ӧ�����ֲ�ͬ�������½���ʵ�飬�ұ���CO2����ʼŨ�ȷֱ�Ϊ1.0mol/L��3.0mol/L������ʵ�����T1��,0.3MPa,��ʵ��II��III�ֱ�ı���ʵ�������������ұ���Ũ����ʱ��ı仯��ͼ����ʾ��
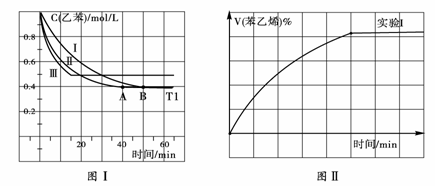
�� ʵ��I�ұ���0��50minʱ�ķ�Ӧ����Ϊ
�� ʵ�����ܸı���������
��ͼII��ʵ����б���ϩ�������V%��ʱ��t�ı仯���ߣ�����ͼII�в���ʵ����б���ϩ��
������V%��ʱ��t�ı仯���ߡ�
��2����ʵ����н��ұ�����ʼŨ�ȸ�Ϊ1.2 mol/L�������������䣬�ұ���ת���ʽ� �����������С�����䡱���������ʱƽ�ⳣ��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������ͬ���ܱ�����һ��ʢ���Ȼ��⣬��һ��ʢ��H2��Cl2�Ļ�����壬��ͬ��ͬѹ�£����������ڵ�����һ��������ͬ�� �� ��
A.���� B. ԭ������ C.�������� D.��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ơ�����þ������ȡ0.1mol���ֱ�Ͷ��������ϡH2SO4�У���ַ�Ӧ�ų������壨 ����
A������� B��һ���� C������� D�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�أ�K�����ƣ�Na���������Ͼ��кܴ�������ԣ���K��Na�Ļ�����ǿ�������Ǹ���Na�����ʶ�K�����ʵ�Ԥ�⣬������ȷ���ǣ� ����
A��K�Ļ�����ǿ�����Լ�Ӧ�ñ�����ú����
B��K�ɱ������е����������������������ڳ��ºͼ��������¾�ΪK2O
C��K��ˮ�ܹ���Ӧ��������Na��ˮ�ķ�Ӧ���ң������ﶼ������
D��K������ˮ���ҷ�Ӧ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���з�Ӧ�У�����ȱ��ֳ���ԭ���ֱ��ֳ����Ե��ǣ� ����
A��CaCO3+2HCl==CaCl2+H2O+CO2��
B��Fe+2HCl===FeCl2+H2��
C��MnO2+4HCl (Ũ) MnCl2+Cl2��+2H2O
MnCl2+Cl2��+2H2O
D��NaOH+HCl==NaCl+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪5KCl+KClO3+3H2SO4=3Cl2��+3K2SO4+3H2O������˵������ȷ���ǣ� ����
��A��KClO3���������������� ����
B���������뱻��ԭ����Ԫ�ص�������Ϊ5:1
C��H2SO4�Ȳ����������ֲ��ǻ�ԭ��������
D��1mol KClO3�μӷ�Ӧʱ��10mol����ת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪�����¿���Co2O3�Ʊ�Cl2����Ӧǰ�������������Co2O3�pH2O�pCl2��H+ ��Cl����Co2+ ��������������ȷ����
A����������ΪCl2
B���������뻹ԭ�������ʵ���֮��Ϊ1��2
C������3mol H2O���ɣ���Ӧ����2mol����ת��
D�����÷�Ӧ����2.24L Cl2ʱ����Ӧ����0.1mol����ת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼװ���У���֪A��B������Һ�������Ϊ200mL��
��1���ж�װ�õ����ƣ�A��Ϊ ��
��2��A�������ʯī��Ϊ ���� �缫��ӦʽΪ �� A�����ܷ�Ӧ��ѧ����ʽΪ ��
��3������Ӧ��ʼʱ��CuSO4��Һ��Ũ��Ϊ1.0mol/L������һ��ʱ���ȡ���缫����õ�����ͨ����0.04mole������Ӧ��A��c��Cu2+)Ϊ mol/L������仯���Բ��ƣ���

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com