
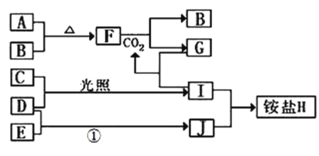
【题目】如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质,且在常温常压下都是气体;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①是化工生产中的一种重要的固氮反应。
(1)F的电子式_____________。
(2)F和CO2反应的化学方程式为__________________________,写出G溶液中逐滴加入等物质的量的I溶液反应的离子方程式_________________。
(3)铵盐H中阳离子的电子式__________,检验H中阳离子的方法是_________________。
【答案】![]() 2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2CO2=2Na2CO3+O2 ![]() +H+=
+H+=![]()
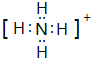 取少量H样品放入试管中,加入NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明含有
取少量H样品放入试管中,加入NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明含有![]()
【解析】
C、D在光照下发生反应,又由题意得它们是非金属单质,可得二者是H2和Cl2,则I是HCl,I和J反应得到铵盐可知J是NH3,H是NH4Cl,从而可确定C是Cl2,D是H2,E是N2。由化合物G的焰色反应为黄色,可知G为钠盐,又由题意得B是非金属单质,可是B是O2,A是Na,则F是Na2O2,G是Na2CO3,据此解答。
(1)由上面的推导过程可得F是Na2O2,含有离子键和非极性键,其电子式为![]() ;
;
(2)Na2O2 和CO2反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2,Na2CO3溶液中逐滴加入等物质的量的HCl溶液生成碳酸氢钠,反应的离子方程式是CO32-+H+=HCO3-;
(3)H是NH4Cl,其中的阳离子是NH4+,电子式为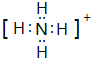 ;铵盐能与强碱反应放出氨气,则检验方法是:取少量H样品放入试管中,加入NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明含有
;铵盐能与强碱反应放出氨气,则检验方法是:取少量H样品放入试管中,加入NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明含有![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】大气污染物NOx、SO2和可吸入颗粒物(PM2.5)等会危害人体健康,影响动植物生长,因此应加强对其监测和治理。请回答:
⑴为降低NOx的排放,在汽车尾气系统中装置催化转化器,可将NOx还原成N2排出。写出NO被CO还原的化学方程式:______________。
⑵某研究小组对PM2.5进行监测时,取其样本用蒸馏水处理制成待测试样,测得有关数据如下:
离子 | H+ | Na+ |
|
|
|
浓度(mol/L) | 1×10-5 | 2×10-5 | 3×10-5 | 4×10-5 |
试样中c(H+)=______mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象得出的结论正确的是
操作 | 现象 | 结论 | |
A | 将 | 溴水和酸性高锰酸钾溶液均褪色 |
|
B | 向 | 先产生白色沉淀,后产生红褐色沉淀 |
|
C | 向滴有酚酞的 | 有白色沉淀生成,溶液红色变浅 |
|
D | 将 | 产生白色沉淀 | 酸性: |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将VmLNO和NO2的混合气体通过水吸收后,得到amL无色气体A。将此无色气体A与等体积的O2混合,再通过水充分吸收后,收集到4mL无色气体B。试回答:
(1)气体A是___;气体B是___。
(2)A气体的体积是___毫升。
(3)V的取值范围是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用如下装置制备氯酸钾和次氯酸钠。
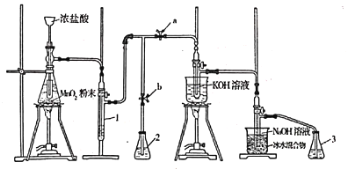
回答下列问题:
(1)滴加浓盐酸的漏斗伸入试管底部,其原因为________________________________。
(2)装置1中盛放的试剂为________;若取消此装置,对实验造成的影响为________。
(3)装置中生成氯酸钾的化学方程式为________________________,产生等物质的量的氯酸钾和次氯酸钠,转移电子的物质的量之比为________。
(4)装置2和3中盛放的试剂均为________。
(5)待生成氯酸钾和次氯酸钠的反应结束后,停止加热。接下来的操作为打开________(填“a”或“b”,下同),关闭________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A.醋酸与氢氧化钠溶液反应:CH3COOH+OH-=CH3COO-+H2O
B.铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑
C.氯化铝溶液与氨水反应:Al3++4OH-=AlO![]() +2H2O
+2H2O
D.碳酸钠溶液与稀盐酸的反应:Na2CO3+2H+=CO2↑+H2O+2Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)2017年中科院某研究团队通过设计一种新型Na-Fe3O4/HZSM-5多功能复合催化剂,成功实现了CO2直接加氢制取辛烷值汽油,该研究成果被评价为“CO2催化转化领域的突破性进展”。
已知:H2(g)+1/2O2(g)=H2O(l) ΔH1 = -aKJ/mol
C8H18(1)+25/2O2(g)=8CO2(g)+9H2O(1) ΔH2= -bKJ/mol
试写出25℃、101kPa条件下,CO2与H2反应生成汽油(以C8H18表示)的热化学方程式_________________________________。
(2)利用CO2及H2为原料,在合适的催化剂(如Cu/ZnO催化剂)作用下,也可合成CH3OH,涉及的反应有:
甲:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H= — 53.7kJ·mol-1 平衡常数K1
CH3OH(g)+H2O(g) △H= — 53.7kJ·mol-1 平衡常数K1
乙:CO2(g)+H2(g) ![]() CO(g)+H2O(g) △H= + 41.2kJ·mol-1 平衡常数K2
CO(g)+H2O(g) △H= + 41.2kJ·mol-1 平衡常数K2
①CO(g)+2H2(g) ![]() CH3OH(g)的平衡常数K=______(用含K1、K2的表达式表示),该反应△H_____0(填“大于”或“小于”)。
CH3OH(g)的平衡常数K=______(用含K1、K2的表达式表示),该反应△H_____0(填“大于”或“小于”)。
②提高CO2转化为CH3OH平衡转化率的措施有___________(填写两项)。
③催化剂和反应体系的关系就像锁和钥匙的关系一样,具有高度的选择性。下列四组实验,控制CO2和H2初始投料比均为1:2.2,经过相同反应时间(t1min)。
温度(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) | 综合选项 |
543 | Cu/ZnO纳米棒材料 | 12.3 | 42.3 | A |
543 | Cu/ZnO纳米片材料 | 11.9 | 72.7 | B |
553 | Cu/ZnO纳米棒材料 | 15.3 | 39.1 | C |
553 | Cu/ZnO纳米片材料 | 12.0 | 70.6 | D |
由表格中的数据可知,相同温度下不同的催化剂对CO2的转化为CH3OH的选择性有显著影响,根据上表所给数据结合反应原理,所得最优选项为___________(填字母符号)。
(3)以CO、H2为原料合成甲醇的反应为:CO(g)+2H2(g)![]() CH3OH(g)。在体积均为2L的三个恒容密闭容器Ⅰ、Ⅱ、Ⅲ中,分别都充入1molCO和2molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变。下图为三个容器中的反应均进行到5min时H2的体积分数示意图,其中有一个容器反应一定达到平衡状态。
CH3OH(g)。在体积均为2L的三个恒容密闭容器Ⅰ、Ⅱ、Ⅲ中,分别都充入1molCO和2molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变。下图为三个容器中的反应均进行到5min时H2的体积分数示意图,其中有一个容器反应一定达到平衡状态。
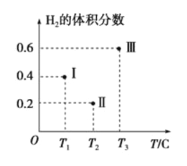
①0~5min时间内容器Ⅱ中用CH3OH表示的化学反应速率为_________________。
②三个容器中一定达到平衡状态的是容器________(填写容器代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿色化学对化学反应提出了“原子经济性”(原子节约)的新概念及要求。理想的原子经济性反应是原料分子中的全部转变成所需产物,不产生副产物,实现零排放。以下反应中符合绿色化学原理的是
A. 乙烯与O2在银催化下生成环氧乙烷![]()
B. 乙烷与氯气制备氯乙烷
C. 苯和乙醇为原料,在一定条件下生产乙苯
D. 乙醇和浓硫酸共热制备乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据乙烯、乙酸、乙醇的性质类比,有机物的结构简式如图,该物质的化学性质中说法正确的有:

①能加聚也能缩聚;②1mol该有机物分别可跟1 molBr2、4molH2加成;③可使酸性KMnO4溶液褪色;④可跟Na2CO3溶液反应;⑤1mol该有机物可消耗2 mol NaOH;⑥可在碱性条件下水解
A.2个B.3个C.4个D.5个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com