
【题目】下列反应的离子方程式书写正确的是( )
A.醋酸与氢氧化钠溶液反应:CH3COOH+OH-=CH3COO-+H2O
B.铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑
C.氯化铝溶液与氨水反应:Al3++4OH-=AlO![]() +2H2O
+2H2O
D.碳酸钠溶液与稀盐酸的反应:Na2CO3+2H+=CO2↑+H2O+2Na+
 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:
【题目】蒽(![]() )反应生成化合物X(立体对称图形),如下图所示:
)反应生成化合物X(立体对称图形),如下图所示:
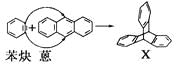
(1)蒽与X都属于________(填选项,下同)。
A.环烃 B.烷烃 C.芳香烃
(2)苯炔的分子式为________,苯炔不具有的性质是________。
A.能溶于水 B.能发生氧化反应
C.能发生加成反应 D.常温常压下为气体
(3)1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决,它不能解释下列 事实。
A.苯不能使溴水褪色 B.苯能与H2发生加成反应
C.溴苯没有同分异构体 D.邻二溴苯只有一种
现代化学认为苯分子碳碳之间的键是 。
(4)下列属于苯的同系物的是________。
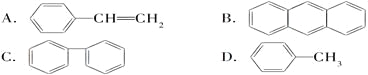
(5)能发生加成反应,也能发生取代反应,同时能使溴水因反应而褪色,也能使酸性高锰酸钾溶液褪色的是________。
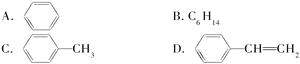
它是生产某塑料的单体,写出合成该塑料的化学方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向如图所示的两个容积相同的刚性容器中分别充入气体M、N(如表所示),使两容器中压强相等。打开开关k,两容器中的气体充分混合后,恢复至常温,容器内的气体压强(固体影响忽略不计)由大到小的顺序正确的是 ( )
装置 | 编号 |
|
|
|
|
| M | NH3 | HI | NO | H2 |
N | Cl2 | Cl2 | O2 | O2 |
A.①=④>②=③ B.①=④>②>③
C.④>①>②>③D.①>④>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,阅读表格回答问题:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
一 | ① | |||||||
二 | ② | ③ | ④ | |||||
三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)元素③的原子序数为___________,被选做相对原子质量标准的核素是___________(填核素符号);
(2)①与②、③、④、⑦、⑧形成的化合物中,最稳定的是___________(填化学式);表中所示元素最高价氧化物对应的水化物中酸性最强的是___________(填化学式);
(3)请画出元素④与⑤按原子个数比1︰1组成的淡黄色固体物质的化学式___________;
(4)请写出⑤的最高价氧化物对应水化物与⑥的单质反应的离子方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质,且在常温常压下都是气体;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①是化工生产中的一种重要的固氮反应。
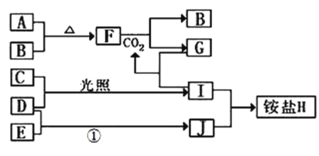
(1)F的电子式_____________。
(2)F和CO2反应的化学方程式为__________________________,写出G溶液中逐滴加入等物质的量的I溶液反应的离子方程式_________________。
(3)铵盐H中阳离子的电子式__________,检验H中阳离子的方法是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷、乙烯是常见的化工原料。
(1)甲烷的分子构型为___(填“平面正方形”或“正四面体形”)。
(2)写出甲烷和氯气按分子数之比为1∶1发生反应的化学方程式:___。该反应的类型为___反应。
(3)乙烯中含有官能团的名称为___。
(4)写出乙烯与氢气发生反应的化学方程式:___。该反应的类型为___反应。
(5)下列试剂不能鉴别甲烷和乙烯的是___(填字母)。
a.溴水
b.酸性高锰酸钾溶液
c.NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用如下方法由NaOH溶液制取Na2CO3·10H2O:
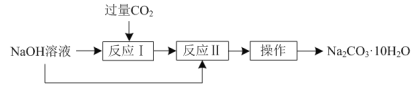
(1)“反应Ⅰ”的化学方程式为___。
(2)“反应Ⅱ”的离子方程式为___。
(3)“操作”的名称为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,利用培养皿探究NH3的性质。实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面。下表中对实验现象所做的解释正确的是( )

选项 | 实验现象 | 解释 |
A | 浓盐酸附近产生白烟 | NH3与浓盐酸反应产生了NH4Cl固体 |
B | 浓硫酸附近无明显现象 | NH3与浓硫酸不发生反应 |
C | 氯化物溶液变浑浊 | 该溶液一定是AlCl3溶液 |
D | 干燥红石蕊试纸不变色,湿润红石蕊试纸变蓝 | NH3是一种可溶性碱 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是
A. 常温常压下,124 g P4中所含P—P键数目为4NA
B. 100 mL 1mol·L1FeCl3溶液中所含Fe3+的数目为0.1NA
C. 标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
D. 密闭容器中,2 mol SO2和1 mol O2催化反应后分子总数为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com