
【题目】在强酸性溶液中能大量共存并且溶液为无色透明的离子组是
A.Ba2+ Na+ NO3- S2-B.Mg2+ Cl- Al3+ SO42-
C.K+ Cl- HCO3- NO3-D.Ca2+ Na+ Fe3+ NO3-
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:
【题目】已知A、B、C、D为气体,其中A为黄绿色气体。E、F为固体且均含三种元素,G是氯化钙,它们之间的转换关系如下图所示:
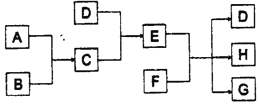
(1)D的化学式是__________________________。
(2)H的电子式为__________________________。
(3)A和B反应生成C的化学方程式是__________________________。
(4)将A通入F的澄清溶液中所发生反应的离子方程式是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
(1)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为______(写离子符号);若所得溶液c(HCO3)∶c(CO32)=2∶1,溶液pH=___________。(室温下,H2CO3的K1=4×107;K2=5×1011)
(2)CO2与CH4经催化重整,制得合成气:
CH4(g)+ CO2(g) ![]() 2CO (g)+ 2H2(g)
2CO (g)+ 2H2(g)
①已知上述反应中相关的化学键键能数据如下:
化学键 | C—H | C=O | H—H | C |
键能/kJ·mol1 | 413 | 745 | 436 | 1075 |
则该反应的ΔH=_________。分别在VL恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1 mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是_______(填“A” 或“B ”)。
②按一定体积比加入CH4和CO2,在恒压下发生反应,温度对CO和H2产率的影响如图3所示。此反应优选温度为900℃的原因是________。

(3)O2辅助的Al~CO2电池工作原理如图4所示。该电池电容量大,能有效利用CO2,电池反应产物Al2(C2O4)3是重要的化工原料。
电池的负极反应式:________。
电池的正极反应式:6O2+6e![]() 6O2
6O2
6CO2+6O2![]() 3C2O42
3C2O42
反应过程中O2的作用是________。
该电池的总反应式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室由Al盐制备Al(OH)3最佳选择NH3·H2O,其离子反应方程式:____________________________
(2)12.4g Na2X含有0.4mol Na+, Na2X的摩尔质量为________。
(3)由氨气和氢气组成的混合气体的平均相对分子质量为12,则氨气和氢气的物质的量之比为_________
(4)已知![]() 离子可与R2-离子反应,R2-被氧化为R单质,
离子可与R2-离子反应,R2-被氧化为R单质,![]() 的还原产物中M为+3价;又已知100mL c(
的还原产物中M为+3价;又已知100mL c(![]() )=0.2 mol·L-1的溶液可与100mL c(R2-)=0.6 mol·L-1的溶液恰好完全反应,则n值为__________
)=0.2 mol·L-1的溶液可与100mL c(R2-)=0.6 mol·L-1的溶液恰好完全反应,则n值为__________
A.4B.5C.6D.7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]
锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为________________。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Ⅰ1(Zn)_______Ⅰ1(Cu)(填“大于”或“小于”)。原因是________________。
(3)ZnF2具有较高的熔点(872 ℃),其化学键类型是_________;ZnF2不溶于有机溶剂而ZnCl2、ZnBr2、ZnI2能够溶于乙醇、乙醚等有机溶剂,原因是________________。
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为________________,C原子的杂化形式为________________。
(5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为_______________。六棱柱底边边长为a cm,高为c cm,阿伏加德罗常数的值为NA,Zn的密度为________________g·cm-3(列出计算式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把2.3g钠放入水中,要使每100个水分子中含有1个Na+离子,所需水的质量是( )
A. 184g B. 181.8g C. 180g D. 183.6g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列四种有机物的有关说法正确的是

A. 甲的名称为反-2-丁烯
B. 乙中所有碳原子一定处于同一平面
C. 1mol丙分别与足量Na、NaOH、NaHCO3反应,消耗这三种物质分别是3mol、4mol、1mol
D. 丁的二氯代物有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“纳米材料”是当今材料科学研究的前沿,其研究成果广泛应用于催化及军事科学中。“纳米材料”是指研究、开发出的直径从几纳米至几十纳米的材料。如将“纳米材料”分散到液体分散剂中,所得混合物可能具有的性质是
A.所得分散系不稳定B.能全部透过半透膜
C.不能透过滤纸D.有丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在光照条件下,等物质的量的CH3CH3与Cl2充分反应后,得到产物中物质的量最多的是( )
A. CH3CH2ClB. CH2ClCH2Cl
C. CCl3CH3D. HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com