
【题目】下列过程吸收热量的是
A. 酸碱中和反应 B. 浓硫酸的稀释
C. 水的分解 D. 化学反应中化学键的形成
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】姜黄素有抗氧化、保肝护肝、抑制肿瘤生长等功能。它的结构简式如图所示

已知:
下列有关姜黄素的说法正确的是
A. 姜黄素在一定条件下能发生水解、加成、氧化反应
B. 1个姜黄素分子一定有15个原子共平面
C. 1mol姜黄素在镍(Ni)、加热条件下最多10molH2发生加成反应
D. 姜黄素的分子式为C21H18O6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据科技日报网报道,南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现烯丙醇高效、绿色合成。烯丙醇及其化合物可成甘油、医药、农药香料,合成维生素E和KI及天然抗癌药物紫杉醇中都含有关键的烯丙醇结构。丙烯醇的结构简式为CH2=CH-CH2OH。请回答下列问题:
(1)基态镍原子的价电子排布式为___________________。
(2)1 mol CH2=CH-CH2OH含__________molσ键,烯丙醇分子中碳原子的杂化类型为_____________。
(3)丙醛(CHCH2CHO)的沸点为49℃,丙烯醇(CH2=CHCH2OH)的沸点为91℃,二者相对分子质量相等,沸点相差较大的主要原因是_______________________________。
(4)羰基镍[Ni(CO)4)用于制备高纯度镍粉,它的熔点为-25℃,沸点为43℃。羰基镍晶体类型是_________________。
(5)Ni2+能形成多种配离子,如[Ni(NH3)6]2+、[Ni(CN)2]2-和[Ni(SCN)2]-等。NH3的空间构型是_____________,与SCN-互为等电子体的分子为____________。
(6)“NiO”晶胞如图所示。

①氧化镍晶胞中原子坐标参数:A(0,0,0)、B(1,1,0),则C原子坐标参数为____________。
②已知:氧化镍晶胞密度为dg·cm-3,NA代表阿伏加德罗常数的值,则Ni2+半径为__________nm(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝广泛应用于电子陶瓷等工业领域。在一定条件下,AlN可通过以下反应合成:Al2O3+N2+3C![]() 2AlN+3CO。有关该反应下列叙述正确的是
2AlN+3CO。有关该反应下列叙述正确的是
A. 上述反应中,N2是还原剂,Al2O3是氧化剂
B. 上述反应中,每生成1 mol AlN需转移3 mol电子
C. AlN中氮的化合价为+3
D. AlN的摩尔质量为41 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向X的溶液中,加入Y试剂,产生的沉淀示意图如图所示情形的是(注意线段的斜率)
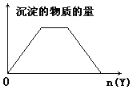
A. 向含NaOH的NaAlO2溶液中滴加盐酸
B. 向HCl和AlCl3的混合液中滴加NaOH
C. 向NH4Cl和AlCl3的混合液中滴加NaOH
D. 向NaOH和Ca(OH)2的混合液中通入CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.5molH2S中,约含有________________个氢原子,共有_________mol原子,其质量为____________克,在标况下体积为_____________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组提取三处被污染的水源进行了如下分析,给出了如下实验信息:其中一处被污染的水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E为五种常见化合物,均由下表中的离子形成:
阳离子 | K+ Na+ Cu2+ Al3+ |
阴离子 | SO42- HCO3- NO3- OH- |
为了鉴别上述化合物,分别完成以下实验,其结果是
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加入过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出B、D的化学式:B________,D________。
(2)写出D、E发生反应的离子方程式:___________________________。
(3)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,该化合物为__________。
(3)C常用作净水剂,用离子方程式表示其净水原理:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A.硅元素广泛存在于自然界中,天然单质硅叫硅石
B.二氧化硅在信息高速传输中有重要应用
C.常温下硅很稳定,不与强酸发生反应
D.二氧化硅可用于制造玻璃、单质硅、光导纤维
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com