
【题目】在100mL的溶液中溶有0.1mol NaCl和0.1mol MgCl2 , 此溶液中Cl﹣的物质的量浓度为( )
A.3 mol/L
B.2 mol/L
C.0.3 mol/L
D.0.2 mol/L
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】为探究苯与溴的取代反应,甲用如图装置Ⅰ进行如下实验: 
将一定量的苯和溴放在烧瓶中,同时加入少量铁屑,3~5min后发现滴有AgNO3的锥形瓶中有浅黄色的沉淀生成,即证明苯与溴发生了取代反应.
(1)装置I中①的化学方程式为 , . ②中离子方程式为 .
(2)①中长导管的作用是 .
(3)烧瓶中生成的红褐色油状液滴的成分是 , 要想得到纯净的产物,可用试剂洗涤.洗涤后分离粗产品应使用的仪器是 .
(4)乙同学设计如图所示装置Ⅱ,并用下列某些试剂完成该实验.可选用的试剂是:苯;液溴;浓硫酸;氢氧化钠溶液;硝酸银溶液;四氯化碳.a的作用是 . b中的试剂是 . 比较两套装置,装置Ⅱ的主要优点是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在蒸馏实验中,下列叙述不正确的是
A.在蒸馏烧瓶中加入约1/3体积的自来水,并放入几粒碎瓷片
B.蒸馏操作中,烧瓶可直接加热
C.冷水从冷凝管的下口入,上口出
D.收集冷凝水时,应弃去开始蒸馏出的部分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列鉴别碳酸钠和碳酸氢钠固体的方法中错误的是( )
A.分别取两种固体样品,加热产生气体的是碳酸氢钠
B.分别取样溶于水后加入氯化钙溶液,若有白色沉淀则是碳酸钠
C.分别取样溶于水后加入澄清石灰水,若有白色沉淀则是碳酸钠
D.分别取等质量的两种固体样品,与足量的硫酸反应,产生气体较多的是碳酸氢钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( ) 
A.图1某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH 变化曲线,用等浓度NaOH溶液分别和等体积b、c处溶液反应,消耗NaOH溶液体积Vb>Vc
B.图2中曲线a、b分别表示过量纯锌、过量粗锌(含Cu、C杂质)与同浓度等体积盐酸反应过程中产生H2体积的变化趋势
C.图3表示25℃用0.1000 molL﹣1NaOH溶液滴定20.00mL 0.1000 molL﹣1 CH3COOH溶液得到的滴定曲线
D.图4表示某温度下AgBr在水中的沉淀溶解平衡曲线的图象,向AgBr的饱和溶液中加入NaBr固体,可以使溶液由c点到b点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产中容易产生有害的含铬工业废水和含氰废水,严重威胁人类的健康和安全.图1是处理工业含铬废水和含氰废水的工艺流程. 
已知:含铬废水中铬的存在形式为Cr2O72﹣ , Cr元素常见的化合价+3、+6,含氰废水中有CN﹣存在.
请回答下列问题:
(1)含氰废水中有CN﹣存在,其中C元素的化合价为 .
的代数式表示)
(2)向含铬废水中加下列哪种物质将pH调整到2~3,(填字母).
a.稀盐酸 b.稀硫酸 c.稀硝酸
的代数式表示)
(3)pH>10时,图中反应Ⅱ中的NaClO可以将CN﹣氧化为两种无毒物质,请写出反应的离子方程式 .
的代数式表示)
(4)经过图中反应Ⅰ和图中反应Ⅱ后,将两种废水混合的目的是
的代数式表示)
(5)工业上也常用电解法处理酸性含铬废水,用耐酸电解槽,铁板作电极,槽中盛放酸性含Cr2O72﹣的废水,原理示意图如图2: 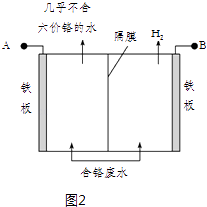
阳极区域溶液中发生反应的离子方程式为 . 若不考虑气体的溶解,当收集到H2 13.44L(标准状况)时,被还原的Cr2O72﹣物质的量为 . 为了使Cr3+和Fe3+转化为Fe (OH)3和Cr(OH)3沉淀,向反应后的溶液中加入一定量的烧碱,若溶液中c(Fe3+)=2.0×10﹣12 molL﹣1 , 则溶液中c (Cr3+)=molL﹣1 . (已知:Ksp[Fe (OH)3]=4.0×10﹣38 , Ksp[Cr(OH)3]=6.0×10﹣31)
的代数式表示)
(6)在25℃下,将a molL﹣1 NaCN溶液与0.01molL﹣1盐酸等体积混合(忽略溶液体积变化),反应后测得溶液pH=7,HCN的电离常数Ka为 . (用含a的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅及其化合物在材料领域中应用广泛。下列说法正确的是 ( )
A. 光导纤维的主要成分是硅 B. 晶体硅能用来制造太阳能电池
C. 水晶项链的主要成分是硅酸盐 D. 二氧化硅是一种半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量CO2通入某浓度的NaOH溶液中,反应后得到溶液A,向A溶液中逐滴滴入某浓度稀盐酸,加入V(HCl)与生成n(CO2)的关系如图所示.下列有关叙述正确的是( ) 
A.通入的CO2气体为11.2 L
B.A溶液中n(NaHCO3)=2n(Na2CO3)
C.A溶液中既含NaOH,又含Na2CO3
D.A溶液中一定只有Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释实验事实的离子方程式正确的是( )
A.硫酸亚铁在空气中被氧化:4Fe2++3O2+6H2O═4Fe(OH)3
B.向CH2Br﹣COOH中加入足量的NaOH溶液并加热:CH2Br﹣COOH+OH﹣ ![]() CH2Br﹣COO﹣+H2O
CH2Br﹣COO﹣+H2O
C.FeCl3溶液中通入SO2 , 溶液黄色褪去:2Fe3++SO2+2H2O═2Fe2++SO42﹣+4H+
D.碳酸钠溶液滴入酚酞变红:CO32﹣+2H2O?H2CO3+2OH﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com