
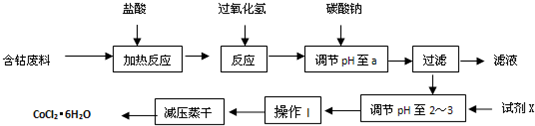
CoCl2��6H2O��һ������Ӫ��ǿ�������Ժ��ܷ��ϣ�������Fe��Al�����ʣ���ȡCoCl2��6H2O��һ���¹�����������ͼ��
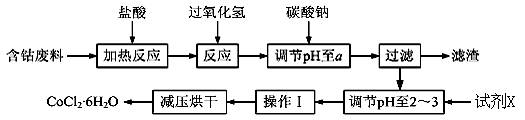
��֪��
���������ᷴӦ�Ļ�ѧ����ʽΪ��Co��2HCl=CoCl2��H2��[��Դ:ѧ���ơ���]
��CoCl2��6H2O�۵�86�棬������ˮ�����ѵȣ��������ȶ�����������110~120��ʱ��ʧȥ�ᾧˮ����ж�����ˮ�Ȼ��ܡ�
�۲���������������������ʽ����ʱ��Һ��pH���±���
|
������ |
Fe(OH)3 |
Fe(OH)2 |
Co(OH)2 |
Al(OH)3 |
|
��ʼ���� |
2.3 |
7.5 |
7.6 |
3.4 |
|
��ȫ���� |
4.1 |
9.7 |
9.2 |
5.2 |
��ش��������⣺
��1���������¹����У��á����ᡱ����ԭ�����С�����������Ļ��ᡱֱ���ܽ⺬�ܷ��ϣ�����Ҫ�ŵ�Ϊ ��
��2������̼���Ƶ���pH��a��a�ķ�Χ�� ��pH����a����ˣ������Լ�X����Һ��pH������2-3�������õ��Լ�XΪ___________��
��3�����������3������ʵ������������� �� ���ˡ�
��4���Ƶõ�CoCl2��6H2O���ѹ��ɵ�ԭ���� ��
��5��Ϊ�ⶨ��Ʒ��CoCl2��6H2O������ijͬѧ��һ��������Ʒ����ˮ���������м���������AgNO3��Һ�����ˣ�����������ɺ������������ͨ�����㷢�ֲ�Ʒ��CoCl2��6H2O��������������100������ԭ������� ��д������ԭ��
��6����ʵ�����У�Ϊ�˴�������Ʒ�л�ô�����CoCl2��6H2O�����õķ����� ��
 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ������ | Fe��OH��3 | Fe��OH��2 | Co��OH��2 | Al��OH��3 | ��ʼ���� | 2.3 | 7.5 | 7.6 | 3.4 | ��ȫ���� | 4.1 | 9.7 | 9.2 | 5.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
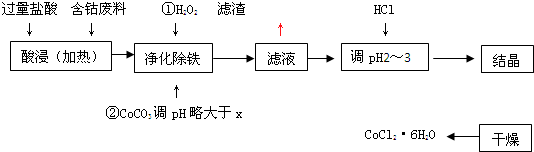
| ��ѧʽ | �ܶȻ�������ʱ��Ksp | ������ȫʱ��pH | �Ȼ��ܾ�������� |
| Co��OH��2 | 5.9��10-15 | 9.4 | CoCl2?6H2O�ʺ�ɫ���������ȶ���110��C��120��Cʱ��ˮ�����ɫ��ˮ�Ȼ��� |
| Fe��OH��2 | 1.6��10-14 | 9.6 | |
| Fe��OH��3 | 1.0��10-35 | x |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
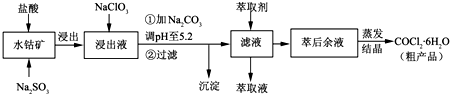
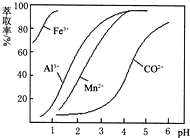
| ������ | Fe��OH��3 | Fe��OH��2 | Co��OH��2 | Al��OH��3 | Mn��OH��2 |
| ��ʼ���� | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| ��ȫ���� | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| ������ | Fe��OH��3 | Fe��OH��2 | Co��OH��2 | Al��OH��3 |
| ��ʼ���� | 2.3 | 7.5 | 7.6 | 3.4 |
| ��ȫ���� | 4.0 | 9.7 | 9.2 | 5.2 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com