
【题目】膳食纤维具有突出的保健功能,近年来受到人们的普遍关注,被世界卫生组织称为人体的“第七营养素”。木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构简式如图所示。下列有关芥子醇的说法正确的是( )
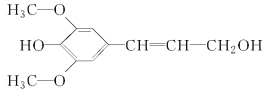
A.芥子醇的分子式是C11H12O4
B.芥子醇分子中所有碳原子不可能在同一平面
C.芥子醇能与FeCl3溶液发生显色反应
D.1 mol芥子醇与足量溴水发生加成或取代反应时共消耗3 mol Br2
科目:高中化学 来源: 题型:
【题目】某化学课外活动小组为了验证元素非金属性递变规律,设计了如下图所示的两套实验方案进行实验探究:
方案一 方案二
方案二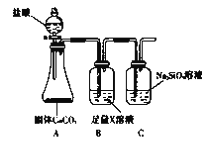
(1)根据方案一装置回答以下问题:
Ⅰ.写出装置①发生的化学反应方程式:_________________。
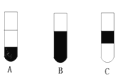
Ⅱ.若将反应后②中的溶液倒入CCl4中,出现的现象与下图吻合的是________。(填代号)
Ⅲ.装置③中的现象是____________________。
(2)根据方案二装置回答以下问题:
Ⅰ.方案二验证元素非金属性递变的理论依据是:__________________________。
Ⅱ.B装置的作用是_________________,X是_______________________。
Ⅲ.能说明碳元素和硅元素非金属性强弱的实验现象是______________________。
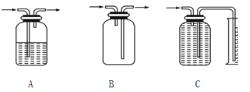
(3)方案一、二中多次用到广口瓶,在化学实验中广口瓶可以配合玻璃管和其他简单仪器组成各种功能的装置,被称为气体实验的“万能瓶”。分析下图中广口瓶组合装置的用途;
A____________;B_____________;C____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答问题:
(1)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合,其结构如下图所示。

组成M的元素中,电负性最大的是__________(填名称)。
(2)钛元素基态原子未成对电子数为________个,能量最高的电子占据的能级符号为________。
(3)①已知Al 的第一电离能为578 kJ·mol-1、第二电离能为1 817 kJ·mol-1、第三电离能为2 745 kJ·mol-1、第四电离能为11 575 kJ·mol-1。请解释其第二电离能增幅较大_______________________________。Al单质为面心立方晶体,其晶胞参数a=0.405 nm,晶胞中铝原子的配位数为________。
②第二电离能I(Cu)________(填“>”或“<”)I (Zn)。
(4)在硅酸盐中,SiO44—四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。
图(b)为一种无限长单链结构的多硅酸根(其中硅原子数为n):其中Si原子的杂化形式为_________,Si与O的原子数之比为__________,化学式为____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是模拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是( )
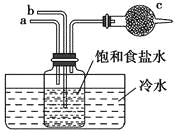
A. a通入CO2,然后b通入NH3,c中放碱石灰
B. b通入NH3,然后a通入CO2,c中放碱石灰
C. a通入NH3,然后b通入CO2,c中放蘸稀硫酸的脱脂棉
D. b通入CO2,然后a通入NH3,c中放蘸稀硫酸的脱脂棉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法正确的是![]()
![]()
A. 1mol苯分子中含有C=C双键数目为3NA
B. 标准状况下,11.2LCCl4中含有的共价键数目为2NA
C. 1mol乙烯和乙醇的混合物完全燃烧时消耗O2的分子数为3NA
D. 常温常压下,17g羟基含有的电子总数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2020年1月在武汉爆发了新型冠状病毒肺炎,引起了全世界人民的关注。瑞德西韦(remdesivir)是一种可能的特效药,其结构简式如图所示,下列说法不正确的是(磷酸酯与酯性质类似)( )
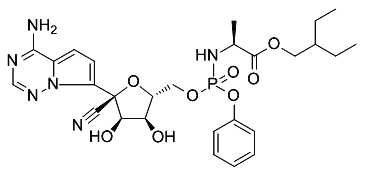
A.瑞德西韦的分子式是C27H32N6O8P
B.已知一个碳原子连接四个不同的原子(或基团)是具有手性的,瑞德西韦具有的手性碳原子有5个
C.若只考虑酯键的水解,瑞德西韦在水解后会成为4个分子
D.瑞德西韦的合成原料之一可能有苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 铝粉投入到NaOH溶液中:2Al+2OH-+2H2O══ 2AlO2—+3H2↑
B. AlCl3溶液中加入足量的氨水:Al3++ 3OH- ══ Al(OH)3↓
C. 三氯化铁溶液中加入铁粉![]()
D. FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氮及其化合物在化工生产和国防工业中具有广泛应用。请回答:
(1)科学家研究利用某种催化剂,成功实现将空气中的碳氧化合物和氮氧化合物转化为无毒的大气循环物质。已知:
①N2(g)+O2(g)![]() 2NO(g) ΔH1=+180kJ·mol1
2NO(g) ΔH1=+180kJ·mol1
②NO2(g)+CO(g)![]() NO(g)+CO2(g) ΔH2=-235kJ·mol1
NO(g)+CO2(g) ΔH2=-235kJ·mol1
③2NO(g)+O2(g)![]() 2NO2(g) ΔH3=-112kJ·mol1
2NO2(g) ΔH3=-112kJ·mol1
则反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g)的ΔH=__kJ·mol1,有利于提高CO平衡转化率的条件是__(填标号)。
N2(g)+2CO2(g)的ΔH=__kJ·mol1,有利于提高CO平衡转化率的条件是__(填标号)。
A.高温低压 B.低温高压 C.高温高压 D.低温低压
某温度下,在体积为2L的容器中加入2molNO、2molCO,达到平衡时CO的转化率是50%,其平衡常数为__。
(2)在密闭容器中充入10molCO和8molNO,发生反应,如下图为平衡时NO的体积分数与温度,压强的关系。
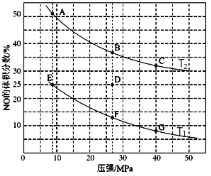
①由图判断,温度T1__T2(填“低于”或“高于”),理由是__?升高温度时,下列关于该反应的平衡常数(K)和速率(v)的叙述正确的是__填标号)。
A.K、V均增加 B.K增加,v减小
C.K减小,V增加 D.K、V均减小
②压强为20MPa、温度为T2下,若反应进行到10min达到平衡状态,容器的体积为2L,则此时CO的转化率=__,用CO2的浓度变化表示的平均反应速率v(CO2)=__,该温度下,如图所示A、B、C对应的pA(CO2)、pB(CO2)、pC(CO2)从大到小的顺序为__。
③若在D点对反应容器降温的同时缩小体积至体系压强增大,重新达到的平衡状态可能是图中A~G点中的__点。
(3)用活化后的V2O5作催化剂,氨气将NO还原成N2的一种反应历程如图所示。
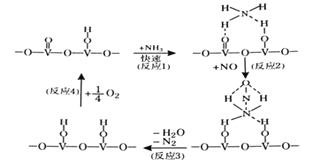
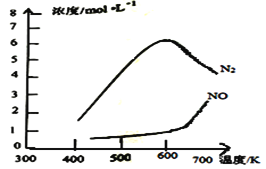
测得该反应的平衡常数与温度的关系为1gK=5.08+217.5/T,该反应是__反应(填“吸热”或“放热”)。该反应的含氮气体浓度随温度变化如图所示,则将NO转化为N2的最佳温度为__;当温度达到700K时,发生副反应的化学方程式__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应:2SO2(g)+O2(g)![]() 2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
A. 增大压强 B. 升高温度 C. 使用催化剂 D. 多充O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com