
����Ŀ����ͼ��ʾ�ס����ǵ绯ѧʵ��װ�á�

��1�� ���ס������ձ��о�ʢ��NaCl��Һ��
�� ����ʯī���ϵĵ缫��ӦʽΪ______________________________��
�� �����ܷ�Ӧ�����ӷ���ʽΪ________________________________��
�� ��ʪ��ĵ���KI��ֽ�������ձ��Ϸ���������ֽ�ȱ�������ɫ��������Ϊ������Cl2���������ɵ�I2������Ӧ��Cl2��I2�����ʵ���֮��Ϊ5��1�������������ᣬ�÷�Ӧ�Ļ�ѧ����ʽΪ________________________
��2�� ���ס������ձ��о�ʢ��CuSO4��Һ��
�� ���������ϵĵ缫��ӦʽΪ___________________________��
�� �����ʼʱ����ʢ��200 mL pH��5��CuSO4��Һ(25 ��)��һ��ʱ�����Һ��H��Ϊ1����Ҫʹ��Һ�ָ������ǰ��״̬��������Һ�м���__________(��д���ʵĻ�ѧʽ)________g��
���𰸡���1����2H2O+O2+4e-�T4OH-
��2Cl-+2H2O![]() H2��+Cl2��+2OH-
H2��+Cl2��+2OH-
��5Cl2+I2+6H2O�T10HCl+2HIO3
��2����Fe-2e-�TFe2+
��CuO����CuCO3����0.8����1.24��
��������
�����������1�� ���ס������ձ��о�ʢ��NaCl��Һ���� ��Ϊ����������ʴ��ʯī��������ʯī���ϵĵ缫��ӦʽΪ2H2O+O2+4e-�T4OH-���� ���ݵ�������ʯī����������Ϊ�ö��Ե缫����Ȼ�����Һ�������ܷ�Ӧ�����ӷ���ʽΪ2Cl-+2H2O ![]() H2��+Cl2��+2OH-��������Ӧ��Cl2��I2�����ʵ���֮��Ϊ5��1�������������ᣬ���ݵ����غ㣬5mol����ʧ����10mol��2mol I2�õ���10mol����Ļ��ϼ�����Ϊ+5�ۣ��÷�Ӧ�Ļ�ѧ����ʽΪ5Cl2+I2+6H2O�T10HCl+2HIO3����2�� ���ס������ձ��о�ʢ��CuSO4��Һ���� ��Ϊԭ��أ���Ϊ�����������ϵĵ缫��ӦʽΪFe-2e-�TFe2+������2CuSO4+2H2O
H2��+Cl2��+2OH-��������Ӧ��Cl2��I2�����ʵ���֮��Ϊ5��1�������������ᣬ���ݵ����غ㣬5mol����ʧ����10mol��2mol I2�õ���10mol����Ļ��ϼ�����Ϊ+5�ۣ��÷�Ӧ�Ļ�ѧ����ʽΪ5Cl2+I2+6H2O�T10HCl+2HIO3����2�� ���ס������ձ��о�ʢ��CuSO4��Һ���� ��Ϊԭ��أ���Ϊ�����������ϵĵ缫��ӦʽΪFe-2e-�TFe2+������2CuSO4+2H2O![]() 2Cu+O2��+2H2SO4��Ҫʹ��Һ�ָ�ԭ״̬���ɼ���CuO(��CuCO3)��һ��ʱ�����Һ��pH��Ϊ1����c(H+)=0.1mol/L��n(H+)=0.2L��0.1mol/L=0.02mol�����ɵ�ⷴӦ��֪������Cu�����ʵ���Ϊ0.01mol����Cuԭ���غ��֪��m(CuO)=0.01mol��80g/mol=0.8g����m(CuCO3)=0.01mol��124g/mol=1.24g��
2Cu+O2��+2H2SO4��Ҫʹ��Һ�ָ�ԭ״̬���ɼ���CuO(��CuCO3)��һ��ʱ�����Һ��pH��Ϊ1����c(H+)=0.1mol/L��n(H+)=0.2L��0.1mol/L=0.02mol�����ɵ�ⷴӦ��֪������Cu�����ʵ���Ϊ0.01mol����Cuԭ���غ��֪��m(CuO)=0.01mol��80g/mol=0.8g����m(CuCO3)=0.01mol��124g/mol=1.24g��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ѧ�������ʵ���Ũ�ȵĸ����,����Ϊ1 mol/L������Һ�ĺ���Ӧ��( )
A��ÿ1 Lˮ�к���1 mol H2SO4
B��ÿ1 L��Һ�к�1 mol H+
C����98 g H2SO4����1 Lˮ������ɵ���Һ
D��ָÿ1 L������Һ�к���98 g H2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�����仯������һ�������µ�ת����ϵ��
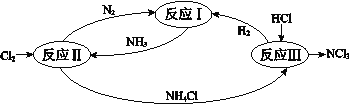
��1�����ݷ�ӦI����500����20MPaʱ����N2��H2ͨ�뵽���Ϊ2 L���ܱ������У���Ӧ�����и������ʵ����ʵ����仯����ͼ��ʾ:

��1��10 min����NH3��ʾ�÷�Ӧ��ƽ�����ʣ�v(NH3)= ��
��2����10~20min��NH3Ũ�ȱ仯��ԭ������� (����ĸ)��
a.���˴���
b.�����¶�
c.����NH3�����ʵ���
��3���ÿ��淴Ӧ�ﵽƽ��ı�־��_______(����ĸ)��
a��3v(H2)�� = 2v(NH3)��
b�����������ܶȲ�����ʱ��仯
c�������ڵ���ѹǿ������ʱ����仯
d�� N2��H2��NH3�ķ�����֮��Ϊ1��3��2
��4����һ��ƽ��ʱ��ƽ�ⳣ��K1�� (����ѧ����ʽ��ʾ)��
��5����ӦI��N2(g)+3H2(g)![]() 2NH3(g) ��H=�C92.4 kJmol��1
2NH3(g) ��H=�C92.4 kJmol��1
��ͼ��ʾ��ӦI��ƽ��������NH3������������¶Ȼ�ѹǿ�仯�����ߣ�ͼ��L(L1��L2)��X�ֱ�����¶Ȼ�ѹǿ������X��������____________(��¶ȡ���ѹǿ��)���ж�L1��L2�Ĵ�С��ϵ��˵������_______ ��
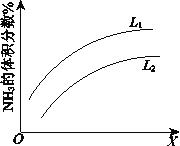
��6����ӦII����һ����ӦΪ
2NH3 (g)+3Cl2(g) =N2 (g) +6HCl(g) ��H=�C462 kJmol��1
��֪��![]()
�Ͽ�1 mol H�CN����Ͽ�1 mol H�CCl�������������ԼΪ_________ kJ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʢ������A������ɱ���ܱ������У�����ѹǿһ��������B��������Ӧ��A(s��+2B(g�� ![]() 4C(g��+D(g������H��0����һ���¶ȡ�ѹǿ�´ﵽƽ�⣮ƽ��ʱC�����ʵ���������B�����ʵ����ı仯��ϵ��ͼ������˵����ȷ����( ��
4C(g��+D(g������H��0����һ���¶ȡ�ѹǿ�´ﵽƽ�⣮ƽ��ʱC�����ʵ���������B�����ʵ����ı仯��ϵ��ͼ������˵����ȷ����( ��
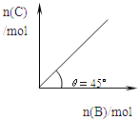
�������¶����ߺ���ͼ������45��
�����ټ���B���������淴Ӧ���ʾ�������
�����ټ���B�����ٴδﵽƽ��ʱ��Ӧ��ϵ�����ܶȲ���
��ƽ��ʱB��ת����Ϊ50%
A���٢� B���ڢ� C���٢� D���ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Һ���ܴ���������ǣ� ��
A.Al3+��NO3����OH����Cl��
B.H+��Ba2+��Ag+��Cl��
C.Fe2+��Fe3+��Na+��NO3��
D.Ca2+��H+��Cl����CO32��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� ��Դ��ȱ���������ٵ��ش����⡣�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ������˼״�����Ϊ21���͵�����ȼ�ϡ�
��1����֪�ڳ��³�ѹ�£�
��2CH3OH(l)ʮ3O2(g) 2CO2(g)+4H2O(g) ��H=��1275.6 kJ��mol��1
��H2O(l) H2O(g) ��H=+44.0 kJ.mol-1
д����ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽ ��
��2��ij�ּ״�������ȼ�ϵ���Dz��ò���Ϊ�缫��ϡ�������������Һ���乤��ʱ�����ĵ缫��Ӧʽ�ɱ�ʾΪ ��
�� ����Ҳ��һ�����ȼ�ϣ�������ȫȼ��ʱ��Ч�ʽ��Ͳ�������ж����������Ⱦ��
��֪��CH4(g)+2O2(g)��CO2(g)+2H2O(l) ��H1���D890.3kJ/mol
2CO(g)+O2(g)��2CO2(g) ��H2���D566.0kJ/mol
��3�����������ȫȼ������һ����̼��Һ̬ˮʱ����Ч��ֻ����ȫȼ��ʱ��________��������������1λС������
��4������ȼ�ϵ�ؿ���������������������ͼ�����ü���ȼ�ϵ�ص��50 mL 2 mol/L���Ȼ�ͭ��Һ��װ��ʾ��ͼ��
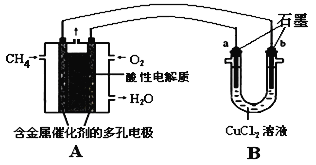
��ش𣺵���·����0.1 mol����ͨ��ʱ��________������a������b����������________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ˮ����ˮ������Ӧ������ˮ�������Է�Ӧ��
������ʾ���ڲ�ͬ�¶��£�������ˮ������Ӧ�IJ��ﲻͬ���¶ȵ���570 ��ʱ������FeO������570��ʱ������Fe3O4��
ij�о���ѧϰС������ͼ��ʾʵ��װ�ã���ɻ�ԭ������ˮ������Ӧ��ʵ�飬�������о��������ɡ�
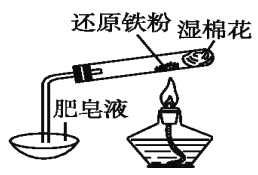
��1������Һ��������____________��
��2����ͬѧΪ̽��ʵ����Թ��ڵĹ��庬����Щ���ʣ�������������ʵ�飺
ʵ���� | ʵ����� | ʵ������ |
�� | ȡ������ɫ��ĩX�����Թ��У��������ᣬ�� | ��ɫ��ĩ���ܽ⣬��Һ����ɫ�����������ݲ��� |
�� | ���Թ��еμӼ���KSCN��Һ���� | ��Һû�г��ֺ�ɫ |
��������ʵ�飬��ȷ��������һ�����ڵ�������______________�������IJ����������ܷ�ȷ����Ӧ�����в�����Fe3O4��________������ܡ����ܡ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ӦX+Y==M +NΪ���ȷ�Ӧ,�Ը÷�Ӧ������˵������ȷ��
A��X������һ������M
B�� Y������һ������N
C��X��Y��������һ������M��N��������,
D .��÷�ӦΪ���ȷ�Ӧ,�ʲ��ؼ��ȾͿɷ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com