
科目:高中化学 来源:不详 题型:单选题
 Fe(OH)2 +2Ni(OH)2下列推断不正确的是( )
Fe(OH)2 +2Ni(OH)2下列推断不正确的是( )| A.放电时,Fe为正极,Ni2O3为负极 |
| B.充电时,阴极上的电极反应式是:Fe(OH)2 +2e-→Fe+2OH- |
| C.放电时,负极上的电极反应式是:Ni2O3 +3H2O+2e-→2Ni(HO)2 +2OH- |
| D.该蓄电池的电极必须是浸在某种碱性电解质溶液中 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
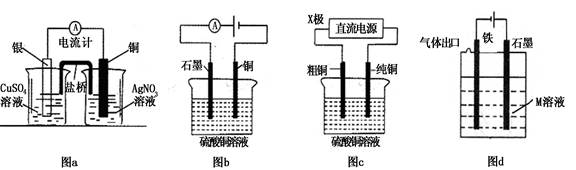
| A.图a是原电池装置,可以实现化学能转化为电能 |
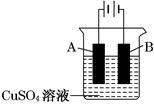
| B.图b电解一段时间后,加入适量CuCO3固体,可以使硫酸铜溶液恢复到原浓度 |
| C.图c中的X极若为负极,则该装置可实现粗铜的精炼 |
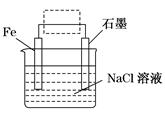
| D.图d中若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
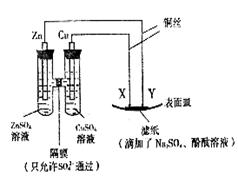
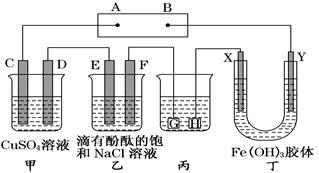
| A.Y为阴极,发生还原反应 |
| B.X为正极,发生氧化反应 |
| C.Y与滤纸接触处有氧气生成 |
| D.X为滤纸接触处变红 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
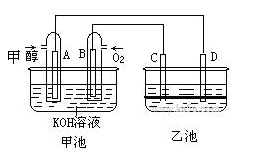
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
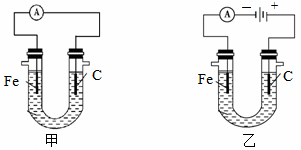
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com