
| 元素 | 相关信息 |
| X | X原子基态时最外层电子数是其内层电子总数的2倍 |
| Y | Y的基态原子最外层电子排布式为nsnnpn+2 |
| Z | Z元素的最高正价与负价代数和为6 |
| W | W基态原子未成对电子数是前30号元素中最多的 |
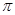 键数目为 。
键数目为 。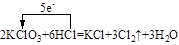 (3分)
(3分)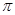 键数目为2NA。
键数目为2NA。

科目:高中化学 来源:不详 题型:单选题
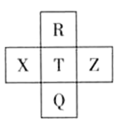
| A.Ⅰ A族元素与ⅦA族元素间形成的化合物一定含离子键 |
| B.第二周期元素从左到右,最高正价从+1递增到+7,最低负价从—4升高到—1 |
| C.同主族非金属元素的简单阴离子还原性越强,其气态氢化物的稳定性越弱 |
| D.同周期主族金属元素的化合价越高,其原子失电子能力越强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.通常用小黑点来表示电子的多少,黑点密度大,电子数目大 |
| B.黑点密度大,单位体积内电子出现的机会大 |
| C.通常用小黑点来表示电子绕核作高速圆周运动 |
| D.电子云图是对电子运动无规律性的描述 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.P、S、Cl的最高价含氧酸的酸性依次增强 |
| B.第ⅠA族元素铯的同位素137Cs比133Cs多4个质子 |
| C.第二周期元素从左到右,最高正价从+1递增到+7 |
| D.元素周期表位于金属与非金属分界线附近的元素属于过渡元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.作调味剂 | B.用于食物防腐 | C.用于氯碱工业 | D.用于医疗 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②④ | B.②③⑤ | C.①②③ | D.③④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com