
����Ŀ����һ��þ���Ͻ�����þ��������������8��9������200mLϡHNO3ʹ��ǡ����ȫ�ܽ⣬����NO�����ڱ�״���µ����Ϊ3.36L��Ȼ������Һ���ټ���NaOH��Һ�������������ٷ����仯�����ˡ�ϴ�ӡ����������
��1���Ͻ����������ʵ���Ϊ_________��������ó���������Ϊ_________��
��2����ȡ200 mLԭϡHNO3��300 mLϡ������ɻ��Һ�������м�ͭ��ʹ֮��ַ�Ӧ���õ�ֻ��һ�����ʵ���Һ��������ϡ��������ʵ���Ũ�ȡ���������̲����֣�____________
���𰸡� 0.09 mol 5.22 g 3 mol��L��1
��������(1).��Ͻ����������ʵ���Ϊx�����������ʵ���ͬ��Ϊx���ɵ���غ�ã����ɵ���������ʵ���Ϊ![]() �����x=0.09�����ԺϽ����������ʵ���Ϊ0.09mol��þ�����ʵ���Ϊ0.09mol����������NaOH��Һ���������������ᱻ�ܽ⣬�������������ٷ����仯��˵������Ϊ������þ�������������Ϊ0.09��58g/mol=5.22g��
�����x=0.09�����ԺϽ����������ʵ���Ϊ0.09mol��þ�����ʵ���Ϊ0.09mol����������NaOH��Һ���������������ᱻ�ܽ⣬�������������ٷ����仯��˵������Ϊ������þ�������������Ϊ0.09��58g/mol=5.22g��
(2).�������·�Ӧ3Cu+2NO3-+8H+=3 Cu2++2NO��+4H2O������֪�ã��Ͻ���ȫ�ܽ���ÿmolþ��ȫ��Ӧ��������![]() ��ÿmol����ȫ��Ӧ��������
��ÿmol����ȫ��Ӧ��������![]() ������������0.6mol����(2)��Ӧ�У�8H+�а��������ṩ��2����λ�������ṩ��6����λ�����Է�Ӧ��������0.9mol������ϡ��������ʵ���Ũ��
������������0.6mol����(2)��Ӧ�У�8H+�а��������ṩ��2����λ�������ṩ��6����λ�����Է�Ӧ��������0.9mol������ϡ��������ʵ���Ũ��![]() ��
��


 Ӧ����㲦ϵ�д�
Ӧ����㲦ϵ�д� ״Ԫ����ϵ�д�
״Ԫ����ϵ�д� ͬ������ϵ�д�
ͬ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����X��A12O3��Fe2O3��Cu��SiO2�е�һ�ֻ���������ɡ�
I.��������ʵ�飺

��ش�
��1������õ���ɫ��Һ���ù�����һ�������Ļ�ѧ��Ӧ�ǣ������ӷ���ʽ��ʾ��______��
��2����ӦII�Ļ�ѧ����ʽ��______________ ��X��һ�����е�������________��
II.Ϊ��һ��ȷ�����������X�ijɷ֣���ȡ9.4gX��������ʵ�顣

��3���������˲������ȱ��ϴ�Ӳ��裬��ʹ�òⶨ�Ĺ���������_______����ƫ��ƫС����Ӱ�죩
��4�������������ɫ��Һ��������Ϊ___________________��5��ԭ�������SiO2��������___________X��һ�������е�������_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������(C9H10O2)����ɫ����ˮ��������Һ�壬�׳ư�Ϣ�����������������ܼ������ϡ�����˵����ȷ���ǣ� ��
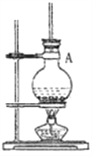
A. ����ͼװ���Ʊ�����������,Ӧ����ƿA���ȼ���3mLŨH2SO4��4g�����ᣬȻ�������ƿ����������10mL�Ҵ�
B. ��ͼ���Ʊ������������ļ���װ�ã�A�в������ܸ�������������Ч������
C. �Ƶõı����������ֲ�Ʒ����ͨ��ˮϴ��NaOH��Һϴ�ӡ�ˮϴ����ȥ�����������еIJ�������
D. ����ʽΪC9H10O2,���б��������뱥��NaHCO3��Һ��Ӧ�ų�������л��ﹲ��15��(���������칹)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʼ���ˮ�У���ˮ�ĵ����ܲ����ٽ����õ���
A. NH4Cl B. NaOH C. NaCl D. H2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����(Bi)�뵪ͬ�壬��������(BiOCl)�㷺���ڲ��Ե��ϡ����������������ɫ������������ȡ�һ�����û���ͭ���̲�����ͭת¯�̳�(������Ļ�����֮��,����CuSO4��ZnSO4��CuS��Fe2O3��PbSO4��As2O3)�Ʊ��ߴ���������Ĺ����������£�

��ش�
(1)BiOCl��BiԪ�صĻ��ϼ�Ϊ__________��
(2)����������á���Һ1���м���Zn�ۣ���ҪĿ����__________________________��
(3)����ͭ��ʱ,�е��������ɣ��䷴Ӧ�����ӷ���ʽΪ____________________________��
(4)�����顱ʱ,�¶����ߣ���Ľ����ʽ��ͣ���ԭ��Ϊ____________________________��
(5)�����顱ʱ�������Һ��pH=3.0,��ʱBiCl3������Ӧ�Ļ�ѧ����ʽΪ__________��
(6)����Ǧ���顱ʱ,���Բ����������ַ�����
�ټ�������ǻ���ʯ����(HAP)����Һ2��HAP��Һ�̱�(L/S)��Ǧ����ȥ�����Լ������������Ĺ�ϵ���±���
L/S | 125��1 | 50��1 | 25��1 | 15��1 |
Pb2+ȥ����/% | 84.86 | 94.15 | 95.40 | 96.83 |
As3+ȥ����/% | 98.79 | 98.92 | 98.34 | 99.05 |
m(����)/g | 2.34 | 2.33 | 2.05 | 1.98 |
ʵ����Ӧ���õ�L/S=__________��
�����������������Һ2�м���Fe2(SO4)3,������pH,����FeAsO4����������Һ��c(AsO43-)=1��10-9mol/L,�Ҳ�����Fe(OH)3����,��ʱ��Һ��pHΪ__________��(��֪��1g2=0.3;FeAsO4��Fe(OH)3��Ksp�ֱ�Ϊ5��10-21��4��10-38��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����Ȼ�ѧ����ʽ��˵����ȷ����
A. H2��ȼ����Ϊ285.8 kJ��mol1�����ʾH2ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��H2(g)+ ![]() O2
O2![]() H2O(g) ��H=285.8 kJ��mol1
H2O(g) ��H=285.8 kJ��mol1
B. �к���Ϊ57.3 kJ��mol1����NaOH����ᷴӦ���к��ȿ��Ա�ʾ���£�NaOH(aq)+CH3COOH(aq)![]() CH3COONa(aq)+H2O(l) ��H=57.3 kJ��mol1
CH3COONa(aq)+H2O(l) ��H=57.3 kJ��mol1
C. ��֪��C(s�����ʯ)+O2(g)![]() CO2(g) ��H=395.4 kJ��mol1��C(s��ʯī)+O2(g)
CO2(g) ��H=395.4 kJ��mol1��C(s��ʯī)+O2(g)![]() CO2(g) ��H=393.5 kJ��mol1����C(s�����ʯ)
CO2(g) ��H=393.5 kJ��mol1����C(s�����ʯ)![]() C(s��ʯī)��H=1.9 kJ��mol1
C(s��ʯī)��H=1.9 kJ��mol1
D. ��֪1 mol CH4��ȫȼ������CO2��Һ̬ˮ�ų�890.4 kJ����������÷�Ӧ��ת��1 mol����ʱ�ų�������Ϊ222.6 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������50 kg�Ľ����˺�FeԪ��Լ2 g����Ҫ��Fe2����Fe3����ʽ�����������ڡ�Fe2���ױ����գ���ƶѪ�߲�������Ӧ���京Fe2����������(��FeSO4)������Vc����ʹʳ���е�Fe3��ת��ΪFe2����
�������о�������Fe2��![]() Fe3����ת�����ڹ���A�У�Fe2����_______��������B��Fe3����______����
Fe3����ת�����ڹ���A�У�Fe2����_______��������B��Fe3����______����
��VcʹFe3��ת��ΪFe2����VC����һ��������___________������____________�ԡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������10 mL 0.1 mol��L-1 NaOH��Һ����μ���0.1 mol��L-1��һԪ��HA����ҺpH�ı仯������ͼ��ʾ��

��1��a�㣨������Ϊ10����ʾ��Һ������Ũ�ȴӴ�С��˳��Ϊ___________________ ������c(Na+)______c(A-)+c(HA��������>����<������=������
��2��c����ʾ��Һ�У�c(Na+)_____c(A-)������>����<������=������
��3��b����ʾ��Һ�У�c(A-)_____c(HA��������>����<������=������
��4��a��b��c����ʾ��Һ��,ˮ�ĵ���̶�������__________________________��
��5�����µζ������ᵼ��V(HA)ƫ�����____________��
A���ζ��ܵζ�ǰ���������ζ���������ʧ
B����ƿϴ�Ӻ�û�и���
C���ζ�ʱ��ƿ����Һ�彦��
D���ζ���ʼǰ����ʱƽ�ӣ��ζ��յ㣬����ʱ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com