
髙纯氧化铁(a-Fe2O3)是现代电子工业重要材料。实验室用硫铁矿烧渣 (Fe2O3、FeO、SiO2等)为原料制备髙纯氧化铁的步骤如下。请回答有关问题: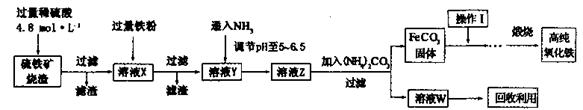
(1)过滤操作中的玻璃仪器为________。
(2)实验室需240mL4.8mol ? L-1的硫酸溶液,若用18.4 mol ? L-1的浓硫酸进行配制,所需要的最主要仪器为________。
(3)溶液X发生反应的离子方程式为________。
(4)简述如何检验溶液Z中的阴离子________。
(5)操作I的名称是________。列举W的一种用途________。
(6) 某实验小组设计的氨气制备实验流程为:发生装置→净化→收集→尾气处理,则接口的连接顺序是_______________。
(7)将多余的氨气分别通入水中或盐酸中,若得到25℃0.1 mol.L-1的NH3 ? H2O溶液或NH4Cl溶液,请你设计实验,比较NH3 ? H2O的电离程度和NH4Cl的水解程度大小。
(每空2分,共14分)(1)漏斗、烧杯、玻璃棒(少一项扣1分,最多扣2分)
(2)250ml容量瓶(木容积不得分) (3)2Fe3++Fe=3Fe2+
(4)取少量溶液Z于试管中,然后加入稀盐酸,无沉淀产生,再加入BaCl2溶液,有白色沉淀产生,证明有SO42-。 (5)洗涤(1分);用于化肥(1分) (6)a→e→d→h→g→f
(7)常温下,将等物质的量浓度(0.1mol/L)、等体积的氨水、NH4Cl溶液混合,若混合液pH>7,表明电离程度大于水解程度;否则电离程度小于水解程度。或用pH计分别测25℃时0.1mol/L氨气、NH4Cl溶液的pH,然后比较c(OH-)和c(H+),若c(OH-)>c(H+)表明电离程度大于水解程度;若c(OH-)<c(H+)表明电离程度小于水解程度。
解析试题分析:(1)过滤操作中的仪器有铁架台(带铁圈)、漏斗、烧杯、玻璃棒,其中玻璃仪器是漏斗、烧杯、玻璃棒。
(2)由于没有250ml容量瓶,所以要配制240ml稀硫酸,所需要的最主要仪器为250ml容量瓶。
(3)由于溶液X中含有铁离子,因此加入铁粉发生反应的离子方程式为2Fe3++Fe=3Fe2+。
(4)根据流程图可知,溶液Y是氯化亚铁和硫酸的混合液。通入氨气后生成硫酸铵,因此溶液Z中含有SO42-。检验SO42-的操作是取少量溶液Z于试管中,然后加入稀盐酸,无沉淀产生,再加入BaCl2溶液,有白色沉淀产生,证明有SO42-。
(5)固体从溶液中过滤出来后,需要洗涤。因此操作I的名称是洗涤;溶液Z中加入碳酸铵后生成碳酸亚铁和硫酸铵,因此W是硫酸铵,其主要用途是用于化肥。
(6)根据装置图可知,A是发生装置。由于氨气密度小于空气且极易溶于水,所以用E装置收集氨气,D装置进行尾气吸收。由于生成的氨气中含有水蒸气,因此要干燥管高燥氨气,所以正确的连接顺序是a→e→d→h→g→f。
(7)要比较NH3 ? H2O的电离程度和NH4Cl的水解程度大小,可以通过测量等浓度、等体积的二者混合液的pH,或直接测量等浓度溶液的pH。即常温下,将等物质的量浓度(0.1mol/L)、等体积的氨水、NH4Cl溶液混合,若混合液pH>7,表明电离程度大于水解程度;否则电离程度小于水解程度。或用pH计分别测25℃时0.1mol/L氨气、NH4Cl溶液的pH,然后比较c(OH-)和c(H+),若c(OH-)>c(H+)表明电离程度大于水解程度;若c(OH-)<c(H+)表明电离程度小于水解程度。
考点:考查过滤、物质的量浓度配制等基本实验操作;铁及其化合物的性质;SO42-的检验;氨气制备、收集、除杂以及尾气处理;电离程度与水解程度比较等实验方案的设计等


 培优三好生系列答案
培优三好生系列答案科目:高中化学 来源: 题型:实验题
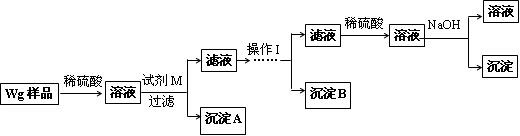
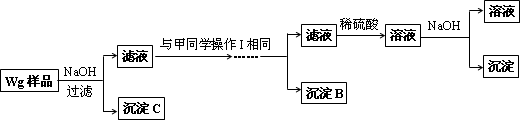
某混合金属粉末,除Mg外,还含有Al、Zn中的一种或两种,含量都在10%以上.某研究小组设计实验探究该混合金属粉末中铝、锌元素的存在.
所用试剂:样品、pH试纸、稀H2SO4、NaOH溶液、稀NH3·H2O.
该小组探究过程如下:
●查阅资料:
| ①镁、铝、锌都是银白色的金属; ②锌(Zn)可以与NaOH溶液反应生成H2; ③Zn(OH)2为白色固体,难溶于水,可溶于强碱及NH3·H2O; ④Zn2+易形成络合物如[Zn(NH3)4]2+,该络合物遇强酸分解生成Zn2+、NH4+. |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
I.下图表示从固体混合物中分离Q的2种方案,请回答有关问题。
(1)选用方案(i)时,Q应该具有的性质是_____________,残留物应该具
有的性质是__________________________________。
(2)选用方案(ii)从某金属粉末(含有Au、Ag和Cu)中分离Au,加入的试剂为____________。
(3)为提纯某Fe2O3样品(主要杂质有SiO2.Al2O3),参照方案(i)和(ii),请设计一种以框图形式表示的实验方案(注明物质和操作):
______________________________________________________________________________。
Ⅱ.某种含有少量氧化钠的过氧化钠样品(己知样品质量为1.560g、锥形瓶和水的质量为
190.720g),利用右下图所示装置测定混合物中Na2O2的质量分数,每隔相同时间读得电
子天平的数据如下表:
(4)写出Na2O2与H2O反应的化学方程式:________________________________________.
(5)计算Na2O2质量分数时,必需的数据是_________________________________________.
不必作第6次读数的原因是_____________________________________________________.
(6)测定上述样品(1.560g)中Na2O2质量分数的另一种方案,其操作流程如下:
操作②的名称是____________,该方案需直接测定的物理量是_____________ ,测定过程中
需要的仪器有电子天平、蒸发皿、酒精灯,还需要___________、__________(固定、夹
持仪器除外),在转移溶液时,如溶液转移不完全,则Na2O2质量分数的测定结果_______(填
“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
化学学习中,有关物质性质的学习离不开实验,请阅读下列对应的内容,并按要求完成填空
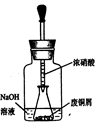
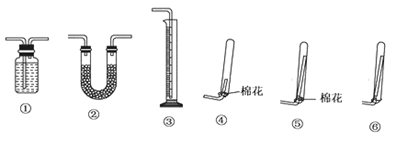
(1)实验室经常用烧杯进行性质实验研究,如图所示装置及下表中试剂,过一段时间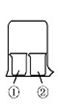
| 实验编号 | ①中的物质 | ②中的物质 |
| 1 | 淀粉碘化钾溶液 | 浓硝酸 |
| 2 | 酚酞溶液 | 浓硫酸 |
| 3 | 氯化铝溶液 | 浓氨水 |
| 4 | 湿润的红纸 | 饱和氯水 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
碳酸钠俗称纯碱,其用途很广。实验室中,用碳酸氢铵和饱和食盐水可制得纯碱。各物质在不同温度下的溶解度见表。
  温度℃ 温度℃溶解度 溶质 g/100g水 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
| NH4HCO3 | 15.8 | 21.0 | 27.0 | | | | |
| NaHCO3 | 8.2 | 9.6 | 11.1 | 12.7 | 14.4 | 16.4 | |
| NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
下面是提纯大理石(主要杂质是氧化铁)的流程图:
按要求回答下列问题:
(1)在工业生产中,将块状大理石磨成粉末,并在反应池中安装搅拌机。目的是________。
(2)操作Ⅱ中A物质最好应选择___________(填化学式),在该过程中要随时测定pH,在实验室中用pH试纸测定溶液pH的操作是______________________________。
(3)检验Fe3+已完全生成Fe(OH)3沉淀的方法是________________________________。
(4)由滤液B得到晶体B,操作过程包括___________(填操作名称)、冷却结晶。
(5)某化学小组在实验中用浓硝酸和铜反应制取二氧化氮并探究二氧化氮是否能支持木炭的燃烧,其实验装置图如下:
①按气流方向连接各仪器接口,顺序为a→______→______→______→______→f。装置C、装置D 的作用分别是__________________、__________________。
②实验开始后,能证明二氧化氮支持燃烧的实验现象是_______________________。
③已知二氧化氮和碳反应生成两种物质的量比为1:1有毒气体,则该反应的化学方程式为:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
现从锌制品加工企业回收的废渣(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质)来制取氧化锌,流程如下:
有关氢氧化物完全沉淀的pH见下表:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 6.7 | 8.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
FeSO4·7H2O俗称绿矾,广泛用于医药和工监领域。
(1)已知FeSO4·7H2O晶体在加热条件下发生如下反应:
 。利用下图装置检验该反应的气体产物。
。利用下图装置检验该反应的气体产物。
请填写下列空白:
①仪器的连接顺序为 (用a~i的字母表示)。
②装置C中的试剂X化学式为 ;该装置中冷水的作用是 。
(2)以下是FeSO4·7H2O的实验窒制备流理图。
根据题意完成下列填空:
①反应Ⅱ需要l00mL l.5mol·L-1l的稀硫酸溶解洁净的铁屑,用质量分数为98%、密度为1.84g·cm-3的浓硫酸配制。所用的仪器有量筒、烧杯、玻璃捧、胶头滴管及 ,量取浓硫酸的体积为 。
②反应1需要加热数分钟,其原因是 ;操作A为 。
③测定FeSO4·7H2O产品中Fe2+含量的常用方法是KMnO4溶液滴定法。已知称取3.0g FeSO4·7H2O产品,配制成溶液,用硫酸酸化的0.01000moL·L-1 KMnO4溶液滴定,消耗KMnO4溶液的体积为200.00mL。发生反应的离子方程式为 ,计算上述样品中FeSO4·7H2O的质量分数为 (保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关实验现象的预测或装置的选用正确的是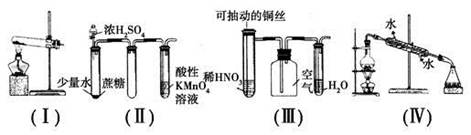
| A.用装置(Ⅰ)加热草酸晶体获取某些气体(草酸晶体的熔点101.5 ℃,分解温度约为150 ℃) |
| B.用装置(Ⅱ)进行实验时,酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 |
| C.用装置(Ⅲ)进行实验时,广口瓶内先有浅红棕色气体出现后又变为无色,且不会产生空气污染 |
| D.用装置(Ⅳ)分离溴苯和苯的混合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com