
����Ŀ����Ӿ�ص�ˮ������Ҫ����Ϊϸ��������ļ��緱ֳ���µġ�
(1)�������ʿ�����Ϊ��Ӿ�ص���������һ��ˮ����������Ӿ��������ˮ�е�����Ӧ������0.3~0.5mg/L��pH������7.4~7.6�����������ϸ����������������ͷ�ֳ��
��¶����Ӿ��ˮ���������������(28~30��)�ᵼ�����������ֳ����ԭ����_____________��
���������Ĵ���ʹ��Ҳ�ᵼ�����������ֳ����Ӿ��ˮ���̡���ˮ�е������Դ�������ʽ���ڣ��ټ���H2O2��������Ҳ�ᵼ�³�ˮ���̣�д����������H2O2������Ӧ��������Ļ�ѧ����ʽ_________________��
(2)������ˮ���̵ķ�����Ϊ�岽��
������ԭ����ͭ���ӿ���ʹҶ�����ж���������ö�������CuSO4��ҺҲ�ܹ�ɱ������ԭ����_________������CuSO4��Һ����Ҫ��ˮѭ��ϵͳ����������_____________��
������������ɱ��������Ҫ���ֳ��Ļ�ѧ������_____________��
��ѡ��Na2CO3����pH��7.5���û�ѧ��������ֽ�����ԭ��_____________��
���ۺ��Ȼ����ɽ�������ͱ�ɱ���ϸС����������صף��ڶ��콫�ص׳����Ƴ���ϡ�;ۺ��Ȼ�����������壬�����ӷ�Ӧ����ʽ��_____________�����¶ȴ���80��ʱ��ˮ���������ӵ���Ũ�Ȼή�ͣ���ԭ����_____________��
���𰸡�(10��)
(1)����ˮ���������ȵ�Ũ�ȣ�ͬʱ������ˮΪ���ԣ��ή����Һ��pH�������ᵼ��ϸ����ˮ�������ֳ���� H2O2 +HClO=HCl+ O2��+H2O��
(2)���ؽ���ʹ�����ʱ��ԣ���Ͼ��ȣ��������ԣ���CO32������������Һ�е������ӣ�������CO2 ����ֱ���ų���ϵ��ͬʱ̼������Һ�Լ��ԣ�CO32��+ H2O![]() HCO3��+OH��������������Һ�������Ե�Ŀ�ģ���Al3++ 3H2O
HCO3��+OH��������������Һ�������Ե�Ŀ�ģ���Al3++ 3H2O![]() Al(OH)3(����)+3 H+���¶����ߣ�Al3++ 3H2O
Al(OH)3(����)+3 H+���¶����ߣ�Al3++ 3H2O![]() Al(OH)3(����)+ 3H+ƽ�������ƶ�������Al(OH)3������
Al(OH)3(����)+ 3H+ƽ�������ƶ�������Al(OH)3������
��������
���������(1)������������Ϣ����ˮ���������ȵ�Ũ�ȣ�ͬʱ������ˮΪ���ԣ��ή����Һ��pH�������ᵼ��ϸ����ˮ�������ֳ�����¶����Ӿ��ˮ���������������(28~30��)�ᵼ�����������ֳ���ʴ�Ϊ����ˮ���������ȵ�Ũ�ȣ�ͬʱ������ˮΪ���ԣ��ή����Һ��pH�������ᵼ��ϸ����ˮ�������ֳ��
����������H2O2������Ӧ��������Ļ�ѧ����ʽΪH2O2 +HClO=HCl+ O2��+H2O���ʴ�Ϊ��H2O2 +HClO=HCl+ O2��+H2O��
(2)��CuSO4��ҺҲ�ܹ�ɱ������ԭ�����ؽ���ʹ�����ʱ��ԡ�����CuSO4��Һ����Ҫ��ˮѭ��ϵͳ��������Һ���Ͼ��ȣ��ʴ�Ϊ���ؽ���ʹ�����ʱ��ԣ���Ͼ��ȣ�
������������ɱ�������������˺�������������ǿ�����ԣ��ʴ�Ϊ�������ԣ�
��CO32������������Һ�е������ӣ�������CO2 ����ֱ���ų���ϵ��ͬʱ̼������Һ�Լ��ԣ�CO32��+ H2O![]() HCO3��+OH��������������Һ�������Ե�Ŀ�ģ��ʴ�Ϊ��CO32������������Һ�е������ӣ�������CO2 ����ֱ���ų���ϵ��ͬʱ̼������Һ�Լ��ԣ�CO32��+ H2O
HCO3��+OH��������������Һ�������Ե�Ŀ�ģ��ʴ�Ϊ��CO32������������Һ�е������ӣ�������CO2 ����ֱ���ų���ϵ��ͬʱ̼������Һ�Լ��ԣ�CO32��+ H2O![]() HCO3��+OH��������������Һ�������Ե�Ŀ�ģ�
HCO3��+OH��������������Һ�������Ե�Ŀ�ģ�
���ۺ��Ȼ���ˮ�����������������壬�ɽ�������ͱ�ɱ���ϸС����������صף������ӷ�Ӧ����ʽΪAl3++ 3H2O![]() Al(OH)3(����)+3 H+���¶����ߣ�Al3++ 3H2O
Al(OH)3(����)+3 H+���¶����ߣ�Al3++ 3H2O![]() Al(OH)3(����)+ 3H+ƽ�������ƶ�������Al(OH)3������ʹ��ˮ���������ӵ���Ũ�Ȼή�ͣ��ʴ�Ϊ��Al3++ 3H2O
Al(OH)3(����)+ 3H+ƽ�������ƶ�������Al(OH)3������ʹ��ˮ���������ӵ���Ũ�Ȼή�ͣ��ʴ�Ϊ��Al3++ 3H2O![]() Al(OH)3(����)+3 H+���¶����ߣ�Al3++ 3H2O
Al(OH)3(����)+3 H+���¶����ߣ�Al3++ 3H2O![]() Al(OH)3(����)+ 3H+ƽ�������ƶ�������Al(OH)3������
Al(OH)3(����)+ 3H+ƽ�������ƶ�������Al(OH)3������


 ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���շ���͡��һ�ֵ���Ѫ֬��ҩ���ṹ��ͼ��ʾ��δ��ʾ����ռ乹���������й����շ���͡������������ȷ������ ��

A������ͨ����Ӧ�γɸ߷��ӻ����� B������ʹ����KMnO4��Һ��ɫ
C���ܷ����ӳɡ�ȡ������ȥ��Ӧ D��1 mol������������1 mol NaOH��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵķ��뷽���У��������ܶȲ�ͬ������ǣ� ��
A.��ʯ�;���������Ϊ���͡�ú�ͺͲ��͵�
B.����ҩʱ��ˮ�������������ȡ��ҩ����Ч�ɷ�
C.�Ѵ�ĥ�����ˮ�ܽ����еĿ����Գɷ֣������˺ֳɶ����Ͷ���
D.����ϴ��ʱ��ȥ���е�ɳ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�е缫a��b�ֱ�ΪAg�缫��Pt�缫���缫c��d����ʯī�缫��ͨ��һ��ʱ�����c��d�����Ϲ��ռ���336 mL (��״��)��������c��d�������������������Ϊ1��2�ش�
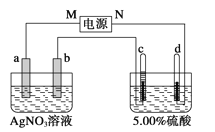
(1)ֱ����Դ�У�MΪ__________����
(2)Pt�缫�����ɵ�������________��������Ϊ_______g��
(3)��Դ����ĵ��ӣ������ʵ�����缫b��c��d�ֱ����ɵ����ʵ����ʵ���֮��Ϊ2��_________��_________��_________��
(4)AgNO3��Һ��Ũ��________(���������С�����䡱����ͬ)��AgNO3��Һ��pH_________�������Ũ��______________________�������pH________��
(5)�����������������5.00%��Ϊ5.02%����ԭ��5.00%������________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л��������˵������ȷ���� ( )
A. ���ȱ��������ȱ����������
B. C2H6��C6 H14һ����Ϊͬϵ��
C. ʯ���ѽ����֬���������ɸ߷�����������С�������ʵĹ���
D. �����������Ӧ�͵����ʵ�ˮ�ⷴӦ������ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�У�A��B��C��D��E�ǵ��ʣ�G��H��I��F��B��C��D��E�ֱ��A�γɵĶ�Ԫ�����
��֪���ٷ�ӦC+G![]() B+H�ܷų��������ȣ��÷�Ӧ��Ӧ��������ĺ��ӣ�
B+H�ܷų��������ȣ��÷�Ӧ��Ӧ��������ĺ��ӣ�
��I��һ�ֳ������������壬����E���Է�����Ӧ��2E+I![]() 2F+D��F��EԪ�ص���������Ϊ60%��
2F+D��F��EԪ�ص���������Ϊ60%��
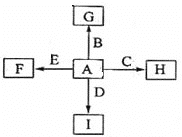
�ش����⣺
�Ţ��з�Ӧ�Ļ�ѧ����ʽΪ______________��
�ƻ�����I�ĵ���ʽΪ_______�����Ŀռ�ṹ��______��
��C�����NaOH��Һ��Ӧ�����ӷ���ʽΪ____________����Ӧ�����������������I��Ӧ�����ӷ���ʽΪ____________________��
��E��I��ȼ�չ۲쵽��������_____________________��
��1.6gG�������ᣬ�õ�����Һ��ͭ����ȫ��Ӧ���������������ͭ�۵�����_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����������з�Ӧ��2Cu��=Cu2����Cu��������ԭ����ͭʵ�����ڷ�Ӧ�¶Ȳ�ͬ�����ܲ���Cu��Cu2O�����߶��Ǻ�ɫ���塣ijͬѧ��ij��������ԭ����ͭ�ĺ�ɫ���������������ʵ�飬ʵ�������ʵ�������б����£�
���� �Լ� | ϡ���� | Ũ���� ������ | ϡ���� | Ũ���� |
ʵ�� ���� | ��ɫ���� ����Ӧ | ��ɫ���� | ��ɫ���� ��ɫ��Һ | ����ɫ���� ��ɫ��Һ |
�ɴ��Ƴ�����������ԭ����ͭʵ��IJ���(����)
A. ��Cu B. ��Cu2O C. һ����Cu��һ����Cu2O D. һ����Cu2O��������Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
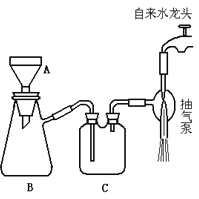
����Ŀ������ʵ�������п���ֱ�Ӽ��ȵ��ǣ�
A. �Թ� B. ����ƿ C. ��Ͳ D. ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ��������и��⣺
��1��KOH�ĵ���ʽ��___��CH��CH3��3������Ϊ��______��
��2�����������ʣ���Cu����H2CO3����BaSO4�������ᡢ��SO2���������������___������ţ���ͬ�����ǵ������___��
��3������ˮ��Ӧ�Ļ�ѧ����ʽΪ��____________��
��֪�ڹ�����FeSO4��Һ�е��뼸��NaClO��Һ�����������H2SO4����Һ������ƣ���д���÷�Ӧ�����ӷ���ʽ��__________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com