
【题目】下列关于原子结构及元素周期表的说法错误的是
A.ⅡA族基态原子最外层电子排布均为ns2
B.第三、第四周期同主族元素的原子序数均相差8
C.第四周期ⅡA族与ⅢA族元素的原子序数相差11
D.基态原子3d轨道上有5个电子的元素位于ⅥB族或ⅦB族
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,在3个体积均为1.0 L的恒容密闭容器中反应2H2(g)+CO(g) ![]() CH3OH(g) 达到平衡,下列说法错误的是( )
CH3OH(g) 达到平衡,下列说法错误的是( )
容器 | 温度/K | 物质的起始浓度/mol·L-1 | 物质的平衡浓度/mol·L-1 | ||
c(H2) | c(CO) | c(CH3OH) | c(CH3OH) | ||
Ⅰ | 400 | 0.20 | 0.10 | 0 | 0.080 |
Ⅱ | 400 | 0.40 | 0.20 | 0 | |
Ⅲ | 500 | 0 | 0 | 0.10 | 0.025 |
A. 该反应的正反应放热
B. 达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的小
C. 达到平衡时,容器Ⅱ中c(H2)大于容器Ⅲ中c(H2)的两倍
D. 达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中NO产生的反应为:N2(g)+O2(g)![]() 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是:
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是:

A. 温度T下,该反应的平衡常数K=![]()
B. 温度T下,随着反应的进行,混合气体的密度减小
C. 曲线b对应的条件改变可能是加入了催化剂
D. 若曲线b对应的条件改变是温度,可判断该反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物结构的说法错误的是
A.环己烷中所有C—C—C键角均为120°
B.CnH2n+1Cl与CnHCl2n+1同分异构体数目相同
C.C原子与N原子之间可形成单键、双键和叁键
D.含有手性碳原子的饱和链烃中,碳原子数最少的一定是3-甲基己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题: 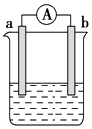
(1)当电极a为Al,电极b为Cu,电解质溶液为浓硝酸时,正极的电极反应式为: .
(2)当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该电池的正极为 , 负极的电极反应式为: , 当反应中收集到标准状况下448mL气体时,消耗的电极质量为g.
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所产生的能量直接转化为电能.现设计一燃料电池,以电极a为正极,电极b为负极,乙醇(C2H5OH)为燃料,采用氢氧化钠溶液为电解液,则乙醇应通入极(填“a”或“b”),该电极的电极反应式为: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com