



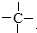 ”,且当两“-CH3”上的H再被一个同种卤素原子取代成为二卤代烃时,只能得到一种结构.回答下列问题:
”,且当两“-CH3”上的H再被一个同种卤素原子取代成为二卤代烃时,只能得到一种结构.回答下列问题: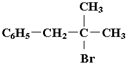

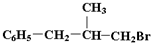
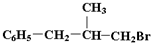


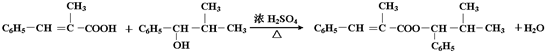
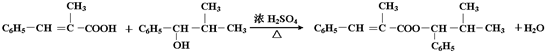
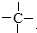 ”,且当两“-CH3”上的H再被一个同种卤素原子取代成为二卤代烃时,只能得到一种结构,说明两个甲基在同一个碳原子上,所以H的结构简式为
”,且当两“-CH3”上的H再被一个同种卤素原子取代成为二卤代烃时,只能得到一种结构,说明两个甲基在同一个碳原子上,所以H的结构简式为 ;
;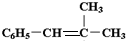 ,I和氢溴酸、臭氧反应生成J,J的结构简式为
,I和氢溴酸、臭氧反应生成J,J的结构简式为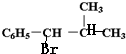 ,A、H、J是同分异构体,所以A的结构简式为
,A、H、J是同分异构体,所以A的结构简式为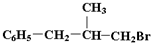 ,则B的结构简式为:
,则B的结构简式为: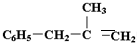 ;J和氢氧化钠的水溶液发生取代反应生成K,则K的结构简式为:
;J和氢氧化钠的水溶液发生取代反应生成K,则K的结构简式为: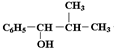 ;
;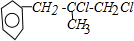 ,C和氢氧化钠的水溶液发生取代反应生成D,D的结构简式为:
,C和氢氧化钠的水溶液发生取代反应生成D,D的结构简式为: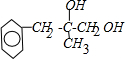 ,D被氧气氧化生成E,E的结构简式为:
,D被氧气氧化生成E,E的结构简式为: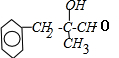 ,E被新制氢氧化铜氧化生成F,F的结构简式为:
,E被新制氢氧化铜氧化生成F,F的结构简式为: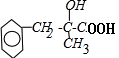 ,F在加热、浓硫酸催化作用下发生消去反应生成G,G的结构简式为:
,F在加热、浓硫酸催化作用下发生消去反应生成G,G的结构简式为: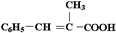 ,G和K发生酯化反应生成L,L的结构简式为:
,G和K发生酯化反应生成L,L的结构简式为: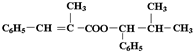 .
.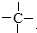 ”,且当两“-CH3”上的H再被一个同种卤素原子取代成为二卤代烃时,只能得到一种结构,说明两个甲基在同一个碳原子上,所以H的结构简式为
”,且当两“-CH3”上的H再被一个同种卤素原子取代成为二卤代烃时,只能得到一种结构,说明两个甲基在同一个碳原子上,所以H的结构简式为 ;
;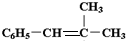 ,I和氢溴酸、臭氧反应生成J,J的结构简式为
,I和氢溴酸、臭氧反应生成J,J的结构简式为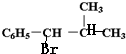 ,A、H、J是同分异构体,所以A的结构简式为
,A、H、J是同分异构体,所以A的结构简式为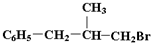 ,则B的结构简式为:
,则B的结构简式为: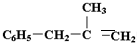 ;J和氢氧化钠的水溶液发生取代反应生成K,则K的结构简式为:
;J和氢氧化钠的水溶液发生取代反应生成K,则K的结构简式为: ;
;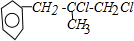 ,C和氢氧化钠的水溶液发生取代反应生成D,D的结构简式为:
,C和氢氧化钠的水溶液发生取代反应生成D,D的结构简式为: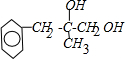 ,D被氧气氧化生成E,E的结构简式为:
,D被氧气氧化生成E,E的结构简式为: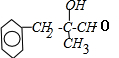 ,E被新制氢氧化铜氧化生成F,F的结构简式为:
,E被新制氢氧化铜氧化生成F,F的结构简式为: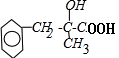 ,F在加热、浓硫酸催化作用下发生消去反应生成G,G的结构简式为:
,F在加热、浓硫酸催化作用下发生消去反应生成G,G的结构简式为: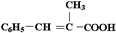 ,G和K发生酯化反应生成L,L的结构简式为:
,G和K发生酯化反应生成L,L的结构简式为: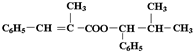 .
. 、
、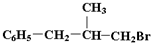 ,
, ;
;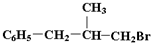 ;
;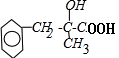 ,所以F中含有羟基和羧基,L的结构简式为:
,所以F中含有羟基和羧基,L的结构简式为: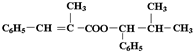 ,所以L通过聚合反应生成高分子化合物,
,所以L通过聚合反应生成高分子化合物, ,
, ;
;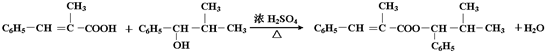 ,
,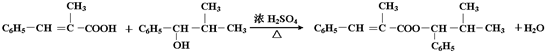 .
.

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| 离子 | 开始沉淀时的pH | 完全沉淀时的pH | 加碱溶解的pH |
| Fe2+ | 7.6 | 9.7 | |
| Fe3+ | 2.7 | 3.7 | |
| Al3+ | 3.8 | 4.7 | >8.5 |
| Mn2+ | 8.3 | 9.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com