
 ______
______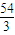 =18,则为Ca2+、Cl-,故XY2是CaCl2;
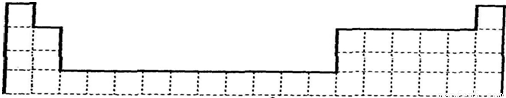
=18,则为Ca2+、Cl-,故XY2是CaCl2;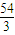 =18,则为Ca2+、Cl-,故XY2是CaCl2,则Ca、Cl的位置为
=18,则为Ca2+、Cl-,故XY2是CaCl2,则Ca、Cl的位置为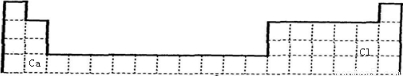 ,
,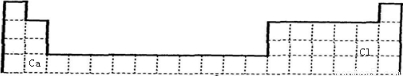 ;
;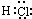 ,故答案为:6;
,故答案为:6;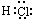 ;
; 

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:




查看答案和解析>>
科目:高中化学 来源: 题型:





查看答案和解析>>
科目:高中化学 来源: 题型:
在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
(1)该融雪剂的化学式是 ;Y的最高价氧化物的水化物中含有的化学键是 。
(2)元素D原子的最外层电子数是其电子层数的2倍,且D与Y相邻;E是短周期最活泼的金属元素,试用电子式表示D与E组成化合物的形成过程为 。
(3)元素W与Y同周期,其氧化物可作为太阳能电子板的材料;元素Z的单质分子Z2中有3个共价键;W与Z能形成一种新型无机非金属材料,其化学式是________ _________。
(4)W的氧化物是玻璃的主要成分,易与烧碱反应,该反应的化学方程式为:
_______________________ ______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com