
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如右图所示。若Y原子的最外层电子数是次外层 电子数的3倍,下列说法中正确的是
电子数的3倍,下列说法中正确的是


A.原子半径:W>Z>Y>X
B.最高价氧化物对应水化物的酸性:Z>W>X
C.四种元素的单质中,Z单质的熔、沸点最低
D.W的单质能与水反应,生成一种具有漂白性的物质
【答案】D
【解析】
试题分析:根据元素在周期表中的相对位置可知,Y是第二周期元素。由于Y原子的最外层电子数是次外层电子数的3倍,所以Y是氧元素。则X是氮元素,Z是硫元素,W是氯元素。A、同周期自左向右原子半径逐渐减小。同主族自上而下原子半径逐渐增大,因此原子半径:Z>W>X>Y,A不正确;B、非金属性越强,最高价氧化物对应水化物的酸性越强。非金属性是W>X>Z,所以最高价氧化物对应水化物的酸性:W>X>Z,B不正确;C、常温下只有单质S是固体,因此四种元素的单质中,Z单质的熔、沸点最高,C不正确;D、氯气溶于水生成氯化氢与次氯酸,其中次氯酸可以作为漂白剂,D正确,答案选D。
考点:考查元素周期表的结构、元素周期律的应用


科目:高中化学 来源: 题型:
A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素符号:
A ,B ,C ,D ,E
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程: 。
(3)写出A、B两元素最高价氧化物的水化物反应的离子方程式: 。
(4)比较C、D的最高价氧化物的水化物的酸性:(用化学式表示) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
以溴乙烷为原料制备1,2二溴乙烷,下列方案中最合理的是( )
A.CH3CH2Br CH3CH2OH
CH3CH2OH CH2===CH2
CH2===CH2 CH2BrCH2Br
CH2BrCH2Br
B.CH3CH2Br CH2BrCH2Br
CH2BrCH2Br
C.CH3CH2Br CH2===CH2
CH2===CH2 CH2BrCH3
CH2BrCH3 CH2BrCH2Br
CH2BrCH2Br
D.CH3CH2Br CH2===CH2
CH2===CH2 CH2BrCH2Br
CH2BrCH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法均摘自学生的作业本,你认为无科学性错误的是
A.煤的气化、液化都是化学变化,可为人类提供清洁高效的燃料
B.氯化氢、氯气、二氧化氮、生石灰溶于水都有化学键被破坏的变化,都属于化学变化
C.苯酚、纯碱、胆矾和OF2分别属于酸、碱、盐和氧化物
D.二氧化碳、氨气、氯气都是非电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
制备水杨酸对正辛基苯基酯( )如下:
)如下:
步骤一:将水杨酸晶体投 入三颈烧瓶中,再加入氯苯,搅拌溶解后,加入无水三氯化铝。
入三颈烧瓶中,再加入氯苯,搅拌溶解后,加入无水三氯化铝。
步骤二:按图12所示装置装配好仪器,水浴加热控制温度在20~40℃之间,在搅拌下滴加SOCl2,反应制得水杨酰氯,该反应为:
 (水杨酸)+SOCl2→
(水杨酸)+SOCl2→ (水杨酰氯)+HCl↑+SO2↑
(水杨酰氯)+HCl↑+SO2↑


步骤三:将三颈烧瓶中的混合液升温至80℃,再加入对正辛苯酚[ ],温度控制在100℃左右,不断搅拌。
],温度控制在100℃左右,不断搅拌。
步骤四:过滤、蒸馏、减压过滤;酒精洗涤、干燥。
(1)步骤一中加入三氯化铝的作用是 。
(2)实验时,冷凝管中的水应从 进 出(选填“a”或“b”);装置c的作用是 。
(3)步骤三中发生反应的化学方程式为  。
。
(4)步骤四减压过滤操作中,除烧杯、玻璃棒外,还必须使用的硅酸盐材料的仪器有 。
(5)步骤四减压过滤时,有时滤纸会穿孔,避免滤纸穿孔的措施是 。
【答案】(1)催化剂(2分) (2)a b(2分);吸收HCl、SO2(2分)
(3) (2分)
(2分)
(4)布氏漏斗、吸滤瓶(2分) (5)减小真空度或者加一层(或多层)滤纸(2分)
查看答案和解析>>
科目:高中化学 来源: 题型:
(一)化学与生活(15分)
(1)良好的生态环境可以提升生活质量。
①空气污染指数API表明了空气的质量。空气污染指数主要是根据空气中 ▲ 、NO2、CO和可吸入颗粒物等污染物的浓度计算出来的数值。
②下列物质可用作混凝剂是 ▲ (填字母)。
a.ClO2 b.FeCl3 c.Ca(ClO)2
③氮氧化物可用氨气处理。已知,氨气与二氧化氮在一定条件下反应可生成对空气无污染的物质,则该反应的化学方程式为 ▲ 。
(2)均衡的膳食结构可以保障身体健康。
①下列维生素中,能防治夜盲症的是 ▲ ,能预防佝偻病的是 ▲ ,能防治坏血病的是 ▲ 。(填字母)
a.维生素A b.维生素C c.维生素D
②葡萄糖在人体内被氧化,最终生成 ▲ 和 ▲ ,同时释放出能量。
(3)材料的不断发展可以促进社会进步。
①下列属于复合材料的是 ▲ (填字母)。
a.石灰石 b.普通玻璃 c.钢筋混凝土
② ABS塑料可用于制造电视机、洗衣机的外壳,ABS塑料属于 ▲ (填字母)。
a.有机高分子材料 b.无机非金属材料 c.金属材料
③制造下列物质时,不需要石灰石的是 ▲ (填字母)。
a.生石灰 b.水泥 c.光导纤维
④黄铜的主要组成元素是铜和 ▲ (填元素名称)。铁器件在潮湿的空气中会发生 ▲ 腐蚀(填“化学”或“电化学”),为防止铁质地下管道的腐蚀可在其表面附着 ▲ (填“锌块”或“石墨”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
利用化合价和物质类别推测物质的性质是化学研究的重要手段。
(1)从化合价的角度可以预测物质的性质。
①将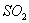 通入酸性
通入酸性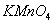 溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是__________A.
溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是__________A.  B.
B. 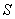 C.
C. 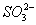 D.
D. 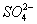
②亚硫酸钠中的硫呈+4价,它既有氧化性又有还原性,现有试剂:溴水、H2S、稀硫酸。
请选取合适的试剂证明Na2SO3具有还原性, 并写出该反应的离子方程式为:________________________________________________.
(2)从物质分类的角度可以推测物质的性质。
①已知蛇纹石由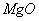 、
、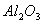 、
、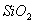 、
、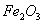 组成。其中属于碱性氧化物的是______________________________。
组成。其中属于碱性氧化物的是______________________________。
②现取一份蛇纹石试样进行实验:
I. 先将其溶于过量的盐酸中、过滤,滤渣的主要成分是_________。
II. 再向滤液中加入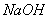 溶液至过量、过滤,滤渣中的主要成分是_________。
溶液至过量、过滤,滤渣中的主要成分是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com