
不能用带橡胶塞的玻璃试剂瓶存放的药品是( )
①浓硝酸 ②稀氢氧化钠溶液 ③液溴 ④纯碱溶液 ⑤水玻璃 ⑥氢氟酸
A.①③⑥ B.①④⑥ C.①⑤⑥ D.②③④⑤
 口算能手系列答案
口算能手系列答案科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 物质的组成性质分类及化学用语练习卷(解析版) 题型:选择题
等质量的镁在足量的(1)O2、(2)N2、(3)CO2、(4)空气中燃烧,生成固体物质的质量从大到小顺序正确的是( )
A.(1)(2)(3)(4) B.(1)(2)(4)(3) C.(2)(3)(4)(1) D.(3)(1)(4)(2)
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 化工生产流程、无机物的判断练习卷(解析版) 题型:选择题
X、Y、Z、W四种物质的转化关系如图所示。下列组合中不符合该关系的是( )

ABCD
XHClNa2O2Na2CO3SO2
YFeCl2NaOHCO2Na2SO3
ZCl2Na2CO3CaCO3H2SO4
WFeCl3NaHCO3Ca(HCO3)2NaHCO3
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 化学实验基础练习卷(解析版) 题型:选择题
用试纸检验气体性质是一种重要的实验方法。如图所示的实验中(可加热),下列试剂的选用、现象、对应结论都正确的一项是( )
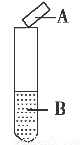
选项试剂B湿润的试纸A现象结论
A碘水淀粉试纸变蓝碘具有氧化性
B浓氨水,生石灰蓝色石蕊试纸变红氨气为碱性气体
CNa2SO3,硫酸品红试纸褪色SO2具有漂白性
DCu,浓硝酸KI-淀粉试纸变蓝NO2为酸性气体
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 化学实验基础练习卷(解析版) 题型:选择题
下列实验操作与预期实验目的或实验结论不一致的是( )
选项实验操作及现象实验目的或结论
A用硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色可证明氧化性:H2O2比Fe3+强
B在0.1 mol/L的NaHCO3溶液中,加2滴酚酞显浅红色,微热,溶液颜色加深 验证盐类水解反应是吸热反应
C将一定量的NaNO3和KCl的混合液加热并浓缩至有晶体析出,趁热过滤 得到NaCl晶体
D苯酚钠溶液中通入足量二氧化碳产生浑浊苯酚的酸性弱于碳酸
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 化学基本理论练习卷(解析版) 题型:选择题
金属冶炼与处理常涉及氧化还原反应。
(1)由下列物质冶炼相应金属时采用电解法的是________。
a. Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)辉铜矿(Cu2S)可发生反应:2Cu2S+2H2SO4+5O2=4CuSO4+2H2O,该反应的还原剂是________。当1 mol O2发生反应时,还原剂所失电子的物质的量为________mol。向CuSO4溶液中加入镁条时有气体生成,该气体是________。

(3)右图为电解精炼银的示意图,________(填“a”或“b”)极为含有杂质的粗银,若b极有少量红棕色气体产生,则生成该气体的电极反应式为________。
(4)为处理银器表面的黑斑(Ag2S),将银器浸于铝质容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用是________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 化学基本理论练习卷(解析版) 题型:选择题
常温下,对下列电解质溶液的有关说法正确的是( )
A.相同浓度和体积的强碱和强酸溶液混合后,溶液的pH一定等于7
B.在NaHCO3溶液中,c(CO32—)>c(HCO3—)
C.在有AgCl沉淀的溶液中加入NaCl固体,c(Ag+)减小
D.将pH相等的CH3COONa和Na2CO3溶液稀释相同倍数,CH3COONa溶液的pH较大
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 化学基本概念练习卷(解析版) 题型:填空题
某工业废水仅含下表中的某些离子,且各种离子的物质的量浓度相等,均为0.1 mol/L(此数值忽略水的电离及离子的水解)。
阳离子 | K+ Ag+ Mg2+ Cu2+ Al3+ NH4+ |
阴离子 | Cl- CO32— NO3— SO42— I- |
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.取该无色溶液5 mL,滴加一滴氨水有沉淀生成,且离子种类增加。
Ⅱ.用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰。
Ⅲ.另取溶液加入过量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是___________________________________。
(2)Ⅲ中加入盐酸生成无色气体的离子方程式是________________________。
(3)甲同学最终确定原溶液中所含阳离子有________,阴离子有________;并据此推测原溶液应该呈________性,原因是____________________________(请用离子方程式说明)。
(4)另取100 mL原溶液,加入足量的NaOH溶液,此过程中涉及的离子方程式为____________________________。充分反应后过滤,洗涤,灼烧沉淀至恒重,得到的固体质量为________g。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 化学与技术练习卷(解析版) 题型:填空题
钛铁矿的主要成分为FeTiO3(可表示为FeO·TiO2),含有少量MgO、CaO、SiO2等杂质。利用钛铁矿制备锂离子电池电极材料(钛酸锂Li4Ti5O12和磷酸亚铁锂LiFePO4)的工业流程如图所示:

已知:FeTiO3与盐酸反应的离子方程式为FeTiO3+4H++4Cl-=Fe2++TiOCl42—+2H2O
(1)化合物FeTiO3中铁元素的化合价是________。
(2)滤渣A的成分是________。
(3)滤液B中TiOCl42—转化生成TiO2的离子方程式是________________。
(4)反应②中固体TiO2转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如图所示。反应温度过高时,Ti元素浸出率下降的原因是________________________________。

(5)反应③的化学方程式是________________________。
(6)由滤液D制备LiFePO4的过程中,所需17%双氧水与H2C2O4的质量比是________。
(7)若采用钛酸锂(Li4Ti5O12)和磷酸亚铁锂(LiFePO4)做电极组成电池,其工作原理为Li4Ti5O12+3LiFePO4 Li7Ti5O12+3FePO4,该电池充电时阳极反应式是____________________。
Li7Ti5O12+3FePO4,该电池充电时阳极反应式是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com