
ijУ��ȤС��ͬѧ��һ��Ũ�ȵ����Ȼ�����Һ��ʴ����ͭ���ľ�Ե�壬�Ƴ�ӡˢ��·�壬�йط�ӦΪ��2FeCl3��Cu��2FeCl2��CuCl2���ֽ�һ�����ͭ���ľ�Ե�����200mLijFeCl3��ҺA�У�һ��ʱ��Ѹ���·��ȡ������������ҺB�м����������۳�ַ�Ӧ��ʣ������˳�������ҺC(���Է�Ӧǰ����Һ����ı仯)��ȡ��20.0mL������ȡ��Һ�е���0.600mol��L��1 AgNO3��Һ100mL����ʱ����Һ�е�������ǡ����ȫ������
�Լ��㣺
(1)��ҺA��FeCl3�����ʵ���Ũ�ȣ�
(2)�������۲����ܽ⣬����ҺB�м����������������Ӧ���ڶ��ٿˣ�
|
����(1)��Ϊ��Ag+��Cl����AgCl�� �������ԣ�n(Fe3+)�� ������ ������c(Fe3+)�� ��������ҺA��FeCl3�����ʵ���Ũ����1.00mol��L��1�� ����(2)��Ϊ��2Fe3+��Cu��2Fe2+��Cu2+��Cu2+��Fe��Fe2+��Cu�� ����2Fe3+��Fe��3Fe2+�� ���������������۵���������n(Fe3+)ֱ�Ӽ��㣺 ����n(Fe)��n(Fe3+)/2�� ����m(Fe)��56g��mol��1��0.100mol��5.60g ����������ҺB�м����������������Ӧ����5.60g�� |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
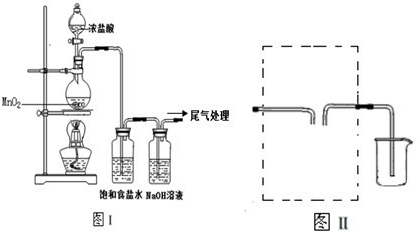
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
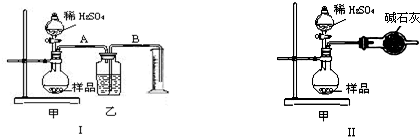
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�걱���ж����������ڶ�ѧ���ۺ���ϰ��������ѧ�Ծ��������棩 ���ͣ�ʵ����
ijУ��ȤС������ͼ��װ����ȡƯ��Һ���������Ѽ��飬�Լ������ӣ������о���������ʡ�
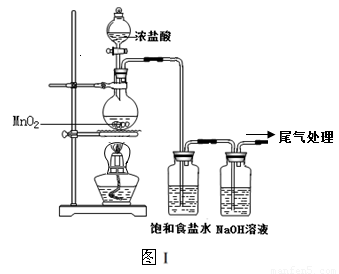
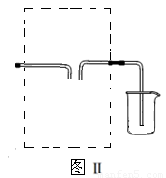
ʵ�����������Һ©���Ļ����������μ�һ����Ũ���ᣬ��ȼ�ƾ��ƣ�һ��ʱ��رշ�Һ©���Ļ�����Ϩ��ƾ��ơ�
��1����ƿ�з�Ӧ�Ļ�ѧ����ʽ�� ��
��2������ʳ��ˮ�������� ��
��3������ͼ��װ���ռ�������������������߿��ڻ�����װ�ü�ͼ��
��4����С��ͬѧ������װ���Ƶõ�Ư��Һ��NaClO��Ũ��ƫ�͡�
�������ϣ�����Һ�з�����Ӧ��
��a��Cl2��g����2NaOH��aq���T NaCl��aq����NaClO��aq����H2O��l��H1=��101.1kJ/mol
��b��3NaClO��aq���T2NaCl��aq����NaClO3��aq��H2=��112.2kJ/mol
��Ӧ��a���ķ�Ӧ���ʺܿ죬��Ӧ��b���������½���
�������ϣ����ͼ��װ������Ľ����飺 ��
��5���ķ�����С��ͬѧ�Ƶ��˽ϸ�Ũ�ȵ�NaClO��Һ�����ǰ�Ư��Һ�͵��з�̪�ĺ�ɫNa2SO3��Һ��Ϻõ���ɫ��Һ��
������룺����NaClO��Na2SO3������
����NaClO�ѷ�̪������
����NaClO��Na2SO3�ͷ�̪��������
������ʵ�鷽���п���֤��NaClO������Na2SO3���� ��
a�����Ϻ����Һ�м����������
b�����Ϻ����Һ�м���������ᣬ�ټ����Ȼ�����Һ
c�����Ϻ����Һ�м���������ᣬ�ټ�����������Һ
d�����Ϻ����Һ�м�������������Һ���ټ����������
��Ϊ֤��NaClO�����˷�̪���ɽ��е�ʵ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���Ĵ�ʡģ���� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com