
【题目】下列离子方程式的书写正确的是
A. 漂白粉溶液中通入SO2气体:Ca2++2ClO-+SO2+H2O===CaSO3↓+2HClO
B. 碳酸氢钙溶液中加入过量的氢氧化钠溶液:HCO![]() +OH-===CO
+OH-===CO![]() +H2O
+H2O
C. 向Fe2(SO4)3溶液中加入过量铁粉:2Fe3++Fe===3Fe2+
D. 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+===H2SiO3↓+2Na+
科目:高中化学 来源: 题型:
【题目】某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响,在常温下按照如下方案完成实验。
实验编号 | 反应物 | 催化剂 |
① | 10 mL 2% H2O2溶液 | 无 |
② | 10 mL 5% H2O2溶液 | 无 |
③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol L-1 FeCl3溶液 |
④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol L-1 FeCl3溶液 |
⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol L-1 FeCl3溶液 |
(1)催化剂能加快化学反应速率的原因是。
(2)实验①和②的目的是。实验时由于较长时间没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是。
(3)写出实验③的化学反应方程式:。
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图。分析如图能够得出的实验结论是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同分异构现象是有机物种类繁多的重要原因之一,下列互为同分异构体的一组化合物是( )
A.甲烷和乙烷
B.乙醇和乙酸
C.正丁烷和异丁烷
D.氯乙烯和乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】立足教材实验是掌握高中化学实验的基础,是理解化学科学的实验原理、实验方法和实验思路,提高学生实验能力的基本途径:
(1)实验1:取一块金属钠,在玻璃片上用滤纸吸干表面的煤油后,用小刀切去一端的外皮,观察钠的颜色,这个实验中还需用到的一种仪器是_________;
(2)实验2:向一个盛有水的小烧杯里滴入几滴酚酞试液,然后把一小块钠投入小烧杯,把反应的现象和相应结论填入空格,“浮”--钠的密度比水小;“红”--反应生成了氢氧化钠;“熔”——______________;
(3)实验3:用坩埚钳夹住一小块用砂纸仔细打磨过的铝,在酒精灯上加热至熔化,发现熔化的铝并不滴落。下列关于上述实验现象的解释正确的是_________
A.火焰温度太低不能使铝燃烧 B.铝在空气中能很快形成氧化膜
C.氧化铝的熔点比倡的熔点高 D.打磨砂纸不能除去表面的氧化膜
(4)实验4:把少量水滴入盛有Na2O2固体的试管中,立即用带火星的木条放在试管口,检验
生成的气体体,向反应后的溶液中加入酚酞试液,可以看到__________;
(5)实验5:在玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,该氧化还原反应的氧化剂是__________,该反应每消耗1mol铁,转移电子的物质的量为_________。
(6)实验6:在试管中注入少量新制备的FeSO4溶液,用胶头滴管吸取NaOH溶液,将滴管尖端插入试管里溶液底部,慢慢挤出NaOH溶液,可以看到开始时析出一种白色的絮状沉淀,并迅速变成灰绿色,最后变成红褐色,发生这种颜也变化的原因是(用化学方程式表示):______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为了探究常温下非金属氧化物形成的某未知气体的成分。该小组成员将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想。
[提出猜想]
猜想1:该气体为CO2
猜想2:该气体为SO2
猜想3:____________________________________
为了验证猜想,该小组设计实验加以探究:
[实验探究]
该小组同学按如图所示装置,将气体从a端通入,则:
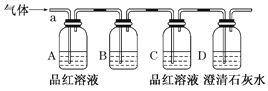
(1)B中应该装的试剂是:__________________________。
(2)A中品红溶液的作用是:_________________________________________。
(3)根据B的作用和B中的现象,证明SO2具有的性质是:_________________。
(4)D中澄清石灰水的作用是:_________________________________________。通过该实验,该小组同学观察到以下三个实验现象:
①A中品红溶液褪色 ②C中品红溶液不褪色 ③D中澄清石灰水变浑浊
[得出结论]
(5)由上述现象该小组同学确认该气体的成分:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用以下三种途径来制取等质量的硝酸铜。
①铜与稀硝酸反应;
②铜与浓硝酸反应;
③铜先与氧气反应生成氧化铜,氧化铜再跟硝酸反应。以下叙述不正确的是
A. 三种途径所消耗铜的质量相等
B. 三种途径所消耗硝酸的物质的量是①>②>③
C. 途径③的制备方法最符合“绿色化学”理念
D. 途径①中被氧化的铜与被还原的硝酸的物质的量之比是3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一元硬币的外观有银白色的金属光泽,一些同学认为它可能是铁制成的。在讨论时,有同学提出:“我们可以先拿磁铁来吸一下。”就“拿磁铁来吸一下”这一过程而言,属于科学探究中的
A.实验
B.比较
C.观察
D.分类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一套检验气体性质的实验装置示意图.如图所示,向装置中缓慢通入气体X,若关闭活塞K,则试管中的品红试液无变化,而烧杯中的石灰水变浑浊;若打开活塞K,则品红试液褪色.根据此现象判断,气体X和洗气瓶内液体Y可能是( ) 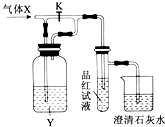
①X:H2S,Y:浓H2SO4
②X:SO2 , Y:饱和NaHCO3溶液
③X:CO2 , Y:Na2SO3溶液
④X:Cl2 , Y:饱和NaHCO3溶液.
A.③和④
B.②和④
C.①和②
D.②和③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com