
分析 (1)先根据溶液的pH计算氢氧根离子浓度,再根据c1V1=c2(V1+V2)计算加入的水体积;
(2)先根据溶液的pH计算氢氧根离子浓度,再根据c1V1+c2V2=c3(V1+V2)计算加入的氢氧化钠溶液体积;
(3)先计算混合溶液中氢氧根离子浓度,再根据c(OH-)=$\frac{n(O{H}^{-})-n({H}^{+})}{{V}_{酸}+{V}_{碱}}$进行解答.
解答 解:(1)pH=12 的NaOH溶液中氢氧根离子浓度为0.01mol/L,pH=11的氢氧化钠溶液中氢氧根离子浓度是0.001mol/L,设加入水的体积是V2,c1V1=c2(V1+V2)=0.01mol/L×0.1L=(0.1+V2)L,V2=$\frac{0.01mol/L×0.1L}{0.001mol/L}$=0.9L=900mL,
故答案为:900;
(2)pH=12 的NaOH溶液中氢氧根离子浓度是0.01mol/L,pH=11的氢氧化钠溶液中氢氧根离子浓度是0.001mol/L,pH=10的氢氧化钠溶液中氢氧根离子浓度是0.0001mol/L,
设加入pH=10的NaOH溶液体积是V2,
c1V1+c2V2=c3(V1+V2)=0.01mol/L×0.1L+0.0001mol/L×V2=0.001mol/L(0.1+V2),
V2=1L=1000mL,
故答案为:1000;
(3)0.008mol/L HCl溶液中氢离子浓度为0.008mol/L,设加入盐酸的体积为V,
c(OH-)=$\frac{0.01mol/L×0.1L-0.008mol/L×VL}{0.1L+VL}$=0.001mol/L,
解得:V=100mL.
故答案为:100.
点评 本题考查溶液pH的简单计算,题目难度中等,注意掌握溶液酸碱性与溶液pH的计算方法,明确酸碱中和反应实质为解答本题的关键,试题培养了学生的化学计算能力.


 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源: 题型:选择题
| A. | 在硫酸亚铁溶液中通入氧气:4Fe2++O2+4H+=4Fe3++2H2O | |
| B. | 用0.3mol/L的氯化铵溶液除去氢氧化铝中少量的氢氧化镁:Mg(OH)2+2NH4+=Mg2++2NH3•H2O | |
| C. | 向1mol明矾的水溶液当中加入氢氧化钡,当沉淀的质量最大时离子方程式科表示为:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O | |
| D. | 酸性高锰酸钾和过氧化氢制取少量氧气:4MnO4-+4H2O2+12H+=4Mn 2++7O2↓+10H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
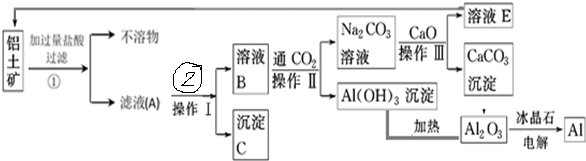
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑥ | B. | ②④⑤ | C. | ①②⑤ | D. | ②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 元素 | 相关信息 |
| A | 在常温、常压下,其单质是气体,随着人类对环境的认识和要求的提高,它将成为备受青睐的清洁燃料 |
| B | 工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障 |
| C | 植物生长三要素之一,它能形成多种氧化物,其中一种是早期医疗中使用的麻醉剂 |
| D | 室温下其单质为淡黄色粉末状固体,加热易熔化.该单质在氧气中燃烧,发出明亮的蓝紫色火焰 |
| E | 它在地壳中储量丰富,是人体不可缺少的微量元素之一.其单质为银白色固体,是工农业生产中不可或缺的金属材料,常用于机械制备、建筑等行业 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 和
和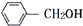 互为同系物,均可以与金属钠反应.
互为同系物,均可以与金属钠反应.| A. | .③④⑤⑥ | B. | ①②③④ | C. | ①②⑤⑥ | D. | ①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油裂解可以得到氯乙烯 | |
| B. | 油脂水解可得到氨基酸和甘油 | |
| C. | 所有烷烃和蛋白质中都存在碳碳单键 | |
| D. | 蔗糖和麦芽糖的组成都是C12H22O11,水解产物均含有葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向碳酸钠与碳酸氢钠的混合溶液逐滴滴入盐酸溶液,立即产生大量气泡 | |
| B. | 某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成,说明该溶液中有SO42- | |
| C. | 常温下,向0.1mol/L NaF和pH=12 NaOH的混合溶液中,滴加MgCl2溶液,先生成 MgF2沉淀(已知K[Mg(OH)]2=7.4×10-11 K( MgF2)=5.6×10-12) | |
| D. | 向 Fe(NO3)2溶液中滴入硫酸酸化的H2O2溶液,则溶液变黄,说明氧化性H2O2>Fe3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com